
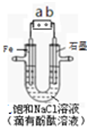
 如图是模拟工业电解饱和食盐水的装置图,下列叙述正确的是( )
如图是模拟工业电解饱和食盐水的装置图,下列叙述正确的是( )| A、a为电源的正极 |
| B、通电一段时间后,石墨电极附近溶液先变红 |
| C、Fe电极的电极反应是4OH--4e-═2H2O+O2↑ |
| D、电解饱和食盐水的总反应是:2NaCl+2H2O═2NaOH+H2↑+Cl2↑ |
| ||


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠与水反应:Na+2H2O=Na++2OH-+H2↑ |
| B、硅酸钠溶液与醋酸溶液反应:SiO32-+2H+=H2SiO3↓ |
| C、硫酸铝溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓ |
| D、浓硝酸中加入烧碱溶液:OH-+H+=H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、V3>V2>V1 |
| B、V3=V2=V1 |
| C、V3>V2=V1 |
| D、V1=V2>V3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、OH-、S042- |
| B、Cl-、N03-、Cu2+ |
| C、Al3+、C032-、Na+ |
| D、Ca2+、HC03-、NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 编号 |
反应温度 (利用水浴加热) |
稀硫酸 溶液 |
MnSO4固体 | 0.10mol/L KMnO4溶液 |
褪色 时间 |
| 1 | 650C | ---- | --- | 1mL | 1OOs |
| 2 | 650C | 10滴 | --- | 1mL | 90s |
| 3 | 750C | 10滴 | ---- | 1mL | 40s |
| 4 | 750C | 10滴 | 加入少许 | 1mL | 3s |
| 实验步骤 | 预期现象和结论 |
| 将很少量Cl2通入过量的FeI2溶液中; 取少量反应后溶液分置于A、B两试管中;往A中滴加 往往B中滴加 |
若 则假设1成立; 若 则假设2成立. |
查看答案和解析>>
科目:高中化学 来源: 题型:
 碳族元素是形成化合物种类最多的元素.
碳族元素是形成化合物种类最多的元素.查看答案和解析>>
科目:高中化学 来源: 题型:
| 高温 |
| 实验序号 | 铁锈质量/g | 氧化铁质量/g |
| ① | 0.856 | 0.640 |
| ② | 1.424 | 1.280 |
| ③ | 0.979 | 0.880 |
| ④ | 1.070 | 0.800 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、IClO |
| B、ICl3 |
| C、I2Cl6 |
| D、KIO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com