

| A£® | ŹĒa mL | B£® | ŹĒ£Ø50-a£©mL | C£® | Ņ»¶Ø“óÓŚa mL | D£® | Ņ»¶Ø“óÓŚ£Ø50-a£©mL |
·ÖĪö øł¾ŻµĪ¶Ø¹ÜæĢ¶ČÖµ“ÓÉĻµ½ĻĀæĢ¶ČÖš½„Ōö“óŅŌ¼°²āĮæŌĄķ£¬×¢ŅāµĪ¶Ø¹Ü×ī“óæĢ¶ČĻĀ·½ĪŽæĢ¶Č£®
½ā“š ½ā£ŗµĪ¶Ø¹ÜæĢ¶ČÖµ“ÓÉĻµ½ĻĀæĢ¶ČÖš½„Ōö“ó£¬ÓÉÓŚµĪ¶Ø¹Ü×ī“óæĢ¶ČĻĀ·½ĪŽæĢ¶Č£¬50mLµĪ¶Ø¹ÜÖŠŹµ¼ŹŹ¢·ÅŅŗĢåµÄĢå»ż“óÓŚ50ml£¬Čē¹ūŅŗĆꓦµÄ¶ĮŹżŹĒa£¬ŌņµĪ¶Ø¹ÜÖŠŅŗĢåµÄĢå»ż“óÓŚ£Ø50-a£©ml£®
¹ŹŃ”D£®
µćĘĄ ±¾Ģāæ¼²éĮĖ¼ĘĮæŅĒĘ÷µÄ¹¹Ōģ¼°ĘäŹ¹ÓĆ·½·Ø£¬ĢāÄæÄŃ¶Č²»“ó£¬×¢ŅāĮæĶ²æĢ¶ČÖµ“ÓĻĀµ½ÉĻÖš½„Ōö“󣬶ųµĪ¶Ø¹ÜæĢ¶ČÖµ“ÓÉĻµ½ĻĀæĢ¶ČÖš½„Ōö“ó£¬ĒŅ×ī“óæĢ¶ČĻĀ·½ĪŽæĢ¶Č£®


 ½šÅĘ½ĢøØÅąÓÅÓÅŃ”¾ķĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø
½šÅĘ½ĢøØÅąÓÅÓÅŃ”¾ķĘŚÄ©³å“Ģ100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| t/s | 0 | 50 | 150 | 250 | 350 |
| n£ØPCl3£©/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
| A£® | ·“Ó¦ŌŚĒ°50sµÄĘ½¾łĖŁĀŹĪŖv£ØPCl3£©=0.0064mol/£ØL•s£© | |
| B£® | ±£³ÖĘäĖüĢõ¼ž²»±ä£¬ÉżøßĪĀ¶Č£¬Ę½ŗāŹ±c£ØPCl3£©=0.11mol/L£¬Ōņ·“Ó¦µÄ”÷H£¼0 | |
| C£® | ĻąĶ¬ĪĀ¶ČĻĀ£¬ĘšŹ¼Ź±ĻņČŻĘ÷ÖŠ³äČė4molPCl3”¢4molCl2£¬“ļµ½Ę½ŗāŹ±£¬Ōņ“Ė·“Ó¦µÄ»ÆŃ§Ę½ŗā³£ŹżĪŖ0.025mol/L | |
| D£® | ĻąĶ¬ĪĀ¶ČĻĀ£¬ĘšŹ¼Ź±¼äĻņČŻĘ÷ÖŠ³äČė2molPCl5”¢0.40molPCl3ŗĶ0.40molCl2£¬“ļµ½Ę½ŗāĒ°v£ØÕż£©£¼v£ØÄę£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Äę·“Ó¦ĖŁĀŹŌö“ó£¬Õż·“Ó¦ĖŁĀŹ¼õŠ”£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ | |
| B£® | Äę·“Ó¦ĖŁĀŹ¼õŠ”£¬Õż·“Ó¦ĖŁĀŹŌö“ó£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ | |
| C£® | Õż”¢Äę·“Ó¦ĖŁĀŹ¶¼¼õŠ”£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ | |
| D£® | Õż”¢Äę·“Ó¦ĖŁĀŹ¶¼Ōö“ó£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £¬Ęä·Ö×ÓµÄæռ乹ŠĶĪŖČż½Ē׶ŠĶ£®
£¬Ęä·Ö×ÓµÄæռ乹ŠĶĪŖČż½Ē׶ŠĶ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NaOH | B£® | FeCl3 | C£® | Na2CO3 | D£® | Ca£ØOH£©2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
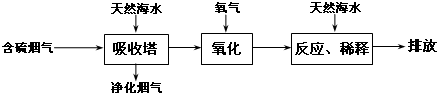
| Ī£ĻÕŠŌ | Ī£ĻÕĘ· |
| “¢ŌĖŅŖĒó | Ō¶Ąė½šŹō·ŪÄ©”¢°±”¢ĢžĄą”¢“¼µČĪļÖŹ£¬ÉčÖĆĀČĘų¼ģ²āŅĒ |
| Š¹Ā©“¦Ąķ | NaOH”¢NaHSO3ČÜŅŗĪüŹÕ |
| °ü×° | øÖĘæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŗĻ½šµÄČŪ·Šµć±ČŌČĪŅ»½šŹōŅŖøß | B£® | ŗĻ½šµÄÓ²¶Č±ČŌČĪŅ»½šŹōŅŖ“ó | ||
| C£® | ·Ē½šŹōŅ²æÉŅŌŹĒŗĻ½šµÄ³É·ÖÖ®Ņ» | D£® | ŗĻ½šµÄÓĆĶ¾±Č“潚ŹōµÄÓĆĶ¾øü¹ć |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆÅŻÄĆš»šĘ÷ | B£® | ÓĆĖ®ĘĖĆš | ||
| C£® | ÓĆøÉŌļµÄɳ×ÓøĒĆš | D£® | ÓĆĆŗÓĶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
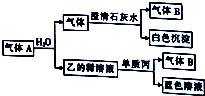 ½«Ņ»ŗŚÉ«¹ĢĢåµ„ÖŹ¼×Ķ¶ČėŅŅµÄÅØČÜŅŗÖŠ¹²ČČ£¬¾ēĮŅ·“Ó¦²śÉś»ģŗĻĘųĢåA£¬A“ęŌŚČēĶ¼×Ŗ»Æ¹ŲĻµ£¬ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
½«Ņ»ŗŚÉ«¹ĢĢåµ„ÖŹ¼×Ķ¶ČėŅŅµÄÅØČÜŅŗÖŠ¹²ČČ£¬¾ēĮŅ·“Ó¦²śÉś»ģŗĻĘųĢåA£¬A“ęŌŚČēĶ¼×Ŗ»Æ¹ŲĻµ£¬ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com