
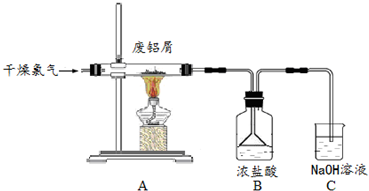
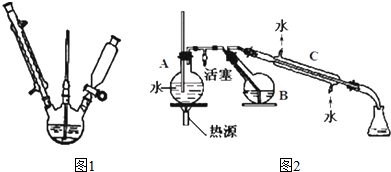
���� ʵ����������������Ӧ�Ʊ�AlCl3��AlCl3����ˮ���յ�AlCl3��Һ������AlCl3��ˮ�⣬���������Ȼ���Ҫ��������Һ���Ȼ���������ˮ������װ��B���÷�ֹ����װ�ã�ʵ����������β����������������Һ���գ����Ƶõ�AlCl3��Һ�ܽ�һ������CaCO3�γ���Һ�����ð�ˮ������Ȼ����տɵ�12CaO•7Al2O3����
��1��ʵ���������������Ũ�����Ʊ������������������Ȼ��ؼ�ˮ�����ݵ���غ��Ԫ���غ���д���ӷ���ʽ��ʵ����������β��������Ⱦ������
��2��AlCl3��ˮ�⣬���������Ȼ���Ҫ��������Һ��Ϊ�˷�ֹAlCl3���������������ܣ�ʵ���мӴֵ��ܡ����̵��ܳ��ȡ����ȵ��ܡ�ͨ�뵪���ȣ�
��3��Bװ���е�AlCl3��Һ�ܽ�CaCO3ʱ��AlCl3��Һˮ������ԣ������ڻ��ʱ���Խ�̼��Ʒ�ĩ�����ӵ��Ȼ�����Һ�У�����̼����ܽ⣻
��4������������������ˮ����Ԫ�ػ�����ʧ������̼���Ҫ�ʵ�������
��5���ð���ʯ����Ҫ�ɷ�ΪCaCO3��MgCO3���Ʊ�����̼��ƣ�Ҫ��ȥԭ���е�þ���ӣ�����þ�Ļ����ﲻ�����������Һ������Ҫ��ȥ̼��þ���Ƚ��������գ������������Һ�ܽ����պ�Ĺ��壬Ȼ����ˣ���������Һ��ͨ�������̼������PHֵ11-12�����˿ɵ�̼��Ƴ�����
��� �⣺��1��ʵ���������������Ũ�����Ʊ������������������Ȼ��ؼ�ˮ����Ӧ�����ӷ���ʽΪClO3-+5Cl-+6H+=3Cl2+3H2O��ʵ����������β��������Ⱦ������������Cװ�����������ƽ���β�����գ�������������ֹ��Ⱦ������
�ʴ�Ϊ��ClO3-+5Cl-+6H+=3Cl2+3H2O��������������ֹ��Ⱦ������
��2��AlCl3��ˮ�⣬���������Ȼ���Ҫ��������Һ��Ϊ�˷�ֹAlCl3���������������ܣ�ʵ���мӴֵ��ܡ����̵��ܳ��ȡ����ȵ��ܡ�ͨ�뵪���ȣ�
�ʴ�Ϊ���Ӵֵ��ܡ����̵��ܳ��ȡ����ȵ��ܡ�ͨ�뵪���ȣ�
��3��Bװ���е�AlCl3��Һ�ܽ�CaCO3ʱ��AlCl3��Һˮ������ԣ������ڻ��ʱ���Խ�̼��Ʒ�ĩ�����ӵ��Ȼ�����Һ�У�����̼����ܽ⣬
�ʴ�Ϊ��̼��Ʒ�ĩ�������뵽AlCl3��Һ�У�
��4������������������ˮ����Ԫ�ػ�����ʧ������̼���Ҫ�ʵ�������
�ʴ�Ϊ��������������ˮ�������ʧ��
��5���ð���ʯ����Ҫ�ɷ�ΪCaCO3��MgCO3���Ʊ�����̼��ƣ�Ҫ��ȥԭ���е�þ���ӣ�����þ�Ļ����ﲻ�����������Һ������Ҫ��ȥ̼��þ���Ƚ��������գ������������Һ�ܽ����պ�Ĺ��壬Ȼ����ˣ���������Һ��ͨ�백����������̼������PHֵ11-12�����˿ɵ�̼��Ƴ�����
�ʴ�Ϊ�����������Һ�ܽ����պ�Ĺ��壬���ˣ���������Һ��ͨ�백����������̼������PHֵ11-12�����˳�̼��Ƴ�����
���� �����ۺϿ������ʵ��Ʊ��Լ������ᴿ��ʵ����������ȣ�Ϊ�߿��������ͣ�������ѧ���ķ�����ʵ�������Ŀ��飬ע��������ʵ������Լ���Ŀ�������Ϣ���Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �٢ڢ� | C�� | �٢ܢ� | D�� | �٢ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na+ | B�� | Cu2+ | C�� | H+ | D�� | Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
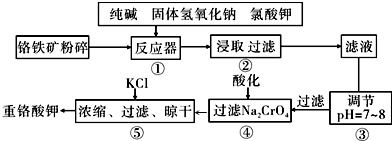
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
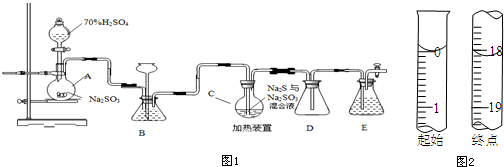
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
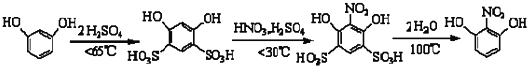
| ���� | ��Է������� | ��״ | �۵� | ˮ���ԣ����£� |
| �䱽���� | 110 | ��ɫ��״���� | 110.7 | ���� |
| 2-����-1��3-������ | 155 | �ۺ�ɫ��״���� | 87.8 | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
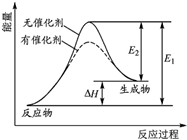 ij��Ӧ�ķ�Ӧ�����������仯��ͼ��ʾ��ͼ��E1��ʾ����Ӧ�Ļ�ܣ�E2��ʾ�淴Ӧ�Ļ�ܣ��������й�������ȷ���ǣ�������
ij��Ӧ�ķ�Ӧ�����������仯��ͼ��ʾ��ͼ��E1��ʾ����Ӧ�Ļ�ܣ�E2��ʾ�淴Ӧ�Ļ�ܣ��������й�������ȷ���ǣ�������| A�� | �÷�ӦΪ���ȷ�Ӧ | |
| B�� | �����ܸı䷴Ӧ���ʱ� | |
| C�� | �����ܸı䷴Ӧ��·�������ͷ�Ӧ����Ļ�� | |
| D�� | ��H=E1+E2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 7�� | B�� | 8�� | C�� | 9�� | D�� | 10�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com