
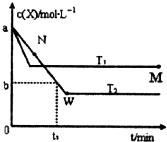
 在恒容密闭容器中通入一定量的X气体与Y气体并发生反应:2X(g)+Y(g)?2Z(g),测得在温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是( )
在恒容密闭容器中通入一定量的X气体与Y气体并发生反应:2X(g)+Y(g)?2Z(g),测得在温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是( )| A、该反应进行到M点放出的热量大于进行到W点放出的热量 | ||
B、T2下,在0?t1时间内,υ(Y)=
| ||
| C、M点的平衡常数比W点的平衡常数小 | ||
| D、M点时再加入一定量的X,平衡后X的转化率增大 |
| 1 |
| 2 |
| a-b |
| 2 |
| a-b |
| 2t1 |


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:
A、电解水制氢:2H2O
| ||||
B、高温使水分解制氢:2H2O
| ||||
C、太阳光催化分解水制氢:2H2O
| ||||
D、天然气制氢:CH4+H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稳定性:W的氢化物>Z的氢化物,沸点:W的氢化物<Z的氢化物 |
| B、元素X、Y、Z的单质晶体可能属于同种类型的晶体 |
| C、XZ2、X2M2、M2Z2均为直线型的共价化合物 |
| D、由Z和W组成的一种化合物能使酸性高锰酸钾溶液褪色,表明其具有漂白性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
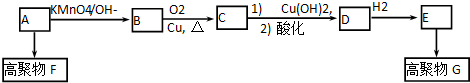
| KMnO4/OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在漂白粉中滴入70%的硫酸,立即产生黄绿色气体,说明硫酸具有还原性 |
| B、实验室从海带中提取单质碘的方法:取样→灼烧→溶解→过滤→萃取 |
| C、燃料电池制作实验中,用KNO3溶液或Na2SO4溶液代替蒸馏水,效果更好 |
| D、润洗滴定管时应从滴定管上口加入润洗溶液,倾斜着转动滴定管使液体润湿内壁,再从上口倒出,重复2-3次 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com