
| A. | 0.5mol | B. | 2mol | C. | 2.5mol | D. | 4mol |
分析 根据碳原子守恒判断四种有机物的物质的量,发生取代反应时甲烷消耗的H原子和氯气的物质的量之比为1:1,据此计算总共消耗的氯气的物质的量.
解答 解:1mol CH4与Cl2发生取代反应,待反应完成后测得4种取代物物质的量相等,则CH3Cl、CH2Cl2、CHCl3、CCl4的物质的量都是0.25mol,CH4与Cl2发生取代反应时消耗的氢原子和氯气的物质的量之比是1:1,
生成0.25molCH3Cl需要Cl2的物质的量为0.25mol,
生成0.25molCH2Cl2需要Cl2的物质的量为0.25mol×2=0.5mol,
生成0.25molCHCl3需要Cl2的物质的量为0.25mol×3=0.75mol,
生成0.25molCCl4需要Cl2的物质的量为0.25mol×4=1mol,
所以总共消耗的氯气的物质的量=(0.25+0.5+0.75+1)mol=2.5mol,
故选C.
点评 本题考查了根据方程式计算、取代反应,难度中等,明确取代反应中被取代的氢原子的物质的量与氯气分子的物质的量的关系是解本题的关键.


 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ②③⑤⑥ | C. | ③④⑥ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
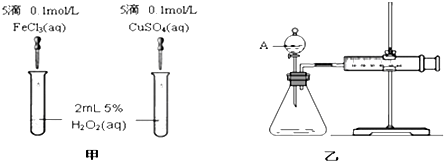
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
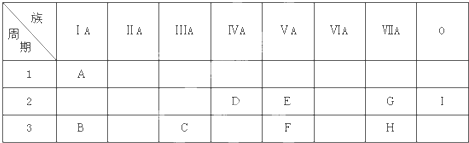
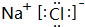 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 8n | B. | 14n | C. | 18n | D. | 44n |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com