
[s1] 元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是
A.同一元素不可能既表现金属性,又表现非金属性
B.第三周期元素的最高正化合价等于它所处的主族序数
C.短周期元素形成离子后,最外层电子都达到8电子稳定结构
D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同
[s1]14.
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
[s1]
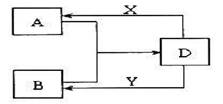 |
(1)若A、B均为气体,在水溶液中反应生成正盐D,其中A是形成酸雨的主要物质。则D的化学式是 。B发生催化氧化反应的化学方程式是 。
(2)若A、B、D含有相同的金属元素,则此元素在元素周期表中的位置是 ,工业上制取该金属单质的化学方程式为: ,现将X滴入B的溶液中至过量,该过程发生的离子方程式为: 。
(3)若A为无色无味的气体,B为盐,且A、B、D三种物质含有相同元素,则A的电子式为: ,A与B溶液反应生成D的离子方程式为: 。
[s1]28.
查看答案和解析>>
科目:高中化学 来源:广西省桂林中学2010-2011学年高三年级8月月考化学 题型:填空题
[s1] 几种短周期元素的原子半径及其某些化合价见下表:
|
元素代号 |
A |
B |
D |
E |
G |
H |
I |
J |
|
常见化合价 |
-1 |
-2 |
+4、-4 |
+6、+4、-2 |
+5、-3 |
+3 |
+2 |
+1 |
|
原子半径/pm |
64 |
66 |
77 |
104 |
110 |
143 |
160 |
186 |
分析上表中有关数据,并结合已学过的知识,回答以下问题,涉及上述元素的答案,请用元素符号表示。
(1)E元素在周期表中位于 周期, 族。
(2) A、H、J对应离子的半径由大到小的顺序是(填离子符号)_______________________________。
(3)A与I所形成的化合物的晶体类型是 。
(4)DB2的电子式__________ 。
(5)D的最高价氧化物与J的最高价氧化物对应水化物X的溶液(足量)发生反应的离子方程式 。
[s1]22.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com