
【题目】1molL﹣1Na2SO4溶液的含义是( )
A.1L溶液中含142gNa2SO4
B.1L溶液中含有1molNa+
C.将142gNa2SO4溶于1L水中配成溶液
D.1L水中含有1molNa2SO4
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】物质应用于其性质密切相关,下列说法错误的是
A. 硅胶可防止食物受潮是由于其具有吸水性
B. 酸性重铬酸钾用于检查酒驾是利用其强氧化性
C. 用菜籽油浸泡花椒制得花椒油的过程主要利用物理性质
D. 河水中有许多杂质和有害细菌,加入明矾消毒杀菌后可以饮用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.需要加热的反应一定是吸热反应
B.所有的化学反应都有能量变化
C.所有的放热反应都可以在常温常压下自发进行
D.核能作为一种反应热,是理想的新能源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂被誉为“金属味精”,以LiCoO2为正极材料的锂离子电池已被广泛用作便携式电源。工业上常以β-锂辉矿(主要成分为LiAlSi2O6,还含有FeO、MgO、CaO等杂质)为原料来制取金属锂。其中一种工艺流程如图所示:
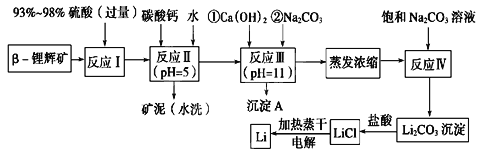
已知:①部分金属氢氧化物开始沉淀和完全沉淀时的pH如下表:
氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 2.7 | 3.7 | 9.6 |
完全沉淀pH | 3.7 | 4.7 | 11 |
②Li2CO3在不同温度下的溶解度如下表:
温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
请回答下列问题:
(1)用氧化物形式表示LiAlSi2O6的组成:________________________。
(2)反应Ⅱ加入碳酸钙的作用是___________________。
(3)流程中两次使用碳酸钠溶液,请说明前后两次使用中浓度不同的原因:______________。
(4)洗涤所得Li2CO3沉淀要使用________(填“热水”或“冷水”),你选择的理由是________________。
(5)将盐酸与Li2CO3完全反应后的溶液,加热蒸干得到固体,再将其熔融电解生产锂。电解时产生的氯气中会混有少量氧气,原因是:__________________________。
(6)下列关于金属锂及碱金属的说法正确的是___________(填序号)。
A.锂是碱金属,其熔点高于钠 B.根据对角线原则,氢氧化锂是强碱
C.金属锂的氧化物形式十分复杂 D.碱金属中密度最小的是锂,其次是钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有稀硫酸、纯碱、二氧化碳、铜片、食盐、生石灰、铁片和木炭粉8种物质。
(1)在这8种物质中,属于电解质的有____________________
(用相应的化学式表示,下同)。
(2)这8种物质中的某5种存在下面的相互关系,选择适当的物质填入①~⑤,使有连线的两种物质能发生反应,并回答下列问题。

①它们的化学式分别为:①______________;②______________;③____________;④________________;⑤______________。
②如果连线对应的反应分别用A、B、C、D、E表示。五个反应中属于氧化还原反应的有________________个;反应A的离子方程式为_____________,反应B________________(填“属于”或“不属于”)离子反应,反应D的化学方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有0.270 kg 质量分数为10 %的CuCl2溶液。计算:
(1)溶液中Cu2+ 和Cl-物质的量。
(2)若该溶液密度为1.08 g/mL,则CuCl2的物质的量浓度是多少?
(3)若取该溶液100 mL,加入铁片(过量),充分反应后对铁片洗涤、烘干、称重,铁片质量增加多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在密闭容器中发生如下反应:N2O4(g)![]() 2NO2(g)△H>0,反应达到平衡时,下列说法不正确的是( )
2NO2(g)△H>0,反应达到平衡时,下列说法不正确的是( )
A.若缩小容器的体积,则容器中气体的颜色先变深后又变浅,且比原平衡颜色深
B.若压强不变,向容器中再加入一定量的N2O4,再次达到平衡时各种物质的百分含量不变
C.若体积不变,向容器中再加入一定量的N2O4,平衡向逆反应方向移动,再次平衡时N2O4的转化率将降低
D.若体积不变,升高温度,再次平衡时体系颜色加深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在空气中直接蒸发下列盐的溶液:①Fe2(SO4)3 ②Na2CO3③KC1 ④CuCl2 ⑤NaHCO3可以得到相应盐的晶体(可以含有结晶水)的是( )
A. ①③⑤ B. ①②③ C. ②④ D. ①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列判断正确的是( )
①维生素C具有还原性,在人体内起抗氧化作用
②NO2溶于水时发生氧化还原反应
③1 mol Cl2参加反应转移电子数一定为2NA
④阴离子都只有还原性
A. ①② B. ②③ C. ③④ D. ①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com