
����Ŀ��I.�к��Ȳⶨ��
��1���к��Ȳⶨ��ʵ���У��õ��IJ����������ձ����¶ȼơ�________��________��
��2����ȡ��Ӧ��ʱ��ȡ50 mL 0.50 mol��L��1�����������������Լ���________(�����)��
a��50 mL 0.50 mol��L��1NaOH��Һ
b��50 mL 0.55 mol��L��1NaOH��Һ
c��1.0 g NaOH����
II.�����к͵ζ��ⶨij�����Ũ�ȣ��й����ݼ�¼���£�
�ζ���� | ����Һ���(mL) | �������ռ��Һ�����(mL) | ||
�ζ�ǰ | �ζ��� | ���ĵ���� | ||
1 | 25.00 | 0.50 | 25.12 | 24.62 |
2 | 25.00 | / | / | / |
3 | 25.00 | 5.00 | 29.58 | 24.58 |
��3��Ӧ��______ʽ�ζ���ʢװ0.2500 mol/L�ռ��Һ����ƿ��װ��25.00mL����������Һ��
��4����ͼ��ʾ�ڶ��εζ�ʱ50 mL�ζ�����ǰ��Һ���λ�á��ôεζ����ñ��ռ���Һ���Ϊ_________mL��

��5�������������ݣ����������������ʵ���Ũ�ȣ�ע�Ᵽ�����ʵ���Ч���֣���c (HCl) = _____________��
��6������ʱ�����ζ�ǰ���ӣ��ζ����ӣ����ʹ���ղⶨ���_________ (���Ӱ�족����ƫ�ߡ�����ƫ�͡�����ͬ)����װ��Һ�ĵζ�����װҺǰδ�ñ�NaOH��Һ��ϴ����ʹ���ղⶨ���_________��
���𰸡������� ���β�������� b �� 24.60 0.2460mol/L ƫ�� ƫ��
��������
��1���к��Ȳⶨʵ���У�����Ҫʹ�õIJ��������в����������β������������2��ͨ�������Թ�����NaOH��Һ��ʹ�����ַ�Ӧ��ע��c����������������ˮҪ���ȣ���Ȼ�����ʣ���3��ȷ��ȡһ�����������������ҺӦʹ�ü�ʽ�ζ��ܣ��������ƻḯʴ��ʽ�ζ���ĥ�ڲ����������֣���4���ζ�ǰ��ʽ�ζ��ܵĶ���Ϊ0.30mL���ζ���ζ��ܵĶ���Ϊ24.90mL������ȡ��NaOH��Һ�����Ϊ24.60mL����5��������������С������Ч��ȡ��ƽ��ֵΪ24.60mL������c(HCl)=0.2500mol/L��![]() =0.2460mol/L����6���ζ�ǰ���ӣ��ζ����ӣ���������ն�ȡ�������ֵƫС�������Դ����ݼ���������Ũ��ƫ�ͣ��Լ�������ʱ����û�һ��ʾ��ͼ�������ζ���ʢװ��Һǰδ��ϴ�����Һ��ϡ�ͣ��ζ�ʱ���õ�������࣬�Դ˼���õ��������Ũ��ƫ�ߡ�
=0.2460mol/L����6���ζ�ǰ���ӣ��ζ����ӣ���������ն�ȡ�������ֵƫС�������Դ����ݼ���������Ũ��ƫ�ͣ��Լ�������ʱ����û�һ��ʾ��ͼ�������ζ���ʢװ��Һǰδ��ϴ�����Һ��ϡ�ͣ��ζ�ʱ���õ�������࣬�Դ˼���õ��������Ũ��ƫ�ߡ�


 ������ÿ�ʱ��ҵϵ�д�
������ÿ�ʱ��ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��![]() ��һ����ɫ������ˮ�ľ��壬�㷺���ڻ�ѧ�������������ݵȡ����ɵ�Ʒ���(����Ԫ���⣬������Cu��Zn��Fe��Cr��Ԫ������)Ϊԭ�ϻ�á������������£�
��һ����ɫ������ˮ�ľ��壬�㷺���ڻ�ѧ�������������ݵȡ����ɵ�Ʒ���(����Ԫ���⣬������Cu��Zn��Fe��Cr��Ԫ������)Ϊԭ�ϻ�á������������£�

��֪:��![]() ��һ�ֲ�����ˮ������ǿ��ij���
��һ�ֲ�����ˮ������ǿ��ij���
����֪![]() ��
��![]() ��
��![]()
(1)Ni��ԭ������Ϊ28�����������ڱ��е�λ��Ϊ______��д��H2O2�Ľṹʽ______��
(2)����������ϡ�����ܽ����ʱ��Ϊ����߽�ȡ�ʿɲ�ȡ�Ĵ�ʩ��______(��дһ��)��
(3)������������ҺI�м�������![]() ��Һ��Ŀ���dz�ȥCu2+��
��Һ��Ŀ���dz�ȥCu2+��![]() �����г�ȥCu2+�����ӷ���ʽΪ______����
�����г�ȥCu2+�����ӷ���ʽΪ______����![]() ֮ǰ�����pH����̫�͵�Ŀ����______��
֮ǰ�����pH����̫�͵�Ŀ����______��
(4)��������Ŀ���dz�ȥFe��Cr���¶Ȳ���̫�ߵ�ԭ����__������![]() ʱ����
ʱ����![]() ��ȥ������ʱ��Һ��
��ȥ������ʱ��Һ��![]() __��
__��
(5)��Һ�������ʵ���Ҫ�ɷ���______��������Һ�����Ƿ�����Ԫ�ص��Լ���______��
(6)�����к�������Fe��Zn��Cu��Pt�����ʣ����õ�ⷨ�Ʊ��ߴ�����������������ȷ����__(��֪��������Fe2+<Ni2+<Cu2+)
A.����������������������
B.����������ԭ��Ӧ����缫��Ӧʽ��![]()
C.�������У����������ļ����������������������
D.������Һ�д��ڵĽ���������ֻ��Cu2+��![]()
E.�����۵ײ�����������ֻ��Cu��Pt
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(2017������)��ѹ���ʻ�������������ԭ��Ϊ��Ni(s)+4CO(g)![]() Ni(CO)4(g)��230��ʱ���÷�Ӧ��ƽ�ⳣ��K=2��105����֪��Ni(CO)4�ķе�Ϊ42.2�����������ʲ����뷴Ӧ��
Ni(CO)4(g)��230��ʱ���÷�Ӧ��ƽ�ⳣ��K=2��105����֪��Ni(CO)4�ķе�Ϊ42.2�����������ʲ����뷴Ӧ��
��һ�Σ���������CO��Ӧת������̬Ni(CO)4��
�ڶ��Σ�����һ�η�Ӧ���������������������230���Ƶøߴ�����
�����ж���ȷ����
A. ����c(CO)��ƽ���������ƶ�����Ӧ��ƽ�ⳣ������
B. �ڶ��Σ�Ni(CO)4�ֽ��ʽϵ�
C. ��һ�Σ���30����50������֮��ѡ��Ӧ�¶ȣ�ѡ50��
D. �÷�Ӧ�ﵽƽ��ʱ��v����[Ni(CO)4]=4v����(CO)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧʽ�У���ȷ���ǣ� ��
A. �����ȼ����Ϊ890.3kJ��mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ�� CH4(g)+2O2(g)=CO2(g)+2H2O(g)����H=-890.3kJ��mol-1
B. 500�桢30MPa�£���0.5molN2��1.5molH2�����ܱ������г�ַ�Ӧ����NH3(g)������19.3kJ�����Ȼ�ѧ����ʽΪ��
N2+3H2(g)![]() 2NH3(g)����H=-38.6kJ��mol-1
2NH3(g)����H=-38.6kJ��mol-1
C. ϡ�����ϡ����������Һ��ϣ����Ȼ�ѧ����ʽΪ��H+(aq)��OH��(aq)=H2O(1)�� ��H=-57.3kJ��mol-1
D. 1molH2��ȫȼ�շ���142.9kJ��������ȼ�յ��Ȼ�ѧ����ʽΪ��2H2(g)+O2(g)=2H2O(1)����H=+285.8kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪һ���¶��ºϳɰ��Ļ�ѧ��Ӧ��N2(g)��3H2(g)![]() 2NH3(g)����H=��92.4kJ/mol���ں��¡���ѹ���ܱ������н�������ʵ�飺��ͨ��1mol N2��3 mol H2����ƽ��ʱ�ų�����ΪQ1����ͨ��2mol N2��6mol H2����ƽ��ʱ�ų�����ΪQ2�������й�ϵ��ȷ����
2NH3(g)����H=��92.4kJ/mol���ں��¡���ѹ���ܱ������н�������ʵ�飺��ͨ��1mol N2��3 mol H2����ƽ��ʱ�ų�����ΪQ1����ͨ��2mol N2��6mol H2����ƽ��ʱ�ų�����ΪQ2�������й�ϵ��ȷ����
A. Q2��2Q1
B. Q1��0.5Q2
C. Q1��Q2��184.8 kJ
D. Q1��Q2��92.4 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2L�ܱ������ڣ�800��ʱ��Ӧ2NO(g)+O2(g)��2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)������Ӧ_____(������������������)���淴Ӧ��
(2)��ͼ��ʾ����ʾNO2�仯���ߵ���____����O2��ʾ0��1s�ڸ÷�Ӧ��ƽ������v=____��

(3)��˵���÷�Ӧ�Ѵﵽƽ��״̬����____(����ĸ)��
a��v(NO2)=2v(O2) b��������ѹǿ���ֲ���
c��v��(NO)=2v��(O2) d���������ܶȱ��ֲ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Դ����ϡ���Ϣһ�𱻳�Ϊ�ִ���ᷢչ������֧���������Դ�ݽߵ�Σ���������Դ�����ʺͿ�������Դ�ǽ����һ�����������Ҫ����
(1)��ѧ��Ӧ���ʺ���������������������أ����ǻ�ѧѧ�ƹ�ע�ķ���֮һ��ijѧ��Ϊ��̽��п�����ᷴӦ�����е����ʱ仯����400mLϡ�����м���������п�ۣ�����ˮ���ռ���Ӧ�ų���������ʵ���¼����(�ۼ�ֵ):
ʱ��/min | 1 | 2 | 3 | 4 | 5 |
�������/mL(���) | 100 | 240 | 464 | 576 | 620 |
����һ��ʱ���ڷ�Ӧ�������__________min(����0��1����1��2����2��3����3��4������4��5��)��
����һѧ��Ϊ���Ʒ�Ӧ���ʷ�ֹ��Ӧ�������Բ�������������������������м���������������Һ�Լ�����Ӧ���ʵ���Ӱ��������������������Ϊ���е���____________(����ĸ���)��
A��KCl��Һ B��Ũ���� C������ˮ D��CuSO4��Һ
(2)��ͼΪԭ���װ��ʾ��ͼ��

�ٽ���Ƭ��ͭƬ�õ���������һ�����Ũ�����У�һ������ռ���Һ�У��ֱ��γ���ԭ��أ���������ԭ����У��������ķֱ���_______(����ĸ)��
A����Ƭ��ͭƬ B��ͭƬ����Ƭ
C����Ƭ����Ƭ D��ͭƬ��ͭƬ
д������Ũ������Һ���γɵ�ԭ��صĸ�����Ӧʽ��_______________��
����AΪCu��BΪʯī�������ΪFeCl3��Һ������ʱ���ܷ�ӦΪ2FeCl3+Cu=2FeCl2+CuCl2��д��B�缫��Ӧʽ��________���õ���ڹ���ʱ��A�缫��������_____(��������������С������������)�����õ�ط�Ӧ������0.1mol FeCl3����ת�Ƶ��ӵ���ĿΪ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����AgCl��Һ�еμӰ�ˮ��ɵõ�������Һ�������μ�Ũ��������г������ɡ��������ϵ�֪��Ag++2NH3��H2O![]() Ag(NH3)2++2H2O��ƽ�ⳣ����ΪK[Ag(NH3)2+],���з�������ȷ���ǣ� ��
Ag(NH3)2++2H2O��ƽ�ⳣ����ΪK[Ag(NH3)2+],���з�������ȷ���ǣ� ��
A. ��Һ�д��ڳ����ܽ�ƽ�⣺AgCl(s)![]() Ag+(aq)+Cl��(aq)
Ag+(aq)+Cl��(aq)
B. ʵ�����ʵ���ҿ��ð�ˮϴ�Ӹ����������Թ�
C. ��ʵ������ж�K[Ag(NH3)2+]>KSP(AgCl)
D. ��������Ϣ����֪����Ũ��������ɵij���ΪAgCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ�������Դ����������ȡ�봢��������Դ����������о��ȵ㡣
��1����֪��CH4(g)+H2O(g)=CO(g)+3H2(g)��H=+206.2kJ/mol��
CH4(g)+CO2(g)=2CO(g)+2H2(g)��H=+247.4kJ/mol��
�Լ���Ϊԭ����ȡ�����ǹ�ҵ�ϳ��õ����ⷽ����CH4(g)��H2O(g)��Ӧ����CO2(g)��H2(g)���Ȼ�ѧ����ʽΪ______________________________________________________��
��2����ҵ�Ͽ���H2��CO2�Ʊ��״����䷴Ӧ����ʽΪCO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)��ij�¶��£���1molCO2��3molH2������������2L�ܱ������У�����������Ӧ����ò�ͬʱ�̷�Ӧǰ���ѹǿ��ϵ���±���ʾ:
CH3OH(g)+H2O(g)��ij�¶��£���1molCO2��3molH2������������2L�ܱ������У�����������Ӧ����ò�ͬʱ�̷�Ӧǰ���ѹǿ��ϵ���±���ʾ:
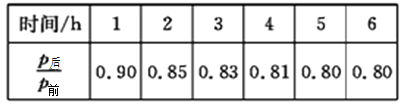
����H2��ʾ��ǰ2h��ƽ����Ӧ����v(H2)=_________��
�ڸ��¶��£�CO2��ƽ��ת����Ϊ______________��
��3����300�桢8MPa�£���CO2��H2�����ʵ���֮��1:3ͨ��һ�ܱ������з���(2)�з�Ӧ���ﵽƽ��ʱ�����CO2��ƽ��ת����Ϊ50%����÷�Ӧ�����µ�ƽ�ⳣ��ΪKp=_____(��ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������)��
��4��CO2��������ɺϳɵ�̼ϩ��:2CO2(g)��6H2(g)![]() C2H4(g)��4H2O(g)��H����0.1MPaʱ����n(CO2)��n(H2)=1��3Ͷ�ϣ���ͼ��ʾΪ��ͬ�¶�(T)�£�ƽ��ʱ������̬���ʵ����ʵ���(n)�Ĺ�ϵ��
C2H4(g)��4H2O(g)��H����0.1MPaʱ����n(CO2)��n(H2)=1��3Ͷ�ϣ���ͼ��ʾΪ��ͬ�¶�(T)�£�ƽ��ʱ������̬���ʵ����ʵ���(n)�Ĺ�ϵ��
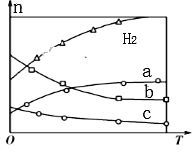
�ٸ÷�Ӧ�ġ�H_______0(�>����<��)��
������c��ʾ������Ϊ______(�ѧʽ)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com