
(15分)铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得.
①铝土矿的主要成分是Al2O3和SiO2等。从铝土矿中提炼Al2O3的流程如图1所示:
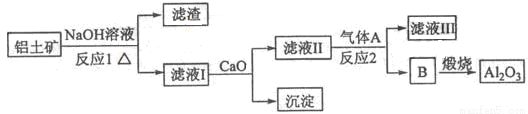
图1
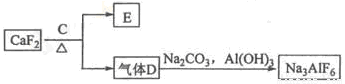
图2
②以萤石(CaF2)和纯碱为原料制备冰晶石的流程如图2所示:
回答下列问题:
(1)写出反应1的化学方程式 ; 。
(2)滤液Ⅰ中加入CaO生成的沉淀是______,反应2的离子方程式为______;
(3)E可作为建筑材料,化合物C是______,写出由D制备冰晶石的化学方程式______;
(4)电解制铝的化学方程式是______,以石墨为电极,阳极产生的混合气体的成分是______。
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源:2015-2016学年广西柳州铁路第一中学高二上段考理化学卷(解析版) 题型:选择题
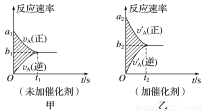
可逆反应mA(g)+nB(g)  pC(g)+qD(g)的v-t图像如图
pC(g)+qD(g)的v-t图像如图 甲所示,若其他条件都不变,只是在反应前加 入合适的催化剂,则其v-t图像如图乙所示。
甲所示,若其他条件都不变,只是在反应前加 入合适的催化剂,则其v-t图像如图乙所示。
①a1=a2 ②a1<a2 ③b1=b2 ④b1<b2 ⑤t1>t2⑥t1=t2 ⑦两图中阴影部分面积相等 ⑧图Ⅱ中阴 影部分面积更大,以上所述正确的为
A.②④⑤⑦ B.②④⑥⑧
C.②③⑤⑦ D.②③⑥⑧
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东广州执信中学高二上期中文化学试卷(解析版) 题型:?????
关于维生素的下列说法不正确的是( )
A. 维生素是生物生长发育和新陈代谢所必需的物质。
B. 水溶性维生素不易被人体吸收,所以容易缺乏
C. 按溶解性的不同,维生素可分为脂溶性维生素和水溶性维生素两类
D. 脂溶性维生素不易排泄,容易在体内积存,主要积存在肝脏
查看答案和解析>>
科目:高中化学 来源:2016届浙江临海台州中学高三上学期第三次统练化学试卷(解析版) 题型:实验题
KI在食品、医药领域有广泛用途。某科研小组利用碘废弃液(主要含I2、I-)制备KI,流程如下:
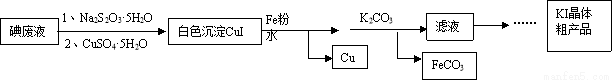
已知:I2+2S2O32-==S4O62-+2I-
(1)加入胆矾的作用 。
(2)为制得KI晶体粗产品,滤液后续操作步骤是 。
(3)用沉淀滴定法测定样品中KI含量的实验步骤如下:
a.称取3.000 g样品,溶解,配制成250 mL溶液
b.量取25.00 mL待测液于锥形瓶中
c.用0.1000 mol•L-1AgNO3标准溶液滴定至终点,记录消耗AgNO3标准溶液的体积
d.重复b、c操作2~3次,平均消耗AgNO3标准溶液16.50 mL
①配制250mL样品溶液时,所需的仪器除烧杯、玻璃棒之外,还缺少的玻璃仪器是 。AgNO3标准溶液在使用之前通常要重新标定,原因是 ;本实验滴定过程中操作滴定管的图示正确的是______(填编号)。
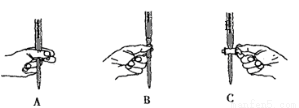
③该样品中KI的质量百分数为 。
④下列因素会导致KI含量的测定结果偏高的是 。
A.配制样品溶液定容时仰视
B.锥形瓶未干燥
C.滴定管未用AgNO3标准溶液润洗
D.滴定终点时滴定管尖嘴中产生气泡
查看答案和解析>>
科目:高中化学 来源:2016届浙江临海台州中学高三上学期第三次统练化学试卷(解析版) 题型:选择题
化学与人类生产和生活密切相关,下列说法正确的是
A.聚乙烯塑料的老化是由于发生了加成反应
B.加碘食盐中加入的I2有利于防止地方缺碘病
C.二氧化硫有漂白性,常用作棉、麻、纸张的漂白
D.汽车尾气污染物中含有氮的氧化物,是汽油不完全燃烧造成的
查看答案和解析>>
科目:高中化学 来源:2016届河北正定中学高三上学期第五次月考理科综合化学试卷(解析版) 题型:选择题
莽草酸可用来合成药物达菲,其结构简式如图所示,下列关于莽草酸的说法错误的是
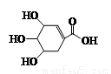
A.分子式为C7H10O5
B.分子中含有两种官能团
C.既可发生加成又可发生取代反应
D.能够使酸性高锰酸钾溶液和溴水褪色
查看答案和解析>>
科目:高中化学 来源:2016届福建省三明市高三上学期第二次月考化学试卷(解析版) 题型:选择题
室温下,将0.100 0 mol·L-1盐酸滴入20.00 mL 未知浓度的某一元碱MOH溶液中,溶液pH随加入盐酸体积变化曲线如图所示。下列有关说法不正确的
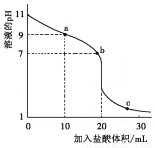
A.该一元碱溶液浓度为0.100 0 mol·L-1
B.a、b、c点的水溶液导电性依次增强
C.室温下,MOH的电离常数Kb=1×10-5
D.b点:c(M+)+c(MOH)=c(Clˉ)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高二12月月考化学卷(解析版) 题型:选择题
80℃时,2L密闭容器中充入0.40molN2O4,发生反应N2O4 2NO2 △H=+QkJ·mol-1(Q>0) ,获得如下数据:
2NO2 △H=+QkJ·mol-1(Q>0) ,获得如下数据:
时间/s | 0 | 20 | 40 | 60 | 80 | 100 |
c(NO2)/mol·L-1 | 0.00 | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
下列判断正确的是
A.升高温度该反应的平衡常数K减小
B.20—40s内,v(N2O4)=0.004mol/(L·s)
C.反应达平衡时,吸收的热量为0.30QkJ
D.100s时再通入0.40molN2O4,达新平衡时N2O4的转化率增大
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高一上期中测试化学试卷(解析版) 题型:选择题
向H2SO4、CuCl2混合溶液中投入足量的铁粉,经充分反应后,过滤、洗涤、干燥、称重,知所得固体的质量与加入的铁粉的质量相等,则原溶液中c(SO42﹣)与c(Cl﹣)之比
A.1:2 B.1:7 C.7:1 D.1:14
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com