
| A、吸热反应 |
| B、放热反应 |
| C、氧化还原反应 |
| D、非氧化还原反应 |
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
| A、试管塞越来越紧,是因为反应消耗了大量NH3 |
| B、溶液逐渐变为浅黄色,是因为反应生成了少量的NO2 |
| C、溶液迅速变为蓝色溶液,是因为反应生成了[Cu(H2O)4]2+ |
| D、上述反应原理可用于测定O2的含量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
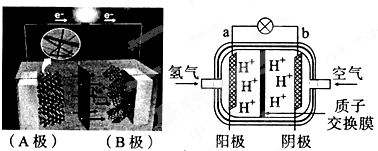
查看答案和解析>>
科目:高中化学 来源: 题型:
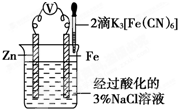 为探究铁腐蚀的保护方法,某同学按图连接好装 置并往Fe电极区滴入2滴黄色K3[Fe(CN)6](铁氰化钾)溶液.
为探究铁腐蚀的保护方法,某同学按图连接好装 置并往Fe电极区滴入2滴黄色K3[Fe(CN)6](铁氰化钾)溶液.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Zn为正极,Cu为负极,CuCl2溶液作电解质溶液 |
| B、Cu为正极,Zn为负极,稀H2SO4作电解质溶液 |
| C、Cu为正极,Zn为负极,CuSO4溶液作电解质溶液 |
| D、Fe为正极,Zn为负极,CuCl2溶液作电解质溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
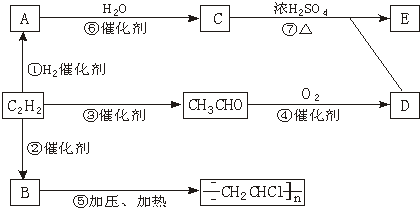
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com