
”¾ĢāÄæ”æ³£ÓĆŠ”½Ī³µ£ØČ¼ÓĶĘū³µ£©ÖŠµÄ¶ÆĮ¦ŗĶÄÜĮæÓė»Æѧ·“Ó¦Ļ¢Ļ¢Ļą¹Ų”£
£Ø1£©ÓĆC8H18“ś±ķĘūÓĶ·Ö×Ó£¬Š“³öĘūÓĶĶźČ«Č¼ÉյĻÆѧ·½³ĢŹ½__________”£
£Ø2£©¹ŲÓŚĘūÓĶŌŚĘųø×ÖŠČ¼ÉÕ·“Ó¦µÄŠšŹöÕżČ·µÄŹĒ__________£ØŠ“×ÖÄø£©
A£®ĘūÓĶ¾ßÓŠµÄ×ÜÄÜĮæøßÓŚÉś³ÉĪļ¶žŃõ»ÆĢ¼ŗĶĖ®¾ßÓŠµÄ×ÜÄÜĮæ
B£®ĢĄÓĶČ¼ÉÕ¹ż³ĢÖŠ£¬»ÆѧÄÜ×Ŗ»ÆĪŖČČÄÜ
C£®¶ĻĮŃĘūÓĶŗĶŃõĘų·Ö×ÓÖŠ»Æѧ¼üĪüŹÕµÄÄÜĮæŠ”ÓŚÉś³ÉĢ¼Ńõ»ÆĪļŗĶĖ®ÖŠ»Æѧ¼ü·Å³öµÄÄÜĮæ
D£®Ęū³µĪ²ĘųÖŠŗ¬NOµÄŌŅņŹĒĘūÓĶÖŠŗ¬ÓŠµŖŌŖĖŲ£¬Č¼ÉÕŗóÉś³ÉNO
£Ø3£©Ęū³µÖŠµÄµēĘæĪŖĒ¦Ėįµē³Ų£¬Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O2£¬ŅŃÖŖPbSO4ÄŃČÜÓŚĖ®£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ__________£ØŠ“×ÖÄø£©
2PbSO4+2H2O2£¬ŅŃÖŖPbSO4ÄŃČÜÓŚĖ®£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ__________£ØŠ“×ÖÄø£©
A£®·ÅµēŹ±£¬øŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗPb-2e-=Pb2+
B£®·ÅµēŹ±£¬Õż¼«µĆµē×ÓµÄĪļÖŹŹĒPbO2
C£®·ÅµēŹ±£¬ĄķĀŪÉĻĆæĻūŗÄ20.7gĒ¦£¬ĶāµēĀ·ÖŠ×ŖŅʵĵē×ÓĪŖ0.4mol
D£®³äµēŹĒŹ¹·ÅµēŹ±µÄŃõ»Æ»¹Ō·“Ó¦ÄęĻņ½ųŠŠ
£Ø4£©ŃŠ¾æĒāŃõČ¼ĮĻµē³ŲÖŠ£¬H2ĖłŌŚµÄµē¼«ĪŖ__________¼«£ØĢī”°Õż”±»ņ”°øŗ”±£©£¬µē¼«·“Ó¦Ź½ĪŖ__________£»ĒāŃõČ¼ĮĻµē³ŲµÄÓŵćÓŠ__________£ØÖĮÉŁĖµ³ö2Ģõ£©”£
”¾“š°ø”æ 2C8H18+25O2![]() 16CO2”ü+18H2O BC BD øŗ H2-2e-+2OH-=2H2O ÄÜĮæ×Ŗ»ÆŠ§ĀŹøߣ¬ĪŽĪŪČ¾µČĘäĖū
16CO2”ü+18H2O BC BD øŗ H2-2e-+2OH-=2H2O ÄÜĮæ×Ŗ»ÆŠ§ĀŹøߣ¬ĪŽĪŪČ¾µČĘäĖū
”¾½āĪö”æ£Ø1£©C8H18ĶźČ«Č¼ÉÕÉś³ÉCO2ŗĶH2OŹ±·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ2C8H18+25O2![]() 16CO2”ü+18H2O£»
16CO2”ü+18H2O£»
£Ø2£©A£®ĘūÓĶČ¼ÉÕŹĒ·ÅČČ·“Ó¦£¬Ōņ²Ī¼Ó·“Ó¦µÄĘūÓĶŗĶŃõĘų¾ßÓŠµÄ×ÜÄÜĮæøßÓŚÉś³ÉĪļ¶žŃõ»ÆĢ¼ŗĶĖ®¾ßÓŠµÄ×ÜÄÜĮ棬¹ŹA“ķĪó£»B£®ĘūÓĶČ¼ÉÕ¹ż³ĢÖŠ£¬ÄÜĮæ×Ŗ»ÆŠĪŹ½ĪŖ»ÆѧÄÜ×Ŗ»ÆĪŖČČÄÜ£¬¹ŹBÕżČ·£»C£®ĘūÓĶČ¼ÉÕŹĒ·ÅČČ·“Ó¦£¬Ōņ¶ĻĮŃĘūÓĶŗĶŃõĘų·Ö×ÓÖŠ»Æѧ¼üĪüŹÕµÄÄÜĮæŠ”ÓŚÉś³ÉĢ¼Ńõ»ÆĪļŗĶĖ®ÖŠ»Æѧ¼ü·Å³öµÄÄÜĮ棬¹ŹCÕżČ·£»D£®ĘūÓĶŹĒĢ¼Ēā»ÆŗĻĪļ£¬²»ŗ¬ÓŠµŖŌŖĖŲ£¬Ęū³µĪ²ĘųÖŠŗ¬NOµÄŌŅņŹĒæÕĘųÖŠµÄµŖĘųŌŚøßĪĀĻĀŃõ»ÆĪŖNO£¬¹ŹD“ķĪ󣻓š°øĪŖBC”£
£Ø3£©A£®·ÅµēŹ±ŹĒŌµē³Ų£¬PbĪŖøŗ¼«£¬Ęäµē¼«·“Ó¦Ź½ĪŖ£ŗPb-2e-+SO42-=PbSO4”ż£¬¹ŹA“ķĪó£»B£®·ÅµēŹ±Ōµē³Ų£¬PbO2ŌŚÕż¼«ÉĻµĆµē×Ó·¢Éś»¹Ō·“Ó¦£¬Éś³ÉPbSO4£¬¹ŹBÕżČ·£»C£®·ÅµēŹ±£¬ĄķĀŪÉĻĆæĻūŗÄ20.7g£ØĪļÖŹµÄĮæĪŖ0.1mol£©Ē¦£¬ĶāµēĀ·ÖŠ×ŖŅʵĵē×ÓĪŖ0.2mol£¬¹ŹC“ķĪó£»D£®³äµēŹ±µē½ā³Ų£¬·¢ÉśµÄ·“Ó¦ĪŖ·ÅµēŹ±µÄŃõ»Æ»¹Ō·“Ó¦Äę·“Ó¦£¬¹ŹDÕżČ·£»“š°øĪŖBD£»
£Ø4£©ŃŠ¾æĒāŃõČ¼ĮĻµē³ŲÖŠ£¬ÄÜO2µÄ¼«ĪŖÕż¼«£¬ŌņH2ĖłŌŚµÄµē¼«ĪŖøŗ¼«£¬·¢ÉśŃõ»Æ·“Ó¦£¬Ęäµē¼«·“Ó¦Ź½ĪŖH2-2e-+2OH-=2H2O£»ĒāŃõČ¼ĮĻµē³ŲĻą¶ŌĘäĖüµē³Ų£¬ĢåĻÖĮĖÄÜĮæ×Ŗ»ÆŠ§ĀŹøߣ¬ĪŽĪŪČ¾µČÓÅµć”£


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¶ŌÓŚø÷ÖÖĪļÖŹµÄÓ¦ÓĆĖµ·Ø“ķĪóµÄŹĒ
A. ¹č½ŗ×÷“ü×°Ź³Ę·µÄĪüŃõ¼Į
B. ¶žŃõ»ÆĮņ×÷Ö½½¬µÄĘÆ°×¼Į
C. Al(OH)3æÉĢķ¼Óµ½ĖÜĮĻÖŠ×÷×čČ¼¼Į
D. ClO2ŹĒŅ»ÖÖ±ČCl2øü°²Č«µÄ×ŌĄ“Ė®Ļū¶¾¼Į
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£ŗ2H2S(g)£«O2(g)===S2(s)£«2H2O(l)”” ¦¤H£½£632 kJ”¤mol£1”£ĻĀĶ¼ĪŖH2SČ¼ĮĻµē³ŲµÄŹ¾ŅāĶ¼”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
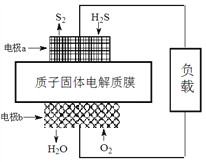
A. µē¼«aĪŖµē³ŲµÄøŗ¼«
B. µē¼«bÉĻ·¢ÉśµÄµē¼«·“Ó¦ĪŖ£ŗO2£«2H2O£«4e£===4OH£
C. ĆæÓŠ1molŃõĘų²Ī¼Ó·“Ó¦£¬µē³ŲÄŚ²æĪüŹÕ632 kJČČÄÜ
D. Ćæ34 g H2S²ĪÓė·“Ó¦£¬µēĀ·ÖŠÓŠ2 mol µē×ÓĶعż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ½įĀŪŹĒ“ÓijĶ¬Ń§µÄ±Ź¼Ē±¾ÉĻÕŖĀ¼µÄ£¬ÄćČĻĪŖĘäÖŠæĻ¶ØÕżČ·µÄŹĒ( )
¢ŁĪ¢Į£°ė¾¶Cl££¾S2££¾S£¾F ¢ŚĒā»ÆĪļµÄĪČ¶ØŠŌ HF£¾HCl£¾H2S£¾H2Se ¢Ū»¹ŌŠŌS2££¾Cl££¾Br££¾I£¢ÜŃõ»ÆŠŌ Cl2£¾S£¾Se£¾Te ¢ŻĖįŠŌ H2SO4£¾HClO4£¾H2SeO4¢ŽµĆµē×ÓÄÜĮ¦F£¾Cl£¾Br£¾I
A. Ö»ÓŠ¢Ł B. ¢Ł¢Ū¢Ü C. ¢Ś¢Ü¢Ž D. Ö»ÓŠ¢Ž
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½ÕżČ·µÄŹĒ
A. Ļ”ĻõĖįŗĶ¹żĮæĢśŠ¼·“Ó¦£ŗ3Fe+8H++2NO3-=3Fe3++2NO”ü+4H2O
B. ĻõĖįŅųČÜŅŗŗĶ¹żĮæµÄ°±Ė®·“Ó¦Ag++3NH3”¤H2O=Ag(NH3)2OH+NH4++2H2O
C. Ģ¼ĖįÄĘČÜŅŗÖŠ¼ÓČė¹żĮæ±½·Ó£ŗ![]()
D. ĻņNH4Al(SO4)2ČÜŅŗÖŠ¼ÓČė¹żĮæµÄBa(OH)2ČÜŅŗ£ŗAl3++2SO42-+4OH-=2BaSO4”ż+AlO2-+2H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĻĀĶ¼ĖłŹ¾£¬Čō¹Ų±Õ»īČū£¬ŌņĘ·ŗģČÜŅŗĪŽ±ä»Æ£¬ŹÆČļŹŌŅŗ±äŗģ£¬³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē£»Čō“ņæŖ»īČū£¬ŌņĘ·ŗģČÜŅŗĶŹÉ«£¬ŹÆČļŹŌŅŗ±äŗģ£¬³ĪĒåŹÆ»ŅĖ®½»»ė×Ē”£¾Ż“ĖÅŠ¶ĻĘųĢåŗĶ¹ćæŚĘæÖŠŹ¢·ÅµÄĪļÖŹ·Ö±šŹĒ£Ø £©

A. SO2ŗĶÅØH2SO4 B. Cl2ŗĶNaHCO3ČÜŅŗ
C. CO2ŗĶNa2CO3ČÜŅŗ D. SO2ŗĶNaHCO3ČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹÖ»ÄÜ×÷»¹Ō¼ĮµÄŹĒ
A. S2£ B. Fe2£« C. SO32£ D. K£«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄŹżÖµ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A. ³£ĪĀ³£Ń¹ĻĀ£¬56 gŅŅĻ©ŗĶ±ūĻ©µÄ»ģŗĻĘųÖŠŗ¬ÓŠµÄĢ¼Ō×ÓŹżĪŖ4NA
B. 1.2 g NaHSO4¾§ĢåÖŠŗ¬ÓŠµÄŃōĄė×ÓŗĶŅõĄė×ÓµÄ×ÜŹżĪŖ0.03NA
C. 12 g½šøÕŹÆÖŠŗ¬ÓŠµÄ¹²¼Ū¼üŹżĪŖ4NA
D. 1 mol Fe2£«Óė×ćĮæµÄH2O2ČÜŅŗ·“Ó¦£¬×ŖŅĘ2NAøöµē×Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æSO2ŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬µ«ĘäŌģ³ÉµÄ»·¾³ĪŹĢāŅ²ŅżĘšĮĖČĖĆĒµÄ¹Ų×¢”£æŖ·¢Ń°ÕŅSO2µÄŗĻĄķĢꓜʷŹĒÄæĒ°»Æ¹¤ŠŠŅµµÄŠĀ¶ÆĢ¬”£
£Ø1£©SO2æÉŅŌÓėĖ®·“Ó¦£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ____________________________________”£SO2ŹĒ“óĘųµÄÖ÷ŅŖĪŪČ¾Īļ£¬ŹĒŌģ³É__________________µÄøłŌ“”£
£Ø2£©¹¤ŅµÉĻ³£ÓĆ»ĘĢśæó£ØFeS2£©ÖʱøSO2£¬»ĘĢśæóÖŠSµÄ»ÆŗĻ¼ŪĪŖ____________”£»ĘĢśæóģŃÉÕŗóÉś³É1.6gFe2O3£¬×ŖŅʵĵē×ÓŹżĪŖ________”£
£Ø3£©¹¤ŅµÉĻŹ¹ÓĆ¼īŅŗĪüŹÕSO2£¬Ź¹ÅŷŵÄĪ²Ęų“ļµ½ŗĻøń±ź×¼£ŗ
¢Ł½«±ź×¼×“æöĻĀ11.2LSO2ĶØČėµ½2L0.5mol”¤L-1µÄ°±Ė®ÖŠ£¬ĖłµĆČÜŅŗÖŠČÜÖŹŹĒ_________£ØĢī»ÆѧŹ½£©”£
¢Ś³£ĪĀĻĀ£¬ČōÓĆ1LNaOHČōÓĆĪüŹÕ0.01molSO2£¬ĶźČ«ĪüŹÕŗóČÜŅŗÖŠc£ØNa+£©=c£ØSO32-£©+c£ØHSO3-£©+c£ØH2SO3£©£¬ŌņŌNaOHČÜŅŗµÄpHÖµĪŖ________”£
£Ø4£©Į¬¶žŃĒĮņĖįÄĘ£ØNa2S2O4£©ÓėSO2ĻąĖĘ£¬¾ßÓŠ¼«ĒæµÄ»¹ŌŠŌ£¬æÉÓĆÓŚ±£“ęĖ®¹ūŹ³Īļ”£ĻÖæÉÓĆČēĶ¼ĖłŹ¾·½·ØĶعżĪüŹÕSO2ŗĶNO£¬»ńµĆNa2S2O4ŗĶNH4NO3£ØGeĪŖīęŌŖĖŲ£©

¢Ł×°ÖĆIIÖŠ£¬ĖįŠŌĢõ¼žĻĀ£¬NO±»Ge4+Ńõ»ÆµÄ²śĪļÖ÷ŅŖŹĒNO3-”¢NO2-£¬ĒėŠ“³öÉś³ÉµČĪļÖŹµÄĮæµÄNO3-ŗĶNO2-µÄĄė×Ó·½³ĢŹ½£ŗ_______________________________”£
¢Ś×°ÖĆIIIµÄ×÷ÓĆÖ®Ņ»ŹĒÓĆÖŹ×Ó½»»»Ä¤µē½ā²Ūµē½āŹ¹µĆGe4+ŌŁÉś£¬Ķ¬Ź±ŌŚĮķŅ»¼«Éś³ÉS2O42-µÄµē¼«·“Ó¦Ź½ĪŖ___________________________”£
£Ø5£©ĻÖ½ń£¬æĘѧ¼ŅŅŃŃŠ·¢³ö±ČSO2øü°²Č«µÄĘ«ÖŲŃĒĮņĖįŃĪ£ØK2S2O5£©£¬¹¤ŅµÉĻ³£ÓĆ2KHSO3=K2S2O5+H2OµÄ·½·ØÖʱø”£ĪŅ¹śŅŖĒóŗģ¾ĘÖŠĢķ¼ÓK2S2O5µÄ±ź×¼£Ø°“µČĮņŌŖĖŲÖŹĮæµÄSO2¼Ę£©ĪŖ0.25g/L”£½ńÄšŌģ500¶ÖĘĻĢŃ¾Ę£¬Šč¼ÓČėK2S2O5µÄÖŹĮæĪŖ_______”££ØĘĻĢŃ¾ĘµÄĆÜ¶Č½üĖĘĪŖĖ®£¬¼ĘĖć½į¹ū±£ĮōŠ”Źżµćŗó2Ī»£©
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com