
下列有关晶体的叙述中,正确的是( )
|
| A. | 在Si晶体中,Si原子与Si﹣Si键之比为1:4 |
|
| B. | 在NaCl晶体中,每个Na+周围距离最近的Na+有6个 |
|
| C. | 在CsCl晶体中,与每个Cs+紧邻的Cs+有8个 |
|
| D. | 在面心立方堆积的金属晶体中,每个金属原子周围紧邻的有12个金属原子 |
考点:
晶胞的计算.
专题:
化学键与晶体结构.
分析:
A.在Si晶体中,每个Si原子形成2个Si﹣Si键;
B.在氯化钠晶体中,每个钠离子周围与它最近且距离相等的Na+有12个;
C.氯化铯晶体中,铯离子的配位数是8,每个Cs+周围等距离紧邻的有6个Cs+;
D.面心立方晶体中,晶胞立方体每个顶点上都有一个原子,面心上都有一个原子.
解答:
解:A.在Si晶体中,每个Si原子形成2个Si﹣Si键,Si原子与Si﹣Si键之比为1:2,故A错误;
B.在NaCl晶体中,每个Na+周围与它最近且距离相等的Na+有3×8×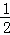 =12,故B错误;
=12,故B错误;
C.氯化铯晶体中,铯离子在体心,氯离子在顶点,铯离子的配位数是8,所以每个Cs+周围紧邻的有8个Cl﹣,但每个Cs+周围等距离紧邻的有6个Cs+,故C错误;
D.面心立方晶体中,晶胞立方体每个顶点上都有一个原子,面心上都有一个原子,所以每个金属原子周围紧邻的金属原子有3×8×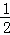 =12,故D正确.
=12,故D正确.
故选D.
点评:
本题考查晶胞分析,注意把握NaCl、CsCl的晶体结构、离子占据的位置是解答的关键,学生具有较好的空间想象能力即可解答,题目难度中等.


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
(1)等质量的O2、CH4、H2的物质的量的比值为 .
38g某二价金属氯化物(ACl2)中含有0.8mol Cl﹣,则ACl2的摩尔质量是 ;A的相对原子质量是 ;ACl2的化学式是 .
(3)新制备的氯水显 黄绿 色,说明氯水中有 (填分子式)分子存在.
(4)向氯水中滴加几滴AgNO3溶液,立即有 生成,说明氯水中有 (填离子符号)存在,反应的化学方程式为 氯水光照后颜色变浅,并放出 气体.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验的叙述,正确的是( )
A. 溴乙烷加氢氧化钠溶液做催化剂加热水解后,再加AgNO3溶液有浅黄色沉淀生成
B. 实验室用分液漏斗分离苯和水的混合物
C. 可以用酸性高锰酸钾溶液除去乙烷中混有的乙烯
D. 除去苯中的少最苯酚,可以先加浓溴水,充分沉淀后过滤即可
查看答案和解析>>
科目:高中化学 来源: 题型:
已知短周期元素的离子.aA2+、bB+、cC3﹣、dD﹣都具有相同的电子层结构,则下列叙述正确的是( )
|
| A. | 原子半径:A>B>C>D | B. | 原子序数:d>c>b>a |
|
| C. | 离子半径:C>D>B>A | D. | 单质的还原性:A>B>D>C |
查看答案和解析>>
科目:高中化学 来源: 题型:
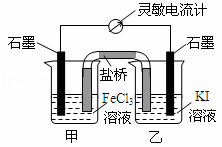
控制适合的条件,将反应2Fe3++2I﹣⇌2Fe2++I2设计成如图所示的原电池.下列判断不正确的是( )
|
| A. | 反应开始时,乙中石墨电极上发生氧化反应 |
|
| B. | 反应开始时,甲中石墨电极上Fe3+被还原 |
|
| C. | 电流计读数为零时,反应达到化学平衡状态 |
|
| D. | 电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电极为负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)Z与X形成只含一个中心原子的共价化合物,则它的分子式是 ,其分子的立体结构是 .
(2)Y的最高价氧化物晶体类型是 晶体.X的氧化物与Y的最高氧化物中,分子极性较小的是(填分子式) .
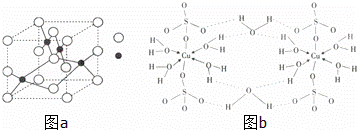
(3)如图a是W的某种氧化物的晶胞结构示意图,可确定该晶胞中阴离子的个数为 .(图中实心球表示W元素)
(4)铜元素和W元素都位于周期表的ds区,胆矾CuSO4•5H2O可写成[Cu(H2O)4]SO4•H2O,其结构示意图如图b,有关它的说法正确的是 (填字母).
A.该胆矾晶体中存在配位键、共价键和离子键
B.该结构中还存在金属键,极性共价键
C.胆矾是分子晶体,分子间存在氢键
D.胆矾中的水在不同温度下会分步失去
(5)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子.已知NF3与NH3的空间构型都是三角锥形,单NF3不易与Cu2+形成配离子,其原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于食品添加剂的叙述中不正确的是( )
|
| A. | 我国应该禁止使用味精 |
|
| B. | 亚硝酸钠可生成致癌物质 |
|
| C. | 醋可同时用作防腐剂和调味剂 |
|
| D. | 苯甲酸钠可用作食品的防腐剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com