
”¾ĢāÄæ”æij¹¤³§ĖįŠŌ·ĻŅŗÖŠŗ¬ÓŠFe3+”¢Al3+”¢Fe2+”¢SO42-£¬ŅŌøĆ·ĻŅŗĪŖŌĮĻÖʱøFe2O3µÄ¹¤ŅÕĮ÷³ĢČēĻĀ(²æ·Ö²Ł×÷ŗĶĢõ¼žĀŌ)£ŗ
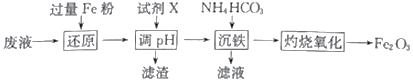
ŅŃÖŖ£ŗ¢ŁNH4HCO3ŌŚČČĖ®ÖŠ»į·Ö½ā”£
¢Ś³£ĪĀĻĀ£¬ČÜŅŗÖŠ²»Ķ¬½šŹōĄė×ÓÉś³ÉĒāŃõ»ÆĪļ³ĮµķŹ±µÄpH¼ūĻĀ±ķ£ŗ
½šŹōĄė×Ó(0.1mol”¤L-l) | Fe3+ | Fe2+ | Al3+ |
æŖŹ¼³ĮµķŹ±µÄpH | 2.4 | 7.6 | 3.4 |
ĶźČ«³ĮµķŹ±µÄpH | 3.7 | 9.6 | 4.8 |
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Š“³ö”°»¹Ō”±²½ÖčÖŠ·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ_________________________________”£
£Ø2£©ŹŌ¼ĮXæÉŃ”ÓĆ_________£ØČĪŠ“Ņ»ÖÖ£¬Ģī»ÆѧŹ½£©£¬”°ĀĖŌü”±µÄÖ÷ŅŖ³É·ÖŹĒ_________________”£
£Ø3£©¼ÓČėĢ¼ĖįĒāļ§ŗó¹żĀĖ£¬·¢ĻÖĀĖŅŗČŌČ»»ė×Ē£¬æÉÄܵÄŌŅņŹĒ_________________________£¬ÓĆ90”ęČČĖ®Ļ“µÓFeCO3³ĮµķµÄÄæµÄŹĒ______________________________________”£
£Ø4£©ČōŌŚŹµŃéŹŅÖŠ×ĘÉÕFeCO3Ó¦ŌŚ_____________(ĢīŅĒĘ÷Ćū³Ę)ÖŠ½ųŠŠ£¬”°×ĘÉÕŃõ»Æ”±·¢ÉśµÄ»Æѧ·½³ĢŹ½ĪŖ__________________________________”£
£Ø5£©Čō¹¤ŅµÉĻ×ĘÉÕŃõ»Æ174.0¶ÖFeCO3µĆµ½117.6¶Ö²śĘ·£¬ŌņøĆ²śĘ·ÖŠFe2O3µÄ“æ¶ČĪŖ___________ (Éč²śĘ·ÖŠŌÓÖŹÖ»ÓŠFeO£¬±£ĮōŅ»Ī»Š”Źż)”£
”¾“š°ø”æ Fe+2H+=Fe2++ H2”ü”¢Fe+2Fe3+=3Fe2+ NH3”¤H2O FeŗĶAl(OH)3 ĀĖÖ½ĘĘĖš»ņÕߏĒ¹żĀĖŹ±ĀĖŅŗ³¬¹żĀĖÖ½ÉĻŌµµČ Ļ“Č„±ķĆęĪüø½µÄĄė×ÓĶ¬Ź±“Ł½ųĢ¼ĖįĒāļ§µÄ·Ö½ā ŪįŪö 4FeCO3+O2![]() 2Fe2O3+4CO2 81.6%
2Fe2O3+4CO2 81.6%
”¾½āĪö”æ£Ø1£©”°»¹Ō”±ŹĒĢś·Ū½«Fe3+×Ŗ»ÆĪŖFe2+£¬Ķ¬Ź±Óė·ĻŅŗÖŠµÄH+·“Ӧɜ³ÉH2£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗFe+2H+=Fe2++ H2”üŗĶFe+2Fe3+=3Fe2+£¬“š°øĪŖ; Fe+2H+=Fe2++ H2”ü”¢Fe+2Fe3+=3Fe2+
£Ø2£©ŹŌ¼ĮXÓĆÓŚµ÷½ŚČÜŅŗµÄpH£¬Ź¹Al3+ĶźČ«³Įµķ£¬Ń”ÓĆNH3”¤H2O£¬²»ŅżČėĘäĖüŌÓÖŹ£¬Ķ¬Ź±Éś³ÉµÄĢ¼ĖįĒāļ§±ćÓŚ³żČ„£»”°ĀĖŌü”±µÄÖ÷ŅŖ³É·ÖŹĒ¹żĮæµÄĢś·ŪŗĶÉś³ÉµÄAl(OH)3³Įµķ”£“š°øĪŖ£ŗNH3”¤H2O ”¢FeŗĶAl(OH)3
£Ø3£©¹żĀĖµÄ¹ż³ĢÖŠČō°Ń²£Į§°ōææŌŚČż²ćĀĖÖ½ÉĻŹ±²»Š”ŠÄ°ŃĀĖÖ½“ĮĘĘĮĖ£¬“ĖŹ±¹żĀĖ³öµÄĀĖŅŗŹĒ»ģ×ĒµÄ£»¹żĀĖŹ±ĀĖŅŗŅŗĆęøßÓŚĀĖÖ½µÄ±ßŌµŹ±£¬ĀĖŅŗ¾Ķ»į²»¾¹żĀĖÖ½¶ųÖ±½Ó“ÓĀĖÖ½ŗĶĀ©¶·Ö®¼äµÄæÕĻ¶ÖŠĮ÷¹ż£¬Ņ²»įµ¼ÖĀ¹żĀĖ³öµÄĀĖŅŗŹĒ»ģ×ĒµÄ£»NH4HCO3ŌŚČČĖ®ÖŠ»į·Ö½ā£¬ÓĆ90”ęČČĖ®Ļ“µÓFeCO3³Įµķ£¬ÄæµÄŹĒĻ“Č„±ķĆęĪüø½µÄĄė×ÓĶ¬Ź±“Ł½ųĢ¼ĖįĒāļ§µÄ·Ö½ā”£“š°øĪŖ£ŗĀĖÖ½ĘĘĖš»ņÕߏĒ¹żĀĖŹ±ĀĖŅŗ³¬¹żĀĖÖ½ÉĻŌµµČ ”¢Ļ“Č„±ķĆęĪüø½µÄĄė×ÓĶ¬Ź±“Ł½ųĢ¼ĖįĒāļ§µÄ·Ö½ā
£Ø4£©ŹµŃéŹŅÖŠ×ĘÉÕ¹ĢĢåĶس£ŌŚŪįŪöÖŠ½ųŠŠ£¬×ĘÉÕŹ±FeCO3ÓėŃõĘųŌŚøßĪĀĻĀ·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬»Æѧ·½³ĢŹ½ĪŖ£ŗ4FeCO3+O2![]() 2Fe2O3+4CO2”£“š°øĪŖ: ŪįŪö”¢4FeCO3+O2
2Fe2O3+4CO2”£“š°øĪŖ: ŪįŪö”¢4FeCO3+O2![]() 2Fe2O3+4CO2
2Fe2O3+4CO2
£Ø5£©¼ŁÉčFe2O3ĪļÖŹµÄĮæĪŖx mol£¬FeOµÄĪļÖŹµÄĮæĪŖy mol£¬ÄĒĆ“Āś×ć£ŗ160x+72y=117.6![]() ”¢2x+y=
”¢2x+y=![]() £¬½āµĆx=6
£¬½āµĆx=6![]() mol£¬ĖłŅŌ²śĪļÖŠFe2O3µÄÖŹĮæ·ÖŹżĪŖ
mol£¬ĖłŅŌ²śĪļÖŠFe2O3µÄÖŹĮæ·ÖŹżĪŖ![]() 81.6%”£“š°øĪŖ£ŗ81.6%
81.6%”£“š°øĪŖ£ŗ81.6%


 æŖŠÄĶÜדŌŖ²āŹŌ¾ķĻµĮŠ“š°ø
æŖŠÄĶÜדŌŖ²āŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ21ŹĄ¼ĶŹĒÄÉĆ×æĘ¼¼ÕøĀ¶Ķ·½ĒµÄŹ±“ś”£ĻĀĮŠ·ÖÉ¢ĻµµÄ·ÖÉ¢ÖŹĮ£×ÓÖ±¾¶ŌŚ1nm”«100nmÖ®¼äµÄŹĒ
A.ŃĪĖįB.ÕįĢĒČÜŅŗC.ÓĶĖ®»ģŗĻĪļD.Fe(OH)3½ŗĢå
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ40mLĪļÖŹµÄĮæÅضČĪŖ0.05molL-1Na2SO3ČÜŅŗĒ”ŗĆÓė25mLÅضČĪŖ0.02molL-1µÄK2X2O6ČÜŅŗĶźČ«·“Ó¦£¬ŅŃÖŖNa2SO3æɱ»K2X2O6Ńõ»ÆĪŖNa2SO4£¬ŌņŌŖĖŲXŌŚ»¹Ō²śĪļÖŠµÄ»ÆŗĻ¼ŪĪŖĻĀĮŠµÄ
A.+1¼ŪB.+2¼ŪC.+3¼ŪD.+4¼Ū
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŠčŅŖ¼ÓČėŃõ»Æ¼Į²ÅÄÜŹµĻֵıä»ÆŹĒ£Ø £©
A.MnO2”śMnSO4
B.KI”śKIO3
C.HNO 3”śNO
D.Al2O 3”śAl£ØOH£©3
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻĪŹĢā½ųŠŠ×÷“š£ŗ
£Ø1£©ŹĀŹµÖ¤Ć÷£¬ÄÜÉč¼Ę³ÉŌµē³ŲµÄ·“Ó¦Ķس£ŹĒ·ÅČČ·“Ó¦£¬ĻĀĮŠ»Æѧ·“Ó¦ŌŚĄķĀŪÉĻæÉŅŌÉč¼Ę³ÉŌµē³ŲµÄŹĒ £Ø £©
A.C£Øs£©+H2O£Øg£©=CO£Øg£©+H2£Øg£©”÷H£¾0
B.NaOH£Øaq£©+HCl£Øaq£©=NaCl£Øaq£©+H2O£Øl£©”÷H£¼0
C.2CO£Øg£©+O2£Øg£©=2CO2£Øl£©”÷H£¼0
D.2H2£Øg£©+O2£Øg£©ØT2H2O£Øl£©”÷H£¼0
£Ø2£©ŅŌKOHČÜŅŗĪŖµē½āÖŹČÜŅŗ£¬ŅĄ¾Ż£Ø1£©ÖŠĖłŃ”·“Ó¦Éč¼ĘŅ»øöŌµē³Ų£¬ĘäÕż¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗ
£Ø3£©¶ĘĶæÉ·ĄÖ¹ĢśÖĘĘ·øÆŹ“£¬µē¶ĘŹ±ÓĆĶ¶ų²»ÓĆŹÆÄ«×öŃō¼«µÄŌŅņŹĒ£ŗ
£Ø4£©ĄūÓĆČēĶ¼×°ÖĆ£¬æÉŅŌÄ£ÄāĢśµÄµē»Æѧ·Ą»¤£® ČōXĪŖĢ¼°ō£¬ĪŖ¼õ»ŗĢśµÄøÆŹ“£¬æŖ¹ŲKÓ¦øĆÖĆÓŚ £ØĢīM»ņÕßN£©“¦£¬“ĖŹ±ČÜŅŗÖŠµÄŅõĄė×ÓĻņ ¼«£ØĢīX»ņĢś£©ŅĘ¶Æ£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĮņĖįŃĒĢśļ§Ę·Ģå[(NH4)2Fe(SO4)2”¤6H2O]ÓÖ³ĘĦ¶ūŃĪ£¬ŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬ÓĆĶ¾Ź®·Ö¹ć·ŗ”£
£Ø1£©»łĢ¬Fe2+µÄŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ_____________________”£
£Ø2£©°±ŹĒŗĻ³ÉĦ¶ūŃĪµÄÖŲŅŖŌĮĻ£¬¹¤ŅµŗĻ³É°±ÖŠ£¬ŌĮĻĘųŌŚ½ųČėŗĻ³ÉĖžĒ°³£ÓĆ“×Ėį¶ž°±ŗĻĶ(I)ČÜŅŗĄ“ĪüŹÕĘäÖŠµÄŌÓÖŹCOĘųĢ壬Ęä·“Ó¦·½³ĢŹ½ĪŖ£ŗ[Cu(NH3)2]Ac+CO+NH3![]() [Cu(NH3)3]Ac”¤CO[“×ĖįōŹ»łČż°±ŗĻĶ(I)](Ac-=CH3COO-)
[Cu(NH3)3]Ac”¤CO[“×ĖįōŹ»łČż°±ŗĻĶ(I)](Ac-=CH3COO-)
¢Ł“×ĖįÖŠĢ¼Ō×ÓµÄŌӻƷ½Ź½ŹĒ_________£¬1molŅŅĖį·Ö×ÓÖŠŗ¬ÓŠ¦Ņ¼üµÄŹżÄæĪŖ_________________”£
¢ŚC”¢N”¢OČżÖÖŌŖĖŲµÄµŚŅ»µēĄėÄÜÓÉŠ”µ½“óµÄĖ³ŠņĪŖ___________________________”£
¢ŪÓėCO»„ĪŖµČµē×ÓĢåµÄ·Ö×ÓĪŖ___________£ØĢī»ÆѧŹ½£©£¬NH3µÄæռ乹ŠĶĪŖ__________________”£
£Ø3£©NŗĶP¶¼ŹĒµŚVA×åŌŖĖŲ£¬Ęä×ī¼ņµ„Ēā»ÆĪļČŪµćµÄ“󊔹ŲĻµĪŖ_________£¬Ö÷ŅŖŌŅņŹĒ__________________________________”£
£Ø4£©ĢśŌŚ²»Ķ¬ĪĀ¶Č·¶Ī§ÓŠ²»Ķ¬µÄ¾§Ģå½į¹¹”£ŹŅĪĀĻĀĢśŹĒ¼ņµ„Į¢·½£¬³ĘĪŖ¦ĮĢś(¦Į-Fe)”£µ±ĪĀ¶ČÉżøßµ½912”ę£¬¦ĮĢś×Ŗ±äĪŖĆęŠÄĮ¢·½£¬³ĘĪŖ¦ĆĢś(¦Ć-Fe)”£µ±ĪĀ¶Č¼ĢŠųÉżøßµ½1394 ”ę£¬¦ĆĢś×Ŗ±äĪŖĢåŠÄĮ¢·½”£³ĘĪŖ¦ÄĢś(¦Ä-Fe)”£

¢Ł¦ĆĢś¾§ĢåÖŠĢśŌ×ÓÅäĪ»ŹżŹĒ____________________”£
¢Ś¦ÄĢś¾§ĢåĆܶČĪŖdg”¤cm-3£¬ŌņĘ侧°ū²ĪŹż(±ß³¤)ĪŖ__________cm(°¢·ü¼ÓµĀĀŽ³£ŹżÓĆNA±ķŹ¾)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æCO2ŹĒŅ»ÖÖĮ®¼ŪµÄĢ¼×ŹŌ“£¬Ęä×ŪŗĻĄūÓĆ¾ßÓŠÖŲŅŖŅāŅ唣CO2ÓėCH4¾“ß»ÆÖŲÕū£¬ÖʵĆŗĻ³ÉĘų£ŗCH4(g)+CO2(g)![]() 2CO(g)+2H2(g)”£
2CO(g)+2H2(g)ӣ
(1)ŅŃÖŖÉĻŹö·“Ó¦ÖŠĻą¹ŲµÄ»Æѧ¼ü¼üÄÜŹż¾ŻČēĻĀ£ŗ
»Æѧ¼ü | C-H | C=O | H-H | C”ŌO(CO) |
¼üÄÜ/kJ”¤mol-1 | 413 | 745 | 436 | 1075 |
ŌņøĆ·“Ó¦µÄ”÷H=______kJ”¤mol£1”£
(2)ĪŖĮĖ¼ÓæģøĆ·“Ó¦µÄĖŁĀŹ£¬æÉŅŌ½ųŠŠµÄ“ėŹ©ŹĒ£Ø_____£©”£
A£®ŗćĪĀŗćŃ¹ĻĀ£¬°“Ō±ČĄż³äČėCH4”¢CO2
B£®ŗćĪĀĻĀ£¬ĖõŠ”ČŻĘ÷Ģå»ż
C£®Ōö“ó·“Ó¦ĪļÓė“߻ƼĮµÄ½Ó“„Ć껿
D£®½µµĶĪĀ¶Č
(3)ŗćĪĀĻĀ£¬Ļņ2LĢå»żŗć¶ØµÄČŻĘ÷ÖŠ³äČėŅ»¶ØĮæµÄCO2”¢CH4£¬Ź¹ĘäŌŚ“߻ƼĮ×÷ÓĆĻĀ½ųŠŠ·“Ó¦£¬¾tminŗ󣬲āµĆCOÓŠamol£¬Ōņv(CO2)=______”£ĻĀĮŠø÷ĻīÄÜĖµĆ÷øĆ·“Ó¦“ļµ½Ę½ŗāµÄŹĒ£Ø______£©”£
A£®ČŻĘ÷ÄŚĘųĢåĆܶȱ£³ÖŅ»¶Ø B£®ČŻĘ÷ÄŚCO2”¢CH4µÄÅضČÖ®±ČĪŖ1”Ć1
C£®øĆ·“Ó¦µÄÕż·“Ó¦ĖŁĀŹ±£³ÖŅ»¶Ø D£®ČŻĘ÷ÄŚĘųĢåŃ¹Ēæ±£³ÖŅ»¶Ø
(4)ÓĆ¼×Ķé×÷Č¼ĮĻµÄ¼īŠŌČ¼ĮĻµē³ŲÖŠ£¬µē¼«²ÄĮĻĪŖ¶ąæ׶čŠŌ½šŹōµē¼«£¬Ōņøŗ¼«µÄµē¼«·“Ó¦Ź½ĪŖ_______________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”放ӊ»ś»Æѧ»ł“””æĻćĮĻGµÄŅ»ÖÖŗĻ³É¹¤ŅÕČēĻĀĶ¼ĖłŹ¾£ŗ
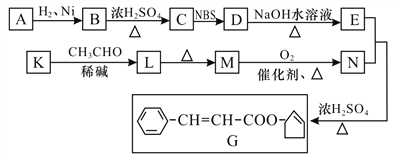
ŗĖ“Ź²ÕńĒāĘ×ĻŌŹ¾AÓŠĮ½Öַ壬ĒŅ·åĆ껿֮±ČĪŖ1”Ć1£¬ĒŅ²»ŗ¬C=C”£
ŅŃÖŖ£ŗCH3CH2CH==CH2![]() CH3CHBrCH==CH2
CH3CHBrCH==CH2
CH3CHO£«CH3CHO![]() CH3CHOHCH2CHO
CH3CHOHCH2CHO
CH3CHOHCH2CHO![]() CH3CH==CHCHO£«H2O
CH3CH==CHCHO£«H2O
Ēė»Ų“š£ŗ
£Ø1£©AµÄ½į¼ņŹ½ĪŖ_______________£¬GÖŠ³ż±½»·Ķā¹ŁÄÜĶŵÄĆū³ĘĪŖ___________________”£
£Ø2£©¼ģŃéMŅŃĶźČ«×Ŗ»ÆĪŖNµÄŹµŃé²Ł×÷ŗĶĻÖĻóŹĒ£ŗ_______________£¬ŌņMŅŃĶźČ«×Ŗ»ÆĪŖN”£
£Ø3£©ÓŠŃ§Éś½ØŅ飬½«M”śNµÄ×Ŗ»ÆÓĆKMnO4(H£«)“śĢęO2£¬ĄĻŹ¦ČĻĪŖ²»ŗĻĄķ£¬ŌŅņŹĒ_____________”£
£Ø4£©K”śLµÄ»Æѧ·½³ĢŹ½ĪŖ___________________________£¬·“Ó¦ĄąŠĶĪŖ______________”£
£Ø5£©FŹĒMµÄĶ¬ĻµĪļ£¬±ČM¶ąŅ»øöĢ¼Ō×Ó”£Āś×ćĻĀĮŠĢõ¼žµÄFµÄĶ¬·ÖŅģ¹¹ĢåÓŠ________ÖÖ(²»æ¼ĀĒĮ¢ĢåŅģ¹¹)£ŗ¢ŁÄÜ·¢ÉśŅų¾µ·“Ó¦£¬¢ŚÄÜÓėäåµÄĖÄĀČ»ÆĢ¼ČÜŅŗ¼Ó³É£¬¢Ū±½»·ÉĻÓŠ2øöČ”“ś»ł£»ÕāŠ©Ķ¬·ÖŅģ¹¹ĢåÖŠ£¬ĘäÖŠ²»ŗ¬¼×»ł”¢Ģ¼Ō×ÓŌŚ±½»·Į½²ą¶Ō³Ę·Ö²¼µÄĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½ĪŖ__________________”£
£Ø6£©ŅŌ±ūĻ©ŗĶNBSŹŌ¼ĮĪŖŌĮĻÖʱøøŹÓĶ(±ūČż“¼)£¬ĒėÉč¼ĘŗĻ³ÉĀ·Ļß(ĘäĖūĪŽ»śŌĮĻČĪŃ”)£ŗ__________”¾ĒėÓĆŅŌĻĀ·½Ź½±ķŹ¾£ŗA![]() B”
B”![]() Äæ±ź²śĪļ”攣
Äæ±ź²śĪļ”攣
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÄ³ŃŠ¾æŠ”×éŅŌ±½·ÓĪŖÖ÷ŅŖŌĮĻ£¬°“ĻĀĮŠĀ·ĻßŗĻ³ÉŅ©Īļ”Ŗ”Ŗɳ¶”°·“¼”£
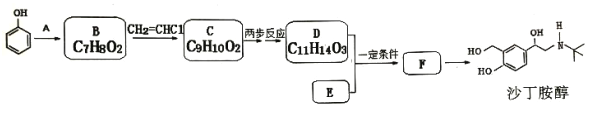
ŅŃÖŖ:£ŗ¢ŁA”śB Ō×ÓĄūÓĆĀŹĪŖ 100%
¢ŚR-OH![]() R-O-CH3£» R-O-CH3
R-O-CH3£» R-O-CH3 ![]() R-OH
R-OH
¢Ū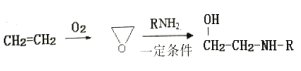
Ēė»Ų“š£ŗ
£Ø1£©Š“³ö C ÖŠ¹ŁÄÜĶŵÄĆū³Ę______________________________”£
£Ø2£©B”śC ·“Ó¦ĄąŠĶĪŖ___________________________________”£
£Ø3£©ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·ŹĒ_________”£
A£®A ŹĒ¼×Č© B£®±½·ÓÓŠ¶¾£¬µ«ÄÜÓĆӌɱ¾śĻū¶¾
C£®»ÆŗĻĪļ D Óė FeCl3ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦ D£®É³¶”°·“¼·Ö×ÓŹ½£ŗ C13H21NO3
£Ø4£©Éč¼Ę»ÆŗĻĪļ C ¾Į½²½·“Ó¦×Ŗ±äĪŖ D µÄŗĻ³ÉĀ·Ļß(ÓĆĮ÷³ĢĶ¼±ķŹ¾) _______________________________________________________________”£
£Ø5£©Š“³ö E µÄ½į¹¹¼ņŹ½_________________________________________”£
£Ø6£©Š“³ö F”ś ɳ¶”°·“¼·“Ó¦µÄĮķŅ»ÖÖ·“Ó¦ĪļŹĒ_________________________”£
£Ø7£©»ÆŗĻĪļ M ŹĒ C µÄĶ¬·ÖŅģ¹¹Ģ壬M ·ūŗĻĻĀĮŠĢõ¼žµÄĶ¬·ÖŅģ¹¹ĢåÓŠ______ÖÖ£»
¢Ł M ±½»·ÉĻÖ»ÓŠĮ½øö¶ŌĪ»Č”“ś»ł£» ¢Ś ÄÜ·¢ÉśĖ®½ā·“Ó¦£»
Š“³öĘäÖŠ 1H-NMR Ę×ÖŠÓŠ 4 ÖÖĒāŌ× M ĖłÓŠæÉÄܵĽį¹¹¼ņŹ½________________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com