
【题目】合金是一类用途广泛的金属材料。下列物质中,不属于合金的是( )
A.不锈钢B.黄铜C.硬铝D.水银
 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:
【题目】表为元素周期表的一部分,针对表中的①~⑨九种元素,请回答有关问题:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
4 | ⑧ | ⑨ |
(1)⑨的元素符号是 .
(2)在这些元素中,化学性质最不活泼的原子结构示意图为 .
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是(填化学式,下同),碱性最强的是 , 显两性的是 .
(4)将元素①与氢元素组成的最简单有机物和⑥的单质按1:1混合后的气体在光照条件下放置一段时间,最多能得到产物.
(5)用电子式表示④和⑥两元素形成化合物的过程为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘是人类必需的生命元素,在人体的生长发育过程中起着重要作用,实验小组进行碘单质的制备。
【查阅资料】碱性条件下,I2会发生歧化反应生成I-和IO3-,酸性条件下, I-和IO3-又会发生归中反应生成I2;碘在水中的溶解度为0.029g。
【碘的制取】以海带为原料,按照以下步骤进行实验。

(1)将海带灼烧成灰后再用水浸取,目的是_______________。
(2)步骤B发生的反应是“氧化”,这一操作中可供选用的试剂: ①Cl2;②Br2;③稀硫酸和H2O2,从无污染角度考虑,你认为合适试剂是______(填编号),反应中I-转化为I2 的离子反应方程式为_______________。
(3)步骤C中使用的起到分离作用的仪器是_____________,使用该仪器时,第一步操作是_______________。
(4)有同学查资料后发现CCl4有毒,提议用乙醇代替,请判断该提议是否可行,原因是_______________。
【碘的分离】得到含I2的CCl4溶液后,利用右图装置进行碘的提取并回收溶剂。

(5)图中有两处明显错误,分别是①_________;②_________。
(6)对实验装置的错误改正之后进行分离操作。预期锥形瓶中得到无色的CCl4,实验结果锥形瓶中得到紫红色液体,请分析出现该实验结果的原因____________,为了保证实验成功,请提出改进方案:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究钠及其化合物有重要意义。
(1)实验室配制0.1molL-1的碳酸钠溶液480mL,根据配制溶液的过程,回答问题:
①实验中除需要托盘天平(带砝码)、药匙、烧杯和玻璃棒外,还需要的其他玻璃仪器是_________。
②实验中需用托盘天平(带砝码)称量碳酸钠固体_______________g。
③某同学配制 Na2CO3溶液的过程如图所示。你认为该同学的错误有___________。
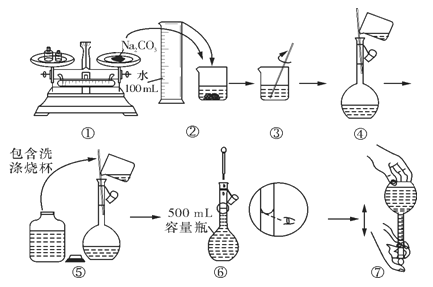
A.①⑥ B.②④⑦ C.①⑤⑥ D.⑤⑥⑦
④下列实验操作会使配得的溶液浓度偏小的是___________。
A.转移溶液后未洗涤烧杯和玻璃棒就直接定容
B.容量瓶使用前没有经过干燥,瓶中有少量的水
C.在容量瓶中定容时俯视刻度线
D.定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水至刻度
(2)过氧化钠保存不当容易变质生成Na2CO3。某过氧化钠样品已经部分变质,请你设计实验,限用一种溶液和水,证明过氧化钠已经部分变质:_________________(说明操作、现象和结论)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.92g Cu片与一定量的浓HNO3作用,当收集到NO2和NO气体共1.12L时(标准状况),金属铜恰好全部作用.则:
(1)反应中消耗HNO3mol,转移电子mol.
(2)用排水法收集生成的气体,最后气体的体积为L(标准状况).
(3)向收集到的气体中通入mL O2(标准状况)才能使水刚好充满整个集气容器.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知2H→H2放出437.6 kJ的热量,下列说法正确的是_______
A. 氢气分子内每个氢原子都达到稳定结构
B. 氢气分子的能量比两个氢原子的能量低
C. 1 mol H2 离解成 2 mol H 要放出437.6 kJ热量
D. 氢原子比氢气分子稳定
(2)已知原电池的总反应式:Cu + 2FeCl3 = CuCl2 + 2FeCl2,请写出电极反应方程式:
负极___________________________________
正极___________________________________
(3)如图所示,在锥形瓶放置装有水的小试管,往小试管中分别加入下列物质:①烧碱固体 ②浓硫酸 ③硝酸铵固体④NaCl固体,其中能使a端液面高于b端液面的是_______________。(填序号)
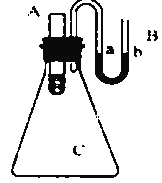
(4)科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术2H2O![]() 2H2↑+O2↑。制得的氢气可用于制作燃料电池.试回答下列问题:
2H2↑+O2↑。制得的氢气可用于制作燃料电池.试回答下列问题:
①分解海水时,实现了光能转化为______能;生成的氢气用于制作燃料电池时,实现了化学能转化为______能;分解海水的反应属于______反应(填“放热”或“吸热”)。
②某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,A极上发生的电极反应为:2H2 + 2O24e=2H2O,则A极是电池的______极,电子从该极______(填“流入”或“流出”),B极的电极反应式为:_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com