
| A、加热 |
| B、Ca(OH)2溶液 |
| C、通入过量的CO2 |
| D、NaOH溶液 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
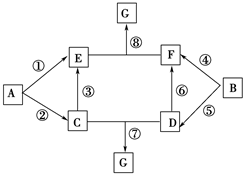 A~G的转化关系如图所示(部分反应物、产物和反应条件未标出).
A~G的转化关系如图所示(部分反应物、产物和反应条件未标出).查看答案和解析>>
科目:高中化学 来源: 题型:
A.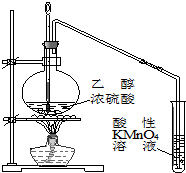 实验室制备并检验乙烯 | B.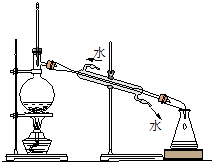 石油分馏 |
C.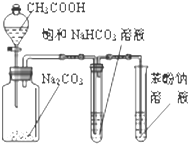 验证醋酸、碳酸、苯酚酸性强弱 | D.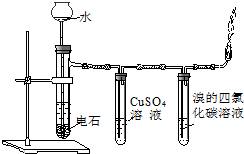 实验室制乙炔 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、阴离子的配位数:CsCl>NaCl>CaF2 |
| B、热分解温度:BaCO3>CaCO3>MgCO3 |
| C、熔点:NaF>MgF2>AlF3 |
| D、硬度:C3N4>金刚石>碳化硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含有共价键的化合物一定是共价化合物 |
| B、共价化合物也有可能含有非极性键 |
| C、离子化合物中不可能含有非极性键 |
| D、任何物质中都一定含有化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 晶体 | NaCl | MgO | AlCl3 | SiCl4 | B(硼) |
| 熔点℃ | 801 | 2852 | 180 | -70 | 2300 |
| 沸点℃ | 1465 | --- | 177 | 57 | 2500 |
| A、晶体的沸点CCl4<SiCl4 |
| B、在火山喷出的岩浆,晶出顺序为MgO先于NaCl |
| C、用AlCl3通过电解法冶炼铝 |
| D、硼的硬度大,不溶于水,但能与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O2 与水反应:2O22-+2H2O=4OH-+O2↑ |
| B、NaHCO3与盐酸:CO32-+2H+=H2O+CO2↑ |
| C、Ca(HCO3)2与过量的NaOH溶液反应:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
| D、醋酸与小苏打溶液反应H++HCO3-=CO2↑+H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com