

分析 (1)根据浓盐酸和二氧化锰的性质判断生成物,从而确定方程式;
(2)反应制得的氯气中有氯化氢和水,铝与氯化氢会产生氢气,无水氯化铝露置于潮湿空气中会爆炸并产生大量白雾,所以制取的氯气必须干燥除杂;
(3)为了制取纯净的无水氯化铝,需排净装置中的空气,点燃A酒精灯用产生的氯气来排净空气后再点燃B酒精灯开始反应制取无水氯化铝;
(4)氯化铝易升华,生成的氯化铝气体会聚集在C处;
(5)装置D既可以吸收多余的氯气,防止污染环境,又可以防止空气中的水蒸气进入D中.
解答 解:(1)浓盐酸和二氧化锰在加热条件下能发生氧化还原反应生成氯化锰、氯气、水,反应为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2 ↑+2H2O,
故答案为:MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2 ↑+2H2O;
(2)浓盐酸具有挥发性,所以混合气体中含有氯化氢,选用饱和食盐水吸收氯化氢气体,无水氯化铝露置于潮湿空气中会爆炸并产生大量白雾,所以制取的氯气必须干燥,故选取浓硫酸干燥,所以A和B间需要加适当的装置为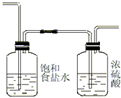 ,
,
故答案为: ;爆炸并产生大量白雾;
;爆炸并产生大量白雾;
(3)为了制取纯净的无水氯化铝,需排净装置中的空气,点燃A酒精灯用产生的氯气来排净空气后再点燃B酒精灯开始反应制取无水氯化铝,
故答案为:A;B;
(4)氯化铝在178℃升华,产物以气体形式存在,主要聚集在C处,故可以在C收集到纯净的氯化铝,
故答案为:AlCl3易升华;
(5)反应有多余的氯气需要用碱性物质吸收,还要防止空气中的水蒸气进入装置,故在D装置中加碱石灰,
故答案为:吸收多余的Cl2且防止水蒸气进入C使AlCl3发生水解.
点评 本题通过氯化铝的制取,考查了氯气的制备和性质的检验,熟悉反应原理是解题关键,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2017届江西省高三上学期期中化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.加入苯酚显紫色的溶液:K+、NH4+、Cl-、I-;加入酚酞呈红色的溶液:SO42-、K+、Cl-、HSO3- 分别都不能大量共存(常温下)
B.c(H+)/c(OH-)=1×10-12的溶液:K+、AlO2-、CO32-、Na+; pH=2的溶液:NO3-、Fe2+、Na+、Al3+分别都可以大量共存(常温下)
C.已知:25℃时,Mg(OH)2的kSP=5.61×10-12,MgF2的kSP=7.42×10-11,25℃时,在Mg(OH)2的悬浊液中加入NaF溶液后,Mg(OH)2 可以转化为MgF2
D.表示H2燃烧热的化学方程式为:H2(g)+1/2O2(g)═H2O(1);△H=-285.8kJ/mol;
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 1-乙氧基萘是一种无色液体,密度比水大,不溶于水,易溶于醇、醚,熔点5.5℃,沸点267.4℃.1乙氧基萘常用作香料,也可作为合成其他香料的原料.
1-乙氧基萘是一种无色液体,密度比水大,不溶于水,易溶于醇、醚,熔点5.5℃,沸点267.4℃.1乙氧基萘常用作香料,也可作为合成其他香料的原料.
 )
)查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有学生用五氧化二磷作为乙醇脱水制乙烯的催化剂,进行相关实验.按如表所示的量和反应条件在三颈瓶中加入一定量P2O5,再注入95%的乙醇,并加热,观察现象.
有学生用五氧化二磷作为乙醇脱水制乙烯的催化剂,进行相关实验.按如表所示的量和反应条件在三颈瓶中加入一定量P2O5,再注入95%的乙醇,并加热,观察现象.| 实验 | P2O5/g | 95%乙醇量/mL | 加热方式 |
| 实验1 | 2 | 4 | 酒精灯 |
| 实验2 | 2 | 4 | 水浴70℃ |
| 实验 | 实验现象 | ||
| 三颈瓶 | 收集瓶 | 试管 | |
| 实验1 | 酒精加入时,立刻产生白雾,当用酒精灯加热时,有气泡产生,并逐渐沸腾,生成黏稠状液体 | 有无色液体 | 溶液褪色 |
| 实验2 | 酒精加入时,立刻产生白雾,当用水浴加热时,不产生气泡,一段时间后,反应瓶内生成黏稠状液体 | 有无色液体 | 溶液不褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上期中化学试卷(解析版) 题型:选择题
有关晶体的下列说法中正确的是
A.晶体中分子间作用力越大,分子越稳定
B.原子晶体中共价键越强,熔点越高
C.冰熔化时水分子中共价键发生断裂
D.氯化钠熔化时离子键未被破坏
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com