
| 元素 | Al | B | Be | C | Cl | X | Li |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 |
| 元素 | Mg | N | Y | O | P | S | Si |
| 电负性 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
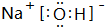 、该物质中的化学键为离子键、共价键.
、该物质中的化学键为离子键、共价键.分析 (1)电负性表示对键合电子的吸引力,电负性越大对键合电子吸引力越大,所以电负性越强非金属性越强;
(2)由表中数据可知,同周期自左而右电负性增大,同主族自上而下电负性降低,所以Y为Na、X为F,Y元素与氧元素、氢元素形成化合物为NaOH,由钠离子与氢氧根离子构成;
(3)Y的最高价氧化物水化物为NaOH,与Al反应生成偏铝酸钠与氢气,反应中所含元素化合价升高的反应物为还原剂.
解答 解:(1)电负性表示对键合电子的吸引力,电负性越大对键合电子吸引力越大,所以电负性越强非金属性越强,故答案为:非金属性;
(2)由表中数据可知,同周期自左而右电负性增大,同主族自上而下电负性降低,Y电负性为0.9,介于Li1.0和Mg1.2间为Na,X电负性最大,为F元素,Y元素与氧元素、氢元素形成化合物为NaOH,由钠离子与氢氧根离子构成,其电子式为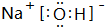 ,含有离子键、共价键,
,含有离子键、共价键,
故答案为:Na;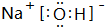 ;离子键、共价键;
;离子键、共价键;
(3)Y的最高价氧化物水化物为NaOH,与Al反应生成偏铝酸钠与氢气,反应离子方程式为:2Al+2OH-+2H2O═2AlO2-+3H2↑,反应中Al元素化合价升高,故Al为还原剂,
故答案为:2Al+2OH-+2H2O═2AlO2-+3H2↑;Al.
点评 本题考查元素周期律,涉及电负性与金属性非金属性的关系、电子式及离子方程式书写、化学键等,题目难度不大,注意理解主族元素电负性的递变规律,注意相关基础知识的积累.


 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酯化反应、硝化反应以及酯的水解均属于取代反应类型 | |
| B. | 乙醇生成溴乙烷和乙烯生成溴乙烷的反应类型相同 | |
| C. | 可用氢氧化钠溶液除去乙酸乙酯中混有的乙酸和乙醇 | |
| D. | 甲烷、苯都属于烃,都不存在同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素W:位于元素周期表中的第三周期,ⅢA族 | |
| B. | 元素X:它的原子中M层比L层少2个电子 | |
| C. | 元素Y:它的焰色反应颜色呈黄色 | |
| D. | 元素Z:它的二价阳离子核外电子总数与氩原子相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+、NO3-、NH4+、Cl- | B. | Mg2+、NH4+、SO42-、K+ | ||
| C. | K+、Ba2+、Cl-、HSO3- | D. | Ca2+、HCO3-、NH4+、AlO2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2+HCl$→_{△}^{催化剂}$CH3CH2Cl | |
| B. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | |
| C. | 2CH3CHO+O2$→_{△}^{催化剂}$2CH3COOH | |
| D. | CH3CH2Br+NaOH$\stackrel{乙醇}{→}$CH2=CH2↑+NaBr+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于18s | B. | 等于12s | C. | 大于18s | D. | 小于18s |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com