
下列溶液中离子浓度关系的表示正确的是( )
A.NaHCO3溶液中:c(H+)+c(Na+)=c(OH-)+c(CO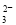 )+c(HCO
)+c(HCO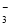 )
)
B.pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后的溶液中:c(OH-)>c(H+)+c(CH3COO-)
C.0.1 mol·L-1的NH4Cl溶液中:c(Cl-)>c(H+)>c(NH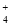 )>c(OH-)
)>c(OH-)
D.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合后的溶液中:
2c(Na+)=c(CH3COOH)+c(CH3COO-)
D
【解析】
试题分析:A.根据电荷守恒可知NaHCO3溶液中:c(H+)+c(Na+)=c(OH-)+2c(CO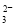 )+c(HCO
)+c(HCO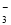 ),错误;B.由于醋酸是弱酸,NaOH是强碱,所以pH=3的CH3COOH溶液与pH=11的NaOH溶液中c(CH3COOH)>c(NaOH)。等体积混合后的溶液中含有CH3COOH和CH3COONa.由于酸过量,醋酸的电离作用大于醋酸根离子的水解作用,所以c(H+) >c(OH-),错误;C.0.1 mol·L-1的NH4Cl溶液中:由于铵根离子的水解作用消耗,所以c(Cl-)> )>c(NH
),错误;B.由于醋酸是弱酸,NaOH是强碱,所以pH=3的CH3COOH溶液与pH=11的NaOH溶液中c(CH3COOH)>c(NaOH)。等体积混合后的溶液中含有CH3COOH和CH3COONa.由于酸过量,醋酸的电离作用大于醋酸根离子的水解作用,所以c(H+) >c(OH-),错误;C.0.1 mol·L-1的NH4Cl溶液中:由于铵根离子的水解作用消耗,所以c(Cl-)> )>c(NH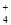 )。水解消耗水电离产生的氢氧根离子,破坏了水的电离平衡,最终使溶液中c(H+>c(OH-),但是盐的水解作用程度是微弱的,所以c(NH
)。水解消耗水电离产生的氢氧根离子,破坏了水的电离平衡,最终使溶液中c(H+>c(OH-),但是盐的水解作用程度是微弱的,所以c(NH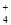 )>c(H+)。因此溶液中离子浓度的关系是:c(Cl-) >c(NH
)>c(H+)。因此溶液中离子浓度的关系是:c(Cl-) >c(NH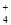 )>c(H+) >c(OH-),错误;D.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合后的溶液中,根据物料守恒可得:2c(Na+)=c(CH3COOH)+c(CH3COO-),正确。
)>c(H+) >c(OH-),错误;D.物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合后的溶液中,根据物料守恒可得:2c(Na+)=c(CH3COOH)+c(CH3COO-),正确。
考点:考查溶液中离子浓度的大小比较的知识。


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源:2013-2014湖南省五市十校高一下学期期中教学质量检测化学试卷(解析版) 题型:选择题
下列有关化学反应速率的说法中,正确的是
A.往容积一定的容器中再通入O2,可以加快反应2SO2+O2 2SO3的反应速率
2SO3的反应速率
B.用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率
C.对于C(s)+H2O(g)  CO(g)+H2(g)的反应,加入固体炭,反应速率加快
CO(g)+H2(g)的反应,加入固体炭,反应速率加快
D.100 mL 2 mol·L-1的盐酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南师大附中第二学期期中考试高一化学试卷(解析版) 题型:填空题
(11分)在第3周期中,置换酸中氢的能力最强的元素的元素符号为 ,化学性质最稳定的元素符号是 ,最高价氧化物的水化物的酸性最强的化合物的化学式是 ,最高价氧化物的水化物的碱性最强的化合物的化学式是 ,显两性的氢氧化物的化学式是 ,该两性氢氧化物与盐酸、氢氧钠溶液分别反应的离子方程式为 、 ,原子半径最大的金属元素的名称是 ,离子半径最小的离子结构示意图是 。
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省黄石市秋季高二化学期中统考试卷(解析版) 题型:填空题
(17分)X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为 、 ;
(2)XZ2与YZ2分子的杂化轨道分别是 、 ,立体结构分别是 、 ,相同条件下两者在水中的溶解度较大的是 (写分子式),理由是 ;
(3)Q的元素符号是 ,它属于第 周期,它的核外电子排布式为 ,在形成化合物时它的最高化合价为 ;
(4)用氢键表示式 写出E的氢化物溶液中存在的所有氢键_______________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省黄石市秋季高二化学期中统考试卷(解析版) 题型:选择题
下图甲池和乙池中的四个电极都是惰性材料,乙池溶液分层,上层溶液为盐溶液,呈中性。请根据图示判断下列有关说法不正确的是( )

A.甲池是原电池、乙池是电解池
B.通入乙醇的惰性电极的电极反应式为:C2H5OH+16OH--12e-=2CO32-+11H2O
C.反应一段时间后,两池溶液的pH均未变化
D.假如乙池中加入NaI溶液,则在乙池反应过程中,可以观察到C电极周围的溶液呈现棕黄色,反应完毕后,用玻璃棒搅拌溶液,则下层溶液呈现紫红色,上层接近无色
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省黄石市秋季高二化学期中统考试卷(解析版) 题型:选择题
以下说法正确的是( )
A.不能自发进行的反应属于吸热反应
B.化学键断裂时吸收的能量大于化学键形成时放出的能量的反应属于放热反应
C.升高反应的温度,活化分子百分数增加,分子间有效碰撞的几率提高,反应速率增大
D.催化剂通过改变反应路径,使反应速率增大,但不改变反应所需的活化能
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省高三5月模拟考试理综化学试卷(解析版) 题型:填空题
(14分)(1)NO2有较强的氧化性,能将SO2氧化生成SO3,本身被还原为NO,已知下列两反应过程中能量变化如图所示:

则NO2氧化SO2的热化学方程式为_________________________________。
(2)在2L密闭容器中放入1mol氨气,在一定温度进行如下反应:2NH3(g) N2(g)+3H2(g),
N2(g)+3H2(g),
反应时间(t)与容器内气体总压强(p)的数据见下表
时间t/min | 0 | 1 | 2 | 3 | 4 | 5 |
总压强p 100 kPa | 5 | 5.6 | 6.4 | 6.8 | 7 | 7 |
则平衡时氨气的转化率为___________。
(3)25℃,某二元弱酸H2A与NaOH溶液反应可生成NaHA、Na2A,溶液中含A各微粒的分布分数(平衡时某含A微粒的浓度占各含A微粒浓度之和的分数)随溶液变化的情况如下图所示:
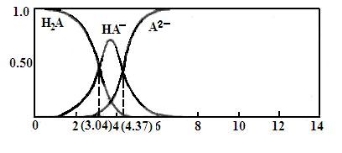
已知:103.04=1.1×103,104.37=2.3×104 25℃,Ka1(H2CO3)= 4.4×10-7 Ka2(H2CO3) = 4.7×10-11
①若向0.1NaHAmol·L-1溶液中加入少量NaOH溶液,c(A2-)/c(HA-)的值 (填“增大”、“减小”或“不变”,下同),c(H+)/c(OH-) 的值 。
②若向0.1NaHAmol·L-1溶液中加入氨水至溶液呈中性,则c(H2A)+c(NH4+) c(A2-) (填“大于”、“小于”或“等于”)。
③计算HA-二级电离平衡常数Ka2= 。
④将过量H2A加入Na2CO3溶液中反应的离子方程式为: 。
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省高一下学期期中联考化学试卷(解析版) 题型:选择题
关于下列图示的说法正确的是
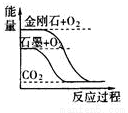

A.图①表示石墨转变为金刚石是吸热反应
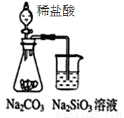
B.图②所示实验可比较非金属性强弱:氯﹥碳﹥硅
C.图③吸收NH3并防倒吸
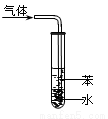
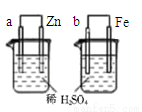
D.图④两装置中金属电极a、b都有气体产生,可判断金属活动性:a﹤b
查看答案和解析>>
科目:高中化学 来源:2013-2014湖北省武汉外国语学校高一下学期期中考试化学试卷(解析版) 题型:选择题
某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,该元素
A.在自然界中只以化合态的形式存在B.单质常用作半导体材料和光导纤维
C.最高价氧化物不与酸反应D.气态氢化物比甲烷稳定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com