
【题目】CoCl26H2O是一种饲料营养强化剂.一种利用水钴矿(主要成分为Co2O3、Co(OH)3 , 还含少量Fe2O3、Al2O3、MnO等)制取CoCl26H2O的工艺流程如图1: 
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:(金属离子浓度为:0.01mol/L)
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③CoCl26H2O熔点为86℃,加热至110~120℃时,失去结晶水生成无水氯化钴.
(1)写出浸出过程中Co2O3发生反应的离子方程式 .
(2)写出NaClO3发生反应的主要离子方程式;若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式 .
(3)“加Na2CO3调pH至a”,过滤所得到的沉淀成分为 .
(4)“操作1”中包含3个基本实验操作,它们依次是、和过滤.制得的CoCl26H2O在烘干时需减压烘干的原因是 .
(5)萃取剂对金属离子的萃取率与pH的关系如图2.向“滤液”中加入萃取剂的目的是;其使用的最佳pH范围是 . A.2.0~2.5 B.3.0~3.5
C.4.0~4.5 D.5.0~5.5
(6)为测定粗产品中CoCl26H2O含量,称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl26H2O的质量分数大于100%,其原因可能是 . (答一条即可)
【答案】
(1)Co2O3+SO32﹣+4H+=2Co2++SO42﹣+2H2O
(2)ClO3﹣+6Fe2++6H+=Cl﹣+6Fe3++3H2O;ClO3﹣+5Cl﹣+6H+=3Cl2↑+3H2O
(3)Fe(OH)3、Al(OH)3
(4)蒸发浓缩;冷却结晶;降低烘干温度,防止产品分解
(5)除去溶液中的Mn2+;B
(6)粗产品含有可溶性氯化物或晶体失去了部分结晶水
【解析】解:(1)向水钴矿[主要成分为Co2O3、Co(OH)3 , 还含少量Fe2O3、Al2O3、MnO等],加入盐酸和亚硫酸钠,浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等,所以Co2O3和亚硫酸钠在酸性条件下发生氧化还原,根据电荷守恒和得失电子守恒,反应的离子方程式为:Co2O3+SO32﹣+4H+=2Co2++SO42﹣+2H2O,所以答案是:Co2O3+SO32﹣+4H+=2Co2++SO42﹣+2H2O; (2)NaClO3的作用是将Fe2+氧化成Fe3+ , 其反应的离子方程式为:ClO3﹣+6Fe2++6H+=Cl﹣+6Fe3++3H2O;在酸性条件下,NaClO3与氯离子发生氧化还原反应生成氯气,其反应的离子方程式为:ClO3﹣+5Cl﹣+6H+=3Cl2↑+3H2O;所以答案是:ClO3﹣+6Fe2++6H+=Cl﹣+6Fe3++3H2O;ClO3﹣+5Cl﹣+6H+=3Cl2↑+3H2O;(3)NaClO3的作用是将Fe2+氧化成Fe3+ , 加Na2CO3调pH至a,铝离子能与碳酸根离子发生双水解生成氢氧化铝和二氧化碳,水解的离子方程式为:2Al3++3CO32﹣+3H2O=2Al(OH)3↓+3CO2↑;铁离子能与碳酸根离子发生双水解生成氢氧化铁和二氧化碳,水解的离子方程式为:2Fe3++3CO32﹣+3H2O=2Fe(OH)3↓+3CO2↑,所以沉淀成分为:Fe(OH)3、Al(OH)3 , 所以答案是:Fe(OH)3、Al(OH)3;(4)利用从溶液中制取固体的方法制取氯化钴固体,其操作步骤为:蒸发浓缩、冷却结晶和过滤;根据题意知,CoCl26H2O常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴,为防止其分解,制得的CoCl26H2O需减压烘干,所以答案是:蒸发浓缩;冷却结晶;降低烘干温度,防止产品分解;(5)根据流程图可知,此时溶液中存在Mn2+、Co2+金属离子;由萃取剂对金属离子的萃取率与pH的关系可知,调节溶液PH在3.0~3.5之间,可使Mn2+完全沉淀,并防止Co2+转化为Co(OH)2沉淀,所以答案是:除去溶液中的Mn2+;B; (6)根据CoCl26H2O的组成分析,造成产品中CoCl26H2O的质量分数大于100%的原因可能是:含有杂质,导致氯离子含量大或结晶水化物失去部分水,导致相同质量的固体中氯离子含量变大, 所以答案是:粗产品含有可溶性氯化物或晶体失去了部分结晶水.


科目:高中化学 来源: 题型:
【题目】常见无机物A、B、C、D、E、X存在如图转化关系.已知A、B、C、D的焰色反应都呈黄色,其中A为单质,X是常见的无色无味气体.(部分生成物和反应条件略去)请回答:
(1)组成单质A的元素符号为 , E的电子式 .
(2)写出由C转化为D的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图所示的原电池,下列说法正确的是( ) 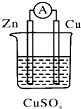
A.电流从锌电极通过电流表流向铜电极
B.锌电极发生还原反应,铜电极发生氧化反应
C.当有13 g Zn溶解时,外电路中就有0.4 mol电子通过
D.铜电极作正极,发生的电极反应为2H++2e﹣═H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能在溶液中大量共存的一组离子是( )
A.Cu2+、SO ![]() 、OH﹣、K+
、OH﹣、K+
B.Fe3+、SCN﹣、Cl﹣、H+
C.K+、CO ![]() 、Cl﹣、H+
、Cl﹣、H+
D.H+、Na+、Cl﹣、SO ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于Na2CO3与NaHCO3的性质判断正确的是( )
A.常温下溶解度:Na2CO3<NaHCO3
B.热稳定性:Na2CO3<NaHCO3
C.与同浓度同体积的盐酸反应的速率:Na2CO3>NaHCO3
D.与澄清石灰水反应,均有白色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意解答
(1)反应3A(g)+B(g)═2C(g)在三种不同的条件下进行反应,在同一时间内,测得的反应速率用不同的物质表示为①vA=1 mol/(Lmin)、②vC=0.5mol/(Lmin)、③vB=0.5mol/(Lmin),三种情况下该反应速率由大到小的关系是 . (用序号表示)
(2)某温度时,在一个5L的恒容容器中,X、Y、Z均为气体,三种物质的量随时间的变化曲线如图所示.根据图中数据填空: 
①该反应的化学方程式为 .
②反应开始至2min,以气体Z表示的平均反应速率为 .
③2min反应达平衡容器内混合气体的平均相对分子质量比起始时(填“大”,“小”或“相等”下同),混合气体密度比起始时 .
④上述反应,在第2min时,X的转化率为 .
⑤将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n (X)=n (Y)=n (Z),则原混合气体中a:b= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】要证明CuSO4溶液显蓝色不是由于SO42﹣造成的,下列实验无意义的是( )
A.观察K2SO4溶液的颜色
B.加水稀释CuSO4溶液,溶液颜色变浅
C.向CuSO4溶液中滴加过量NaOH溶液,振荡后静置,溶液变成无色
D.向CuSO4溶液中滴加过量Ba(NO3)2溶液,振荡后静置,溶液未变成无色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学兴趣小组对以下三种品牌牙膏中摩擦剂成分进行调查,结果如下表.
牙膏品牌 | 两面针儿童牙膏 | 珍珠防臭牙膏 | 中华透明牙膏 |
摩擦剂 | 氢氧化铝 | 碳酸钙 | 二氧化硅 |
试回答下列问题:
(1)上述三种摩擦剂中属于酸性氧化物的是(填化学式,下同);既能与强酸反应又能与强碱反应的是 .
(2)两面针儿童牙膏中摩擦剂成分与NaOH溶液反应的离子方程式是 .
(3)从摩擦剂成分考虑,向珍珠防臭牙膏样品中滴加少量稀盐酸,可观察到的现象是 , 该反应的化学方程式为 .
(4)中华透明牙膏摩擦剂SiO2是工业制备晶体硅的原料,其反应原理是(用化学反应方程式表示).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.
(1)工业上制备ClO2的反应原理常采用:2NaClO3+4HCl=2ClO2↑+Cl2↑+2H2O+2NaCl.
①浓盐酸在反应中显示出来的性质是(填序号).
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
②若上述反应中产生0.1mol ClO2 , 则转移电子的物质的量为mol.
(2)目前已开发出用电解法制取ClO2的新工艺. 
①如图示意用石墨做电极,在一定条件下电解饱和食盐水制取ClO2 . 写出阳极产生ClO2的电极反应式: .
②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解.通过阳离子交换膜的阳离子的物质的量为mol;用平衡移动原理解释阴极区pH增大的原因 .
(3)ClO2对污水中Fe2+、Mn2+、S2﹣和CN﹣等有明显的去除效果.某工厂污水中含CN﹣ a mg/L,现用ClO2将CN﹣氧化,只生成两种气体,其离子反应方程式为;处理100m3这种污水,至少需要ClO2mol.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com