
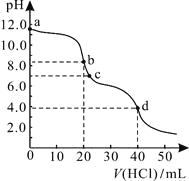
【题目】常温下,用0.1000 mol/L的盐酸滴定20.00 mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示。下列有关叙述正确的是
A. a点溶液呈碱性的原因用离子方程式表示为:CO![]() +2H2O
+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
B. c点处的溶液中c(Na+)-c(Cl-)=c(HCO![]() )+2c(CO
)+2c(CO![]() )
)
C. 滴定过程中使用甲基橙作为指示剂比酚酞更准确
D. d点处溶液中水电离出的c(H+)大于b点处
【答案】B
【解析】试题分析:A. a点溶液中的溶质为碳酸钠,碳酸钠水解溶液显碱性,碳酸钠的水解分步进行,故A错误;B. c点溶液呈中性,电荷守恒有c(Na+)+ c(H+)=c(Cl-)+ c(HCO![]() )+2c(CO
)+2c(CO![]() )+ c(OH-),因为c(H+)=c(OH-),所以c(Na+)=c(Cl-)+ c(HCO
)+ c(OH-),因为c(H+)=c(OH-),所以c(Na+)=c(Cl-)+ c(HCO![]() )+2c(CO
)+2c(CO![]() ),即c(Na+)-c(Cl-)=c(HCO
),即c(Na+)-c(Cl-)=c(HCO![]() )+2c(CO
)+2c(CO![]() ),故B正确;C. 根据图像,滴定终点有2个,1个在pH等于8左右,应该选用酚酞作指示剂,1个在pH等于4左右,应该选用甲基橙作指示剂,故C错误;D. d点溶液显酸性,是碳酸的电离导致的,水的电离受到抑制,b点处溶液显碱性,是碳酸氢钠水解导致的结果,水的电离受到促进,因此b点处溶液中水电离出的c(H+)大于d点,故D错误;故选B。
),故B正确;C. 根据图像,滴定终点有2个,1个在pH等于8左右,应该选用酚酞作指示剂,1个在pH等于4左右,应该选用甲基橙作指示剂,故C错误;D. d点溶液显酸性,是碳酸的电离导致的,水的电离受到抑制,b点处溶液显碱性,是碳酸氢钠水解导致的结果,水的电离受到促进,因此b点处溶液中水电离出的c(H+)大于d点,故D错误;故选B。


科目:高中化学 来源: 题型:
【题目】100g浓度为18 mol/L密度为ρ g/mL 的浓硫酸中加入一定的水稀释成9 mol/L的硫酸,则加入水的体积为 ( )
A. 小于100mL B. 等于100mL
C. 大于100mL D. 等于100/ρmL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业涉及固体燃料的气化,需要研究CO2与CO之间的转化。为了弄清其规律,让一定量的CO2与足量碳在体积可变的密闭容器中反应:C(s)+CO2(g)![]() 2CO(g) H,测得压强、温度对CO、CO2的平衡组成的影响如图所示:
2CO(g) H,测得压强、温度对CO、CO2的平衡组成的影响如图所示:

回答下列问题:
(1)p1、p2、p3的大小关系是______________,欲提高C与CO2反应中CO2的平衡转化率,应采取的措施为 。图中a、b、c三点对应的平衡常数大小关系是____________。
(2)900 ℃、1.013 MPa时,1 mol CO2与足量碳反应达平衡后容器的体积为V,CO2的转化率为_________,该反应的平衡常数K= 。
(3)将(2)中平衡体系温度降至640 ℃,压强降至0.1013 MPa,重新达到平衡后CO2的体积分数为50%。条件改变时,正反应和逆反应速率如何变化?____________,二者之间有何关系?___________。
(4)一定条件下,在CO2与足量碳反应所得平衡体系中加入H2和适当催化剂,有下列反应发生:
CO(g)+3H2(g)![]() CH4(g)+H2O(g) H1=-206.2 kJ/mol
CH4(g)+H2O(g) H1=-206.2 kJ/mol
CO(g)+H2O(g)![]() CO2(g)+H2(g) H2=-41.2 kJ/mol
CO2(g)+H2(g) H2=-41.2 kJ/mol
① 则二氧化碳与氢气反应转化为甲烷和水蒸气的热化学方程式是_________________。
② 已知298 K时相关化学键键能数据为:
化学键 | H—H | O—H | C—H |
|
E/(kJ·mol-1) | 436 | 465 | 413 | 1076 |
则根据键能计算,H1= ,它与上述实测值差异较大的原因可能是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是

A.电极B上发生的电极反应为:O2+2CO2+4e-=2CO32-
B.电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O
C.电池工作时,CO32-向电极B移动
D.反应CH4+H2O![]() 3H2+CO,每消耗1molCH4转移12mol
3H2+CO,每消耗1molCH4转移12mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W代表原子序数依次增大的四种短周期主族元素,它们满足以下条件:①在元素周期表中,Z与Y、W均相邻;②X、Y、W分别位于不同周期;③Y、Z、W三种元素的原子最外层电子数之和为17.下列说法正确的是 ( )
A. X、Y、Z既能形成离子化合物,又能形成共价化合物
B. 元素的原子半径由小到大的顺序为r(Y)<r(Z)
C. X与其余三种元素之间形成的核外电子总数为10的微粒只有4种
D. H2Z的熔点比H2W高,是因为H2Z分子内存在氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 某物质在熔融态钠导电,则该物质一定是离子化合物
B. 金刚石和C60熔化过程中破坏微粒间的作用力相同
C. 常温常压下,气态单质分子中,每个原子的最外层都具有8电子稳定结构
D. 液氯与水的反应需要克服分子间作用力和共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com