
下图为盐酸厂废水处理示意图,排污口流出的废水用碱液池流出的碱中和。已知废水中盐酸的质量分数为0.73%,且废水的流量为5.0kg / s(即每秒钟排出5kg废水)。
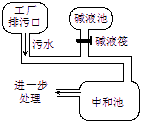
(1)若碱液是NaOH溶液,且流量为1.0kg/s,则该碱液的质量分数是多少?
(2)现将碱液改为K2CO3溶液,将实现既中和废水、又得到钾肥(KCl)之目的。若K2CO3溶液质量分数与NaOH溶液相等,则K2CO3溶液流量是多少?
科目:高中化学 来源: 题型:
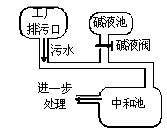
下图为某盐酸厂废水处理示意图,排污口流出的废水用碱液池流出的碱液中和。已知废水中盐酸的质量分数为0.73%,且废水的流量为5.0kg?s-1(即每秒钟排出5kg废水)。
(1)若碱液是NaOH溶液,且流量为1.0kg?s-1,则该碱液的质量分数是多少?
(2)现将碱液改为K2CO3溶液,将实现既中和废水又得到钾肥(KCl)之目的。若K2CO3溶液的质量分数与NaOH溶液的相等,则K2CO3溶液的流量是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com