
| 粒子符号 | 质子数Z | 中子数N | 核外电子数 | 质量数A |
| Cl | 17 | 20 | | |
| S2- | | | 18 | 32 |
| Al3+ | | 14 | | 27 |
| AYm- | | y | | A |
| AXn+ | x | | | A |
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源:不详 题型:填空题
| 氢化物 | A | B | HF | D | E |
| 沸点/℃ | 1317 | 100 | 19.5 | 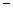 33.35 33.35 | 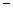 164 164 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 2 | | | | a | b | | |
| 3 | d | e | f | g | | h | i |
| A.①③④ | B.②③⑤ | C.②④⑤ | D.①③⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X可以形成钠盐,其化学式为NaX | B.X的最高价氧化物的水化物是强酸 |
| C.X的最高价氧化物的化学式为X2O7 | D.X的单质为双原子分子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该元素原子的摩尔质量为118g/mol |
| B.该元素属于金属元素 |
| C.该元素原子核内的中子数和核外电子数之差为57 |
| D.该元素原子的质量为293 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com