
【题目】废旧无汞碱性锌锰电池可用于制造隐形战机的机身涂料MnxZn(1-x)Fe2O4,该电池工作反应原理为Zn+2MnO2+2H2O![]() 2MnO(OH)+Zn(OH)2。某化学小组利用废电池制涂料的工艺如下:
2MnO(OH)+Zn(OH)2。某化学小组利用废电池制涂料的工艺如下:
A.浸取:将去除表面塑料的旧电池加入水中浸取并过滤,滤液经操作a得KOH固体;
B.溶液:滤渣中加入过量稀硫酸和足量双氧水,至不再出现气泡时,过滤;
C.测成分:测步骤B中滤液成分,然后加入铁粉;
D.氧化:加入双氧水氧化;
E.调pH:滴加氨水调pH,经结晶处理得MnxZn(1-x)Fe2O4。
(1)浸取时的操作有 ______。
A.拆解、粉碎旧电池 B.降低温度 C.搅拌 D.加压
(2)操作a为________。
(3)溶渣时生成Mn2+的主要离子方程式为______________________________。
(4)若步骤C测得滤液中金属离子组成为:c(Mn2+) +c(Zn2+) =0.8mol/L, c(Fe2+ ) = 0. 1 mol/L。若滤液体积为lm3,要合成MnxZn(1-x)Fe2O4,需加入Fe粉质量为___________kg(忽略体积变化)。
(5)氧化时,因为分解所需双氧水的量比理论值大得多。其原因可能是①温度过高;②______。
(6)最后一步结晶时,处理不当易生成MnFe2O4和ZnFe2O4。要制得MnxZn(1-x)Fe2O4,最后一步结晶时需注意______________________。
(7)某小组构想用ZnSO4、MnSO4溶液为原料,以Fe作电极用电解法经过一系列步骤制得MnxZn(1-x)Fe2O4,则开始电解时阳极反应式为___________________________________。
【答案】 A C 蒸发至有晶胶产生停止加热 2MnO(OH)+H2O2+4H+==2Mn2++O2↑+4H2O 84 生成Fe3+起催化作用促使H2O2分解 均匀结晶(或搅拌均匀) Fe-2e-=Fe2+
【解析】本题考查化学工艺流程,(1)浸取时,需要拆解、粉碎电池,为了加速溶解,需要进行搅拌,故选项A和C正确;(2)KOH溶于水,从滤液中得到KOH,需要进行蒸发至有晶胶产生,停止加热;(3)根据步骤B,滤渣中加入硫酸和足量的双氧水,双氧水的目的是还原+3价Mn,本身被氧化成O2,因此离子反应式为MnO(OH)+H++H2O2→Mn2++H2O+O2↑,Mn的化合价由+3价→+2价,化合价降低1价,H2O2中O共升高2价,最小公倍数为2,然后根据原子守恒和电荷守恒,离子反应方程式为:2MnO(OH)+4H++H2O2=2Mn2++4H2O+O2↑;(4)根据合成物质,得出Zn2+和Mn2+物质的量总和与Fe原子物质的量之比为1:2,因此有0.8×103/[0.1×103+n(Fe)]=1:2,解得n(Fe)=1.5×103mol,即质量为84kg;(5)氧化时,把Fe2+氧化成Fe3+,Fe3+作催化剂,使H2O2分解;(6)均匀结晶或搅拌均匀;(7)因为制备的物质中含有铁元素,因此需要铁电极放电,即铁电极作阳极,电极反应式为Fe-2e-=Fe2+。


 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源: 题型:
【题目】某有机物的结构为右图所示,关于这种有机物不正确的说法有( )

①该物质分子式为C11H12O3,能溶于水;
②能使溴水、酸性KMnO4溶液褪色,且原理相同;
③与Na、NaHCO3反应两者物质的量之比均是1:1;
④能发生取代、加成、水解、氧化、还原反应
A. 1种 B. 2种 C. 3种 D. 4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年10月17日我国神舟十一号载人飞船在酒泉卫星发射中心成功发射,为我们更好地掌握空间交会对接技术、开展地球观测活动奠定了基础。我国制造航天飞船的主要材料是铝,因而其也被称为会飞的金属,请根据其性质回答下列问题:
(1)现在工业冶炼铝的化学方程式为 。
(2)铝锂合金是今年来航空金属材料中发展最为迅速的一个领域,主要因为合金的某些性能优于各成分金属,其中包括 、 等方面。同时铝锂形成化合物LiAlH4既是金属储氢材料又是有机合成中的常用试剂,遇水能得到无色溶液并剧烈分解释放出H2,LiAlH4在化学反应中通常作
(填“氧化”或“还原”)剂。
(3)铝电池性能优越,在现代生产、生活中有广泛的应用。
①Al-Ag2O电池可用作水下动力电源,化学反应为2Al+3Ag2O+2NaOH=2NaAlO2+6Ag+H2O,则负极的电极反应式为 ,正极附近溶液的pH (填“变大”“不变”或“变小”),
②铝一空气电池以其环保、安全而受到越来越多的关注,其原理如下图所示。

该电池的负极反应方程式为 ;正极反应方程式为 ;
电池中NaCl溶液的作用是 ;以该电池为电源,用惰性电极电解Na2SO4溶液,当Al电极质量减少1.8g时,电解池阴极生成的气体在标准状况下的体积为 L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学活动小组设计以下装置进行不同的实验。

已知苯、溴苯的有关物理性质如下表:
苯 | 溴 | 溴苯 | |
密度/g·cm-3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
在水中的溶解度 | 微溶 | 微溶 | 微溶 |
(1)若小组同学欲用装置A、C制备溴苯,则A中反应的方程式____________, A处长导管的作用是冷凝回流,回流的主要物质有______________________(填化学式)实验结束后,向A中依次用10 mL水、8 mL 10%的NaOH溶液、10 mL水洗涤,分液得粗溴苯,NaOH溶液洗涤的作用是____________;若进一步提纯粗产品,依次进行的实验操作名称是___________、__________。
(2)若小组同学欲在B 装置中用正丁醇、冰醋酸合成一种水果香精,则还需连接的装置是________(填序号),该装置中应加入试剂________。反应结束后,取下收集装置充分振荡后静置,分去水层,可得乙酸正丁酯粗产品。现要回收水层中的有机物,依次进行的实验操作名称及相关试剂为________、________、__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
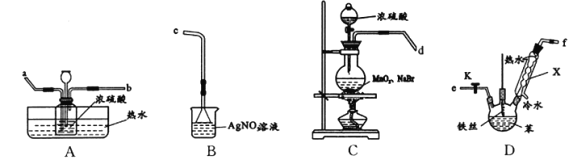
【题目】某化学小组欲通过实验探究:I.苯与液溴发生取代反应;Ⅱ.苯与液溴在催化剂作用下的反应机理。所用装罝如图所示。
已知:MnO2+2NaBr+2H2SO4![]() Br2↑+MnSO4+Na2SO4+2H2O
Br2↑+MnSO4+Na2SO4+2H2O
(1)实验室制备溴苯的化学方程式为___________________;仪器X的名称为___________。
(2)制取溴苯的实验操作步骤如下:
①连接装罝,其接口顺序为(填字母):d接____, _____接_____, ______接c;
②检査装置气密性;
③C中加入固体药品,_______,再打开D处开关K,点燃C处酒精灯;插入铁丝于混合液中,一段时间后,D中液体沸腾,原因是_________ ;
④关闭C中活塞。
(3)A中对广口瓶进行热水浴的目的是 _______________。
(4)若B中有淡黄色沉淀生成,能否确定苯与液溴发生了取代反应?_____(答“能”或“否”)。
(5)査阅文献:苯与液溴在FeBr3催化下的反应机理共分三步:
I Br2+FeBr3![]() Br++FeBr4-
Br++FeBr4-
Ⅱ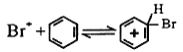
①请完成第三步反应:Ⅲ__________________________;
②该小组将A装置中浓硫酸替换成稀硫酸时实验失败,试从反应机理推测可能原因是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
(1)在③~⑦元素中,原子半径最大的是 ,其离子的原子结构示意图为
(2)元素的最高价氧化物对应的水化物中酸性最强的是 ,碱性最强的是 ,呈两性的氢氧化物是 ;
(3)按要求写出下列两种物质的电子式:①的氢化物 ;⑨的最高价氧化物的对应的水化物 ;
(4)在以上元素的单质中,化学性质最不活泼的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体
B. 煎炸食物的花生油和牛油都是可皂化的饱和酯类
C. 福尔马林、水玻璃、氨水均为混合物
D. “青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com