
| A. | 吸水性 | B. | 脱水性 | C. | 强氧化性 | D. | 酸性 |
分析 浓硫酸有很强的吸水性,可以做干燥剂,吸水同时会放热;
浓硫酸能按水的组成比脱去纸、棉布、木条等有机物中的氢、氧元素,也就是平时说的“脱水”;
浓硫酸有很强的氧化性(比稀硫酸强)能和大多数金属(如Cu)或非金属(如C)起氧化还原反应,浓硫酸被还原为二氧化硫.
解答 解:向一个小烧杯中加入20克蔗糖,加3~4滴水,再加入20ml浓硫酸,观察到的实验现象是:烧杯发热、蔗糖变黑、体积膨胀,变成疏松多孔的海棉状的炭,并放出有制激性气味的气体,其中烧杯发发热是因为浓硫酸具有吸水性,溶于水放出大量的热;蔗糖变黑体现浓硫酸的脱水性;体积膨胀,变成疏松多孔的海棉状的炭,并放出有制激性气味的气体,是因为生成的碳被浓硫酸氧化,反应生成二氧化碳和二氧化硫,体现浓硫酸强的氧化性;
所以整个过程体现浓硫酸的:吸水性、脱水性、强氧化性,未体现酸性;
故选:D.
点评 本题考查了浓硫酸的性质,明确浓硫酸的性质是解题关键,注意浓硫酸的吸水性与脱水性的区别,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | K+、AlO2-、Cl-、SO42- | B. | H+、Ba2+、Cl-、NO3- | ||
| C. | Ca2+、Fe2+、NO3-、HCO3- | D. | Na+、Cl-、CO32-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+、K+、NO3-、SO42- | B. | Al3+、Na+、HCO3-、SO42- | ||
| C. | NH4+、Al3+、NO3-、Cl- | D. | Na+、Cu2+、S2-、CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
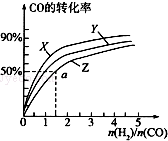 甲醇是重要的燃料,有广阔的应用前景:工业上一般以CO和为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)═CH3OH(g)△H1=-116kJ•mol-1
甲醇是重要的燃料,有广阔的应用前景:工业上一般以CO和为原料合成甲醇,该反应的热化学方程式为:CO(g)+2H2(g)═CH3OH(g)△H1=-116kJ•mol-1查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1稀硫酸中含有硫酸根个数为0.1NA | |
| B. | 标准状况下,0.5NA氟化氢分子所占体积是11.2L | |
| C. | 2.4g金属镁与足量的盐酸反应,生成氢气的体积为2.24L | |
| D. | 12.4g白磷中含有磷原子数为0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加入适量铜粉除去Cu(NO3)2溶液中的AgNO3杂质 | |
| B. | 用NaOH溶液除去CO2中混有的HCl气体 | |
| C. | 稀释浓硫酸时,应将浓硫酸沿器壁慢慢倒入量筒中的水中 | |
| D. | 用乙醇从碘水中萃取碘 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 分子组成相差1个或若干个CH2原子团的物质互称为同系物 | |
| B. | 相对分子质量相同的有机物是同分异构体 | |
| C. | 分子式相同、结构相同的有机物物理性质和化学性质一定相同 | |
| D. | 碳原子之间只以单键相结合的链烃为烷烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
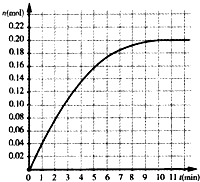 恒温条件下,往容积为2L的密闭容器内加入0.4mol的N2和1.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g),反应中NH3物质的量变化情况如图:下列说法不合理的是( )
恒温条件下,往容积为2L的密闭容器内加入0.4mol的N2和1.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g),反应中NH3物质的量变化情况如图:下列说法不合理的是( )| A. | 其它条件不变,若改用5L容器达到平衡需要的时间将大于10min | |
| B. | N2平衡转化率为25% | |
| C. | 平衡时气体总压强为开始时的90% | |
| D. | 反应前10min反应速率v(H2)=0.01mol?L-1?min-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com