
【题目】下列关于有机物的说法中,正确的一组是
①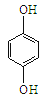 和
和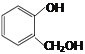 互为同系物
互为同系物
②蛋白质水解和油脂皂化都是高分子生成小分子的过程
③高分子材料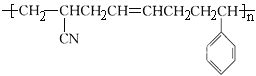 是由三种单体聚合而成的,该高分子材料是体型结构高分子,具有热固性
是由三种单体聚合而成的,该高分子材料是体型结构高分子,具有热固性
④C2H2 和C6H6不论二者以何种比例混合,只要总质量一定,则完全燃烧时消耗O2和生成的H2O的质量不变
⑤塑料、合成橡胶和合成纤维都是合成高分子材料
⑥棉花、蚕丝、人造丝的主要成分都是纤维素
A. ②③④⑤ B. ①③⑤ C. ④⑤ D. ①③④⑤⑥
科目:高中化学 来源: 题型:
【题目】MnO2在电池、玻璃、有机合成等工业生产中应用广泛。利用粗MnO2(含有杂质MnO和MnCO3)制取纯MnO2的流程如下:
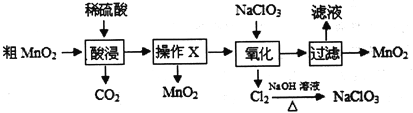
请回答下列问题:
(1)为加快酸浸速率可采取的措施有______________________________________(答两点)。酸浸过程中稀硫酸可否用盐酸代替,回答并说明理由_________________________。
(2)操作X的名称是____________。氧化过程反应的离子方程式是________________。
(3)加热条件下Cl2与NaOH溶液反应,其氧化产物和还原产物的物质的量之比为________。
(4)酸浸过程中得到的溶液所含主要溶质为____________,电解该溶液也可制得MnO2和H2,写出该电解过程中阳极的电极反应式________________________________。
(5)MnO2常用作某些化学反应的催化剂。下图为2H2O2=2H2O+O2↑反应过程中的能量变化示意图,下列说法正确的是__________。
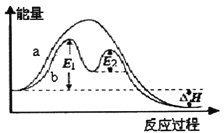
a.该反应为吸热反应,热效应为△H
b.反应历程b有催化剂参加
c.有催化剂时,该反应的活化能为E1+E2
d.改变催化剂,可改变该反应的活化能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物J是治疗心脏病药物的一种中间体,分子结构中含有3个六元环。其中一种合成路线如下:
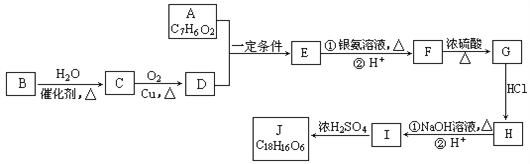
已知:
①A既能发生银镜反应,又能与FeCl3溶液发生显色反应,其核磁共振氢谱显示有4种氢,且峰面积之比为1︰2︰2︰1。
②有机物B是一种重要的石油化工产品,其产量可用来衡量国家的石油化工发展水平。
![]()
回答以下问题:
(1)A中含有的官能团名称是_________________________________。
(2)写出F生成G的化学方程式____________________________________。
(3)写出J的结构简式__________________________________。
(4)E的同分异构体有多种,写出所有符合以下要求的E的同分异构体的结构简式______。
①FeCl3溶液发生显色反应 ②能发生银镜反应
③苯环上只有两个对位取代基 ④能发生水解反应。
(5)参照上述合成路线,设计一条由乙醛(无机试剂任选)为原料合成二乙酸-1,3-丁二醇酯(![]() )的合成路线_____________。
)的合成路线_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S燃料电池应用前景非常广阔,该电池示意图如下。下列说法正确的是( )
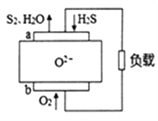
A. 电极a是正极 B. O2-由电极a移向电极b
C. 电极 a 的反应式为:2H2S+2O2--4e-=S2+2H2O D. 当通入1.12LO2,转移电子数0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 标准状况下,2.24 L水含有的分子数为0.1NA
B. 12g14C含有的中子数为8NA
C. 1 L0.1 mol·L-1 FeCl3溶液含阳离子数大于0.1NA
D. 1molN2和3 mol H2充分反应后,生成气体的分子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 常用浸有KMnO4溶液的硅土对水果保鲜 B. 合金的硬度和熔点都高于成分金属
C. 铜是用量最大的合金 D. 工业上常用电解MgCl2溶液制取Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知钡的金属活动性介于钠和钾之间,下列叙述中正确的是( )
A. 钡与水反应不如钠与水反应剧烈 B. 钡可以从NaCl溶液中置换出钠
C. 氧化性:K+>Ba2+>Na+ D. 碱性:KOH>Ba(OH)2>NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C均为短周期元素,A、B同周期,A、C的最低价阴离子分别为A2-、C-,A2-离子半径大于C-,B2+与C-具有相同的电子层结构。下列叙述中一定不正确的是( )
A.它们的原子序数A>B>C B.它们的原子半径C>B>A
C.它们的离子半径A2->C->B2+D.它们的最外层电子数C>A>B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】本题为《化学反应原理(选修4)》选做题。
(1)在一固定容积的密闭容器中进行如下反应:CO2(g)+H2(g)![]() CO(g)+H2O(g),其平衡常数K和温度T的关系如下:
CO(g)+H2O(g),其平衡常数K和温度T的关系如下:
T/℃ | 700 | 800 | 850 | 1 000 | 1 200 |
K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
①K的表达式为____________________;
②该反应的正反应为__________反应(“吸热”或“放热”);
③下列选项中,能判断该反应已经达到化学平衡状态的是____________(填字母代号)。
A.容器中压强不变
B.混合气体中CO浓度不变
C.v正(H2)=v逆(H2O)
D.c(CO2)=c(CO)
(2)下列化合物:①HCl ②NaOH ③CH3COOH ④NH3·H2O ⑤CH3COONa ⑥NH4Cl,溶液呈碱性的有__________(填序号);常温下0.01 mol/L HCl溶液的pH=________;pH=11的CH3COONa溶液中由水电离产生的c(OH-)=________。
(3)已知在Cu2+、Mg2+、Fe2+浓度相同的溶液中,其开始沉淀时的pH如下:
离子 | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
①若向该溶液中滴加NaOH溶液,则先沉淀的是 ____________(填离子符号);
②判断Ksp[Fe(OH)2] ____________Ksp[Mg(OH)2](填“>”、“=”或“<”)。
(4)电解装置如图所示:
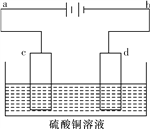
①当用惰性电极电解时,d电极的反应式为____________________;
②若用此装置进行铁上镀铜,已知镀层金属采用纯铜且电镀前两电极材料质量相等,电镀一段时间后对电极进行称量发现两极质量差为16 g,则电路中转移的电子为____________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com