

���� ��1����ͼ��֪���ﵽƽ��ʱ��������0.10mol/L�����ݷ�Ӧ���ʸ�����㷴Ӧ���ʣ�
��2����N2��g��+3H2��g��?2NH3��g����֪�����ɰ���0.2molʱ�μӷ�Ӧ�ĵ���Ϊ0.1mol���Դ˼���ת���ʣ�
��3������H��0���÷�ӦΪ���ȷ�Ӧ�������¶������ƶ�����Ũ�ȼ�С�������¶ȣ������ƶ���Ũ��������Ӧ�ﲻ����ȫ��Ӧ��
��4�����淴Ӧ����ƽ��ʱ��ͬ�����ʵ�����������ȣ�����ֵ�Ũ�ȡ��������ֲ��䣬�ɴ�����������һЩ�����䣬�ж�ƽ���������Ӧ�淴Ӧ���з����仯�����������ɱ仯�����ٱ仯˵������ƽ�⣻
��5�������������Сһ�룬ѹǿ����ƽ�������������С�ķ����ƶ���
��6����5����ĩ�������������Сһ���˲�䰱����Ũ�ȱ�Ϊԭƽ���2����ѹǿ����ƽ�������ƶ���������Ũ�������ڵ�8����ĩ�ﵽ�µ�ƽ��ʱNH3��Ũ��ԼΪ0.25mol•L-1��
��� �⣺��1����ͼ��֪���ﵽƽ��ʱ��������0.10mol/L���䷴Ӧ����Ϊ$\frac{0.1mol/L}{4min}$=0.025 mol•L-1•min-1��
�ʴ�Ϊ��0.025 mol•L-1•min-1��
��2����N2��g��+3H2��g��?2NH3��g����֪�����ɰ���0.2molʱ�μӷ�Ӧ�ĵ���Ϊ0.1mol�����Ե�����ת����Ϊ=$\frac{0.1mol}{0.2mol}$��100%=50%��
�ʴ�Ϊ��50%��
��3������H��0���÷�ӦΪ���ȷ�Ӧ�������¶������ƶ�����Ũ�ȼ�С�������¶ȣ������ƶ���Ũ��������Ӧ�ﲻ����ȫ��Ӧ��
����0��c��NH3����0.2mol/L����NH3�����ʵ���Ũ�Ȳ�����Ϊ0.2mol/L��
�ʴ�Ϊ��a��
��4��a��N2��NH3Ũ�ȹ�ϵ�뵪����ת�����йأ�ƽ��ʱ��һ����ȣ���a����
b��NH3�ٷֺ������ֲ��䣬˵����Ӧ����ƽ�⣬��b��ȷ��
c���淴Ӧ���У�����������ʵ�����С�����º���������ѹǿ��С�������������ѹǿ���䣬˵����Ӧ����ƽ�⣬��c��ȷ��
d��NH3��H2����������֮��Ϊ2��3����˵�����淴Ӧ������ȣ��ﵽƽ��״̬����d��ȷ��
e������������������䣬�����ݻ����䣬�����л��������ܶ�ʼ�ձ��ֲ��䣬��e����
��ѡ��bcd��
��5����Ӧ�ﵽƽ���5����ĩ�����������������䣬��ֻ�������������Сһ��ѹǿ����ƽ�������������϶�Եķ�����У�ƽ��������У�
�ʴ�Ϊ��������Ӧ����
��6����5����ĩ�������������Сһ���˲�䰱��Ũ��Ϊ0.40mol/L��ѹǿ����ƽ�������ƶ���������Ũ�������ڵ�8����ĩ�ﵽ�µ�ƽ��ʱNH3��Ũ��ԼΪ0.50mol•L-1����5����ĩ��ƽ��ʱNH3Ũ�ȵı仯����ͼ��Ϊ��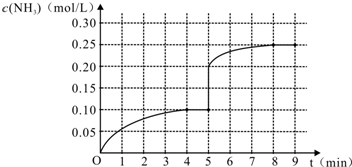 ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼�黯ѧƽ��ļ�����Ӱ�����ء���ѧƽ��ͼ��ƽ��ƽ��״̬�жϡ���ѧƽ��Ľ����ȣ�Ϊ�߿��������ͣ�������ѧ���ķ��������������Ŀ��飬��Ŀ�Ѷ��еȣ���6������ͼע����С���˲�䣬����Ũ�ȱ�Ϊԭ����2����


 ��һ����ͬ���ɽ�����ϵ�д�
��һ����ͬ���ɽ�����ϵ�д� ������Ӧ���ϵ�д�
������Ӧ���ϵ�д� ��ʦ�㾦�ִʾ��ƪϵ�д�
��ʦ�㾦�ִʾ��ƪϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��ѧ��Ӧ | ƽ�� ���� | �¶�/�� | |
| 500 | 800 | ||
| ��2H2��g��+CO��g��?CH3OH��g�� | K1 | 2.5 | 0.15 |
| ��H2��g��+CO2��g��?H2O��g��+CO��g�� | K2 | 1.0 | 2.50 |
| ��3H2��g��+CO2��g��?CH3OH��g��+H2O��g�� | K3 | ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ڿ�����ȼ������������ | |
| B�� | ����Ͷ�������ɫʯ����Һ��ˮ�У�ˮ��Һ��Ϊ��ɫ | |
| C�� | ��һС���Ʒ���CuSO4��Һ�з�����Ӧ���ӷ���ʽ��2Na+Cu2+�T2Na++Cu | |
| D�� | ��4.6gNaͶ�뵽95.4gˮ�У�������Һ�����ʵ�������������8.0% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | Cu��OH��2 | Fe��OH��3 | CuCl | CuI |
| Ksp | 2.2��10-20 | 2.6��10-39 | 1.7��10-7 | 1.3��10-12 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Һ��ɫ���ֲ��䣬˵���������淴Ӧ�ﵽƽ��״̬ | |
| B�� | �����̷���FeSO4•7H2O������ԭ��������1L��ˮ��������Ҫ917.4 g | |
| C�� | ������ת����Ӧ��ƽ�ⳣ��K=l��1014����ת����������Һ��pH=6 | |
| D�� | ������Ksp[Cr��OH��3]=1��10-32��Ҫʹ�������ˮ�е�c��Cr3+ ������1��10-5mol/L��Ӧ����Һ��pH=5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʱ��/min SO2����/10-3g �¶�/�� | 0 | 20 | 40 | 60 | 80 | 100 | 120 |
| T1 | 2100 | 1052 | 540 | 199 | 8.7 | 0.06 | 0.06 |
| T2 | 2100 | 869 | 242 | x | x | x | x |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
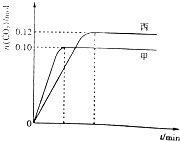 һ���¶��£��������ݻ���Ϊ2.0L�ĺ����ܱ������з�����Ӧ��
һ���¶��£��������ݻ���Ϊ2.0L�ĺ����ܱ������з�����Ӧ��| ���� | �¶�/�� | ��ʼ���ʵ���/mol | |
| NO��g�� | CO��g�� | ||
| �� | T1 | 0.20 | 0.20 |
| �� | T1 | 0.30 | 0.30 |
| �� | T2 | 0.20 | 0.20 |
| A�� | �÷�Ӧ������ӦΪ���ȷ�Ӧ | |
| B�� | �ﵽƽ��ʱ������CO2����������ȼ��е�С | |
| C�� | T1��ʱ������ʼʱ����г���0.40molNO��0.40molCO��0.40molN2��0.40molCO2����Ӧ�ﵽ��ƽ��ǰv��������v���棩 | |
| D�� | T2��ʱ������ʼʱ����г���0.06molN2��0.12molCO2�����ƽ��ʱN2��ת���ʴ���40% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʯ��ˮ | B�� | ����������Һ | C�� | �Ȼ�����Һ | D�� | ����̼������Һ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com