
【题目】(1)现有34 g某气体,它们的摩尔质量为17 g·mol-1。则:
①该气体的物质的量为______mol。
②该气体所含分子数为______NA。
③该气体在标准状况下的体积为______L。
④该气体完全溶解于500 mL水后稀释到2 L,物质的量浓度为______mol·L-1。
(2)______g H2O中的氧原子数目与标准状况下22.4 L CO2 中的氧原子数目相同。
(3)摩尔质量是指单位物质的量的物质所具有的质量。
①已知NH3的相对分子质量为17,则NH3的摩尔质量为_____。
②NA 为阿伏加德罗常数,已知a g 某气体中含分子数为b,则该气体的摩尔质量为_____。
③已知一个铁原子的质量为b g,则铁原子摩尔质量为_____。
【答案】2 2 44.8 1 36 17g/mol ![]() bNA
bNA
【解析】
根据 n=![]() 进行计算,摩尔质量与相对分子质量在数值上相等,表示1mol物质所具有的质量,然后分析。
进行计算,摩尔质量与相对分子质量在数值上相等,表示1mol物质所具有的质量,然后分析。
(1)现有34 g某气体,它们的摩尔质量为17 g·mol-1。则:
①该气体的物质的量为![]() ;
;
②该气体所含分子数为N=nNA=2mol×NAmol-1= 2NA;
③该气体在标准状况下的体积为V=nVm=2×22.4L/mol=44.8L;
④该气体完全溶解于500 mL水后稀释到2 L,物质的量浓度为![]()
(2)标准状况下22.4 L CO2 中分子的数目1mol,一个二氧化碳分子中含有两个氧原子,氧原子数目为2NA,氧原子的物质的量为2mol,一个H2O中含有一个氧原子, 要保证氧原子的物质的量相等,需要2mol水,![]() ;
;
(3)①相对分子质量与摩尔质量在数值上相等,NH3的相对分子质量为17,则NH3的摩尔质量为17g/mol;
②NA 为阿伏加德罗常数,已知a g 某气体中含分子数为b,根据公式![]() ,则该气体的摩尔质量
,则该气体的摩尔质量![]() ;
;
③已知一个铁原子的质量为b g,则铁原子摩尔质量为1mol铁原子具有的质量,为bNA。


科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示,电池总反应为 2Ag + Cl2 = 2AgCl。已知阳离子交换膜只允许阳离子通过,阴离子不能通过,离子交换过程中溶液电荷守恒。下列说法正确的是
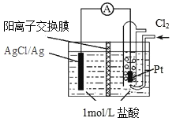
A.正极反应式为 AgCl + e—= Ag + Cl—
B.放电时,交换膜右侧溶液中有大量白色沉淀生成
C.若用 NaCl 溶液代替盐酸,则电池总反应随之改变
D.当外电路中转移 0.1mol e—时,阳离子交换膜左侧溶液中约减少0.2mol 离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数,下列说法正确的是( )
A.6.2g白磷分子(P4)中含P-P键数为0.05NA
B.1mol CH3+含电子数为8NA
C.标准状况下,22.4LSO3中含原子数为4NA
D.常温常压下,11.2LCO2气体通过足量Na2O2充分反应,转移电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】液态化合物AB会发生微弱的自身电离,电离方程式为AB![]() A++B-,在不同温度下其平衡常数为K(25 ℃)=1.0×10-14,K(35 ℃)=2.1×10-14。则下列叙述正确的是 ( )。
A++B-,在不同温度下其平衡常数为K(25 ℃)=1.0×10-14,K(35 ℃)=2.1×10-14。则下列叙述正确的是 ( )。
A.c(A+)随温度升高而降低
B.在35 ℃时,c(A+)>c(B-)
C.AB的电离程度(25 ℃)>(35 ℃)
D.AB的电离是吸热过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室欲配制0.5 mol·L-1的NaOH溶液500 mL,有以下仪器:
①烧杯②药匙③1000 mL容量瓶④500 mL容量瓶⑤玻璃棒⑥托盘天平(带砝码)。
(1)配制时,必须使用的仪器有_____(填代号),还缺少的仪器是_____,该实验中两次用到玻璃棒,其作用分别是_____,_____。
(2)使用容量瓶前必须进行的一步操作是_____。
(3)配制时,一般可分为以下几个步骤:①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤⑦定容 ⑧装瓶,其正确的操作顺序是________。
(4)配制一定物质的量浓度的溶液,造成浓度偏高的操作是_____
A.定容时,滴加蒸馏水超过刻度线 B.定容时,眼睛俯视刻度线
C.洗涤烧杯和玻璃棒的溶液未转入容量瓶中 D.定容时,眼睛仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电-Fenton法是用于水体中有机污染物降解的高级氧化技术,其反应原理如图所示。其中电解产生的H2O2与Fe2+发生Fenton反应生成的羟基自由基(·OH) 能氧化降解有机污染物。下列说法正确的是

A. 电源的X极为正极
B. 与电源Y相连电极的电极反应式为H2O+e-=H++·OH
C. Fenton反应: H2O2+Fe2+=Fe(OH)2++·OH
D. 每消耗22.4L O2 (标准状况),整个电解池中理论上可产生2mol·OH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图所示的转化关系以及现象回答下列问题。
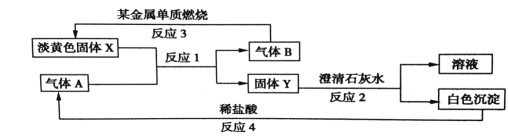
(1)固体 X的化学式是:________________
(2)写出反应1 的化学方程式:____________________________
(3)写出反应2 的离子方程式:________________________________
(4)若15.6gX 和足量的气体 A反应,转移__________mol 电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D四种短周期元素,A分别与B、C、D结合生成甲、乙、丙三种化合物,且甲、乙、丙三分子中含有的质子数都为10,C、D结合生成化合物丁。有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如下图所示:
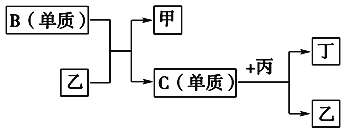
(1)写出B+乙―→甲+C的化学反应方程式______________________________________。
(2)根据以上条件可以确定A、B、C、D四种元素中的三种,不能被确定的第四种元素是________(填写序号)。
①A ②B ③C ④D
(3)依据下列条件可以进一步确定上述第四种元素:
①甲与丙以及乙与丙均能够发生反应,②甲、丙都是无色、有刺激性气味的物质。
据此,请回答下列问题:
写出上述第四种元素在周期表中的位置________________。写出C+丙―→乙+丁的化学反应方程式_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
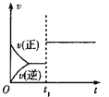
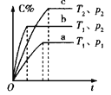
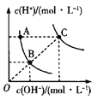
【题目】下列对图像的叙述正确的是
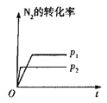
甲 乙 丙 丁
A.图甲可表示压强对反应:![]()
![]() 的影响
的影响
B.图乙中,![]() 时刻改变的条件一定是加入了催化剂
时刻改变的条件一定是加入了催化剂
C.若图丙表示反应:![]() ,则
,则![]() 、
、![]()
D.图丁表示水中![]() 和
和![]() 的关系,ABC所在区域总有
的关系,ABC所在区域总有![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com