
 ���ⶨijNaOH��Һ�����ʵ���Ũ�ȣ�����0.1000mol•L-1��HCl����Һ�����к͵ζ����ü�����ָʾ������
���ⶨijNaOH��Һ�����ʵ���Ũ�ȣ�����0.1000mol•L-1��HCl����Һ�����к͵ζ����ü�����ָʾ������| ʵ����� | ����NaOH��Һ�����/mL | 0.1000mol•L-1HCl��Һ�����/mL | |
| �ζ�ǰ�̶� | �ζ���̶� | ||
| 1 | 25.00 | 0.00 | 26.29 |
| 2 | 25.00 | 1.00 | 31.00 |
| 3 | 25.00 | 1.00 | 27.31 |
���� ��1���ζ�������Һ�ڵζ����У�����Һʢ����ƿ�У�
��2��������Һ�������ʽ�ζ����У�
��3�����ݵζ��յ�ʱ��Һ��ɫ�ɻ�ɫͻ��Ϊ��ɫ���ұ��ְ���Ӳ���ɫ��
��4�����ݵζ��ܵĽṹ�뾫ȷ��Ϊ0.01mL��
��5���ȸ������ݵ���Ч�ԣ���ȥ��2�����ݣ�Ȼ�����1��3��ƽ������V�����ᣩ�����Ÿ��������NaOH��Ӧ���C��NaOH����
��6������c�����⣩=$\frac{c��������V������}{V�����⣩}$��������������V��������Ӱ�죬�Դ��жϣ�
��� �⣺��1������ʽ�ζ���ȡ�������NaOH��Һ����ƿ�У�
�ʴ�Ϊ����ƿ��
��2��ʢװ���������������Ϊ��ʽ�ζ��ܣ�
�ʴ�Ϊ����ʽ�ζ��ܣ�
��3������Һ���������ƣ���ƿ��ʢ�е�����������Һ�е�����ȣ���Һ����ɫ�ǻ�ɫ��������Һ��pH��С�����ε���Һ��pHС��4.4ʱ����Һ��ɫ�ɻ�ɫ��ɳ�ɫ���Ұ���Ӳ���ɫ���ε�������
�ʴ�Ϊ����Һ�ɻ�ɫ��Ϊ��ɫ�Ұ�����ڲ���ɫ��
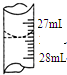
��4����ѧ����ʵ������У���¼�ζ�ǰ�ζ�����Һ�����Ϊ0.50mL���ζ���Һ����ͼΪ27.40ml���ζ����е�Һ�����Ϊ27.40ml-0.50mL=26.90mL��
�ʴ�Ϊ��26.90mL��
��5���������ݵ���Ч�ԣ���ȥ��2�����ݣ���1��3��ƽ������V�����ᣩ=$\frac{26.29mL+26.31mL}{2}$=26.30mL��
HCl+NaOH�TNaCl+H2O
0.0263L��0.1000mol•L-1 0.025L��C��NaOH��
��C��NaOH��=$\frac{0.0263L��0.1000mol•{L}^{-1}}{0.025L}$=0.1052mol/L��
�ʴ�Ϊ��0.1052mol/L��
��6��A����ƿ������ˮϴ�������ô���Һ��ϴ����ʹ��ƿ�����ʵ����ʵ����������V������ƫ����c�����⣩=$\frac{c��������V������}{V�����⣩}$���������c�����⣩ƫ�ߣ���A��ȷ��
B����ʽ�ζ���������ˮϴ�������ñ�Һ��ϴ����V��������Ӱ�죬����c�����⣩=$\frac{c��������V������}{V�����⣩}$���������c�����⣩���䣬��B����
C���ζ�ǰ��ʽ�ζ��ܼ������δ�ų����ζ���������ʧ�������V������ƫ����c�����⣩=$\frac{c��������V������}{V�����⣩}$���������c�����⣩ƫ�ߣ���C��ȷ��
D���ζ�ǰ������ȷ���ζ����ӵζ��ܶ����������V������ƫС������c�����⣩=$\frac{c��������V������}{V�����⣩}$���������c�����⣩ƫ�ͣ���D����
��ѡAC��
���� ���⿼��������к͵ζ�ʵ��IJ������衢�ζ��ܵĽṹ���յ��ж��Լ�����Ӧ�ã��յ��жϣ���Ŀ�Ѷ��еȣ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
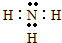
 �����к��еĻ�ѧ���й��ۼ������Ӽ����������� ����
�����к��еĻ�ѧ���й��ۼ������Ӽ����������� �����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | a��b | B�� | a��b | C�� | a=b | D�� | ��ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 26�� | B�� | 27�� | C�� | 28�� | D�� | 29�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
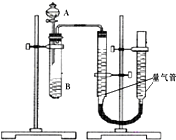 �ס�������С����������KMnO4��H2C2O4��Һ��Ӧ�����ʵ��̽��Ӱ�췴Ӧ���ʵ����أ�2MnO4-+5H2C2O4+6H+=2Mn2++10CO2+8H2O��
�ס�������С����������KMnO4��H2C2O4��Һ��Ӧ�����ʵ��̽��Ӱ�췴Ӧ���ʵ����أ�2MnO4-+5H2C2O4+6H+=2Mn2++10CO2+8H2O��| ��� | A��Һ | B��Һ |
| �� | 2ml 0.2mol/LH2C2O4��Һ | 4ml 0.01mol/LKMnO4��Һ |
| �� | 2ml 0.1mol/LH2C2O4��Һ | 4ml 0.01mol/LKMnO4��Һ |
| �� | 2ml 0.2mol/LH2C2O4��Һ | 4ml 0.01mol/LKMnO4��Һ������MnSO4 |
| ʵ���� | 1 | 2 | 3 | 4 |
| ˮ/ml | 10 | 5 | 0 | X |
| 0.5mol/L H2C2O4/ml | 5 | 10 | 10 | 5 |
| 0.2mol/L KMnO4/ml | 5 | 5 | 10 | 10 |
| ʱ��/s | 40 | 20 | 10 | --- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ijѧ��������֪���ʵ���Ũ�ȵ��������ⶨδ֪���ʵ���Ũ�ȵ�NaOH��Һʱ��ѡ���̪��ָʾ��������д���пհף�
ijѧ��������֪���ʵ���Ũ�ȵ��������ⶨδ֪���ʵ���Ũ�ȵ�NaOH��Һʱ��ѡ���̪��ָʾ��������д���пհף�| �ζ� ���� | ����NaOH��Һ�����/mL | 0.100 0mol/L��������/mL | ||
| �ζ�ǰ�̶� | �ζ���̶� | ��Һ���/mL | ||
| ��һ�� | 25.00 | 0.00 | 26.11 | 26.11 |
| �ڶ��� | 25.00 | 1.56 | 30.30 | 28.74 |
| ������ | 25.00 | 0.22 | 26.31 | 26.09 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | O2��O3 | B�� | 2H2��3H2 | ||
| C�� | H2O��H2O2 | D�� | C2H5COOH��CH3COOCH3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
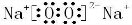 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 һ�������������Ժ�CO2������Ӧ��Fe��s��+CO2��g��?FeO��s��+CO��g����H��0��1 100��ʱ����ij�ܱ������м����������۲�����һ������CO2���壬��Ӧ������CO2��CO��Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ��
һ�������������Ժ�CO2������Ӧ��Fe��s��+CO2��g��?FeO��s��+CO��g����H��0��1 100��ʱ����ij�ܱ������м����������۲�����һ������CO2���壬��Ӧ������CO2��CO��Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ��| ���� | �� | �� |
| ��Ӧ��Ͷ���� | 3mol Fe��2mol CO2 | 4mol FeO��3mol CO |
| CO��Ũ�ȣ�mol•L-1�� | c1 | c2 |
| CO2��������� | ��1 | ��2 |
| ��ϵѹǿ��Pa�� | p1 | p2 |
| ��̬��Ӧ���ת���� | ��1 | ��2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com