
| A. | 等物质的量的水与重水含有的中子数 | |
| B. | 等质量的乙烯和丙烯中含有的共用电子对数 | |
| C. | 同温同压同体积的CO和NO含有的质子数 | |
| D. | 等物质的量的镁和铝分别于足量氯气完全反应时转移的电子数 |
分析 A.1个水分子中含有8个中子,1个重水分子中含有10个中子;
B.乙烯和丙烯的最简式均为CH2,由n=$\frac{m}{M}$可知,等质量时含CH2的个数相同;
C.同温同压同体积的任何气体具有相同分子数,CO含有14 个质子,NO含有15个质子;
D.镁、铝与氯气反应生成氯化镁和氯化铝,镁离子为二价金属,铝离子为三价.
解答 解:A.1个水分子中含有8个中子,1个重水分子中含有10个中子,所以等物质的量的水与重水含有的中子数不相等,故A 错误;
B.乙烯和丙烯的最简式均为CH2,由n=$\frac{m}{M}$可知,等质量时含CH2的个数相同,1个C2H4分子共用6对电子(其中4个C-H,2个C-C),1个C3H6分子共用9对电子(其中6个C-H,3个C-C),因此可以发现规律:1个CH2平均共用3对电子,含CH2的个数相同则共有电子对数相同,故B正确;
C.同温同压同体积的CO和NO含有相同的分子数,CO和NO含有质子数不相同,故C错误;
D.等物质的量的镁和铝分别于足量氯气完全反应时转移的电子数之比为:2:3,故D错误;
故选:B.
点评 本题考查了物质的量有关计算,明确有关物质的量计算公式及基本概念是解题关键,题目难度不大.


 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案 全优冲刺100分系列答案
全优冲刺100分系列答案科目:高中化学 来源: 题型:实验题
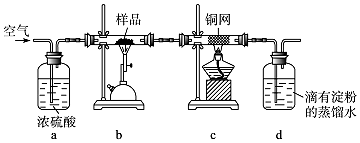
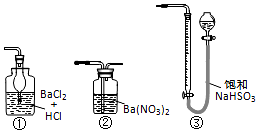
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑥ | B. | ①②⑤⑥ | C. | ③⑤⑥④ | D. | ①③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3、BaCl2、HCl | B. | BaCl2、Na2CO3、H2SO4 | ||
| C. | BaCl2、Na2CO3、HCl | D. | Ba(NO3)2、Na2CO3、HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②③④ | C. | ②③⑤ | D. | ②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 变化 | △H | △S | 方向性 |
| H2O(l)→H2O(g) | |||
| CaO(s)+SO2(g)═CaSO3(s) | |||
| 2Fe3+(aq)+Cu(s)═2Fe2+(aq)+Cu2+(aq) | |||
| NH4Cl(s)═HCl(g)+NH3(g) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com