
Ⅰ.氢能的存储是氢能应用的主要瓶颈,配位氢化物、富氢载体化合物是目前所采用的主要储氢材料。
(1)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。在基态Ti2+中,电子占据的最高能层符号为________,该能层具有的原子轨道数为________。
(2)液氨是富氢物质,是氢能的理想载体,利用N2+3H22NH3实现储氢和输氢。下列说法正确的是________。
a.NH3分子中氮原子的轨道杂化方式为sp2杂化
b.NH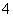 与PH
与PH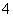 、CH4
、CH4 、BH
、BH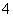 、ClO
、ClO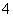 互为等电子体
互为等电子体
c.相同压强下,NH3沸点比PH3的沸点 高
高
d.[Cu(NH3)4]2+中,N原子是配位原子
(3)已知NF3与NH3的空间构型相同,但NF3不易与Cu2+形成配离子,其原因是________________________________________。
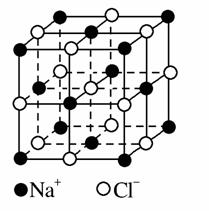
Ⅱ.氯化钠是生活中的常用调味品,也是结构化学中研究离子晶体时常用的代 表物,其晶胞结构如图所示。
表物,其晶胞结构如图所示。
(1)设氯化钠晶体中Na+与跟它最近邻的Cl-之间的距离为r,则与Na+次近邻的Cl-个数为________,该Na+与跟它次近邻的Cl-之间的距离为________。
(2)已知在氯化钠晶体中Na+的半径为a pm,Cl-的半径为b pm,它们在晶体中是紧密接触的,则在氯化钠晶体中离子的空间利用率为________。(用含a、b的式子
表示)
(3)纳米材料的表面原子占总原子数的比例很大,这是它有许多特殊性质的原因。假设某氯化钠颗粒形状为立方体,边长为氯化钠晶胞的10倍,则该氯化钠颗粒中表面原子占总原子数的百分比为___ _。
解析 Ⅰ.(1)基态Ti2+的核外电子排布式为1s22s22p63s23p63d2,电子占据的最高能层为M层,该能层有s、p、d三个能级,具有1+3+5=9个原子轨道。(2)NH3分子中氮原子的轨道杂化方式为sp3杂化,a项错误。NH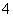 中共有8个价电子,但ClO
中共有8个价电子,但ClO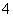 中价电子共有32个,因价电子总数不相等,因此它与NH
中价电子共有32个,因价电子总数不相等,因此它与NH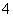 不
不 互为等电子体,故b项错误。NH3能形成分子间氢键,使其沸点高于PH3,c项正确。[Cu(NH3)4]2+中,Cu原子核外有空轨道,而N原子核外有孤对电子,故N原子是配位原子,d项正确。
互为等电子体,故b项错误。NH3能形成分子间氢键,使其沸点高于PH3,c项正确。[Cu(NH3)4]2+中,Cu原子核外有空轨道,而N原子核外有孤对电子,故N原子是配位原子,d项正确。
Ⅱ. (1)根据氯化钠晶胞结构可知与Na+次近邻的Cl-共有8个。
(1)根据氯化钠晶胞结构可知与Na+次近邻的Cl-共有8个。 晶胞面对角线的长度为
晶胞面对角线的长度为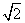 r,所求距离为
r,所求距离为 晶胞体对角线的长度,为
晶胞体对角线的长度,为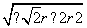 =
=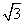 r。(2)晶胞边长=2(a+b)pm,晶胞体积V=[2(a+b)]3pm3;1个晶胞中有4个NaCl,则离子体积V′=[4×
r。(2)晶胞边长=2(a+b)pm,晶胞体积V=[2(a+b)]3pm3;1个晶胞中有4个NaCl,则离子体积V′=[4×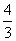 πa3+4×
πa3+4×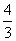 πb3]pm3,所以离子的空间利用率为
πb3]pm3,所以离子的空间利用率为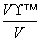 ×100%=
×100%=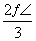 ×
×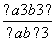 ×100%。(3)若立方体氯化钠颗粒边长为氯化钠晶胞的10倍,则立方体氯化钠颗粒的棱上有21个原子(10个Cl-和11个Na+),那么该立方体的原子总数为213=9 261。而该立方体的每条棱的相应里面一层(紧靠)的棱上有19个原子(10个Cl-和9个Na+),即该立方体中有193=6 859个原子处于立方体内部,所以该立方体表面原子个数为:213-193=2 402,因而表面原子占总原子数的百分比为
×100%。(3)若立方体氯化钠颗粒边长为氯化钠晶胞的10倍,则立方体氯化钠颗粒的棱上有21个原子(10个Cl-和11个Na+),那么该立方体的原子总数为213=9 261。而该立方体的每条棱的相应里面一层(紧靠)的棱上有19个原子(10个Cl-和9个Na+),即该立方体中有193=6 859个原子处于立方体内部,所以该立方体表面原子个数为:213-193=2 402,因而表面原子占总原子数的百分比为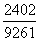 ×100%≈26%。
×100%≈26%。
答案 Ⅰ.(1)M 9 (2)cd (3)N、F、H三种元素的电负性为F>N>H,在NF3中,共用电子对偏向氟原子,偏离氮原子,使得氮原子上的孤电子对难以与Cu2+形成配位键
Ⅱ.(1)8 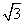 r (2)
r (2)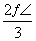 ×
×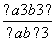 ×100%
×100%
(3)26%或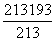 ×100%
×100%


科目:高中化学 来源: 题型:
已知氧化性:Br2>Fe3+>I2;还原性:I->Fe2+>Br-,则下列反应能发生的是( )
A.I2+2Fe2+===2Fe3++2I- B.2Br-+I2===Br2+2I-
C.2Fe3++2I-===2Fe2++I2 D.2Fe3++2Br-===2Fe2++Br2
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:H2(g)+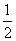 O2(g)===H2O(g) ΔH=-242 kJ/mol,断开1 mol O===O键和1 mol H—O键所吸收的能量分别为496 kJ和463 kJ,则断开1 mol H—H键所吸收的能量为( )
O2(g)===H2O(g) ΔH=-242 kJ/mol,断开1 mol O===O键和1 mol H—O键所吸收的能量分别为496 kJ和463 kJ,则断开1 mol H—H键所吸收的能量为( )
A.920 kJ B.557 kJ
C.436 kJ D.188 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
关于如图所示各装置的叙述中,正确的是( )
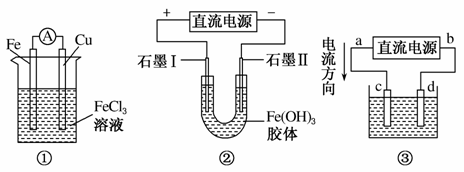
A.装置①是原电池,总反应是Cu+2Fe3+===Cu2++2Fe2+
B.装置①中,铁作负极,负极反应式为Fe3++e-===Fe2+
C.装置②通电一段时间后石墨Ⅱ电极附近溶液红褐色加深
D.若用装置③精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
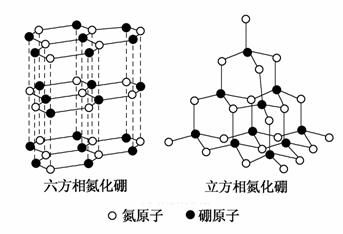
氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如下图所示。
(1)基态硼原子的电子排布式为________。
(2)关于这两种晶体的说法,正确的是________(填选项字母)。
a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B—N键均为共价键
d.两种晶体均为分子晶体
(3)六方相氮化硼晶体层内一个硼原子与相邻氮原子构成的空间构型为________,其结构与石墨相似却不导电,原因是_________________。
(4)立方相氮化硼晶体中,硼原子的杂化轨道类型为__________。该晶体的天然矿物在青藏高原地下约300 km的古地壳中被发现。根据这一矿物形成事实,推断实验室由六方相氮化硼合成立方相氮化硼需要的条件应是______________________________________________________________。
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一。1 mol NH4BF4含有________mol配位键。
查看答案和解析>>
科目:高中化学 来源: 题型:
废旧硬质合金刀具中含碳化钨(WC)、金属钴(Co)及 少量杂质铁,利用电解法可回收WC和Co。工艺流程简图如下:
少量杂质铁,利用电解法可回收WC和Co。工艺流程简图如下:
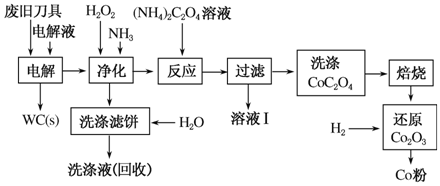
(1)电解时废旧刀具作阳极,不锈钢作阴极,HCl溶液为电解液。阴极主要的电极反应式为________。
(2)净化步骤所得滤饼的主要成分是________。回收的洗涤液代替水配制电解液,目的是回收利用其中的________。
(3)溶液Ⅰ的主要成分是________。洗涤CoC2O4不充分对最终产品纯度并无明显影响,但焙烧时会造成环境污染,原因是______________。
(4)将Co2O3还原成Co粉的化学反应方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验现象及相关的离子方程式均正确的是( )
A.碳酸钙粉末中加入醋酸溶液,固体逐渐减少,生成无色气体:CaCO3+2H+===Ca2++CO2↑+H2O
B.向BaCl2溶液中通入SO2气体,出现白色沉淀:Ba2++SO2+H2O===BaSO3↓+2H+
C.向H2O2溶液中滴加酸化的KMnO4溶液,KMnO4溶液褪色:2MnO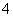 +7H2O2+6H+===2Mn2++6O2↑+10H2O
+7H2O2+6H+===2Mn2++6O2↑+10H2O
D.将等物质的量浓度、等体积的Ba(OH)2溶液和NaHSO4溶液混合,生成白色沉淀:Ba2++SO +H++OH-===BaSO4↓+H2O
+H++OH-===BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列区分植物油和矿物油的方法中,正确的是( )
A.点燃,能燃烧的为矿物油
B.加入水中,浮在水面上的为植物油
C.加入足量的NaOH溶液共煮,不再分层的为植物油
D.尝一尝,能食用的为植物油
查看答案和解析>>
科目:高中化学 来源: 题型:
提纯含有少量硝酸钡杂质的硝酸钾溶液,可以使用的方法为 ( )
A.加入过量碳酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
B.加入过量硫酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
C.加入过量硫酸钠溶液,过滤,除去沉淀,溶液中补加适量硝酸
D.加入过量碳酸钾溶液,过滤,除去沉淀,溶液中补加适量硝酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com