
下列关于外界条件的改变对化学反应速率影响的说法中正确的是( )
|
| A. | 升高温度能加快吸热反应速率,减慢放热反应速率 |
|
| B. | 增大压强能加快气体体积缩小方向的反应速率,减慢气体体积增大方向的反应速率 |
|
| C. | 压强的改变只有通过浓度的改变才能影响化学反应速率 |
|
| D. | 若外界条件的改变引起了正、逆反应速率的改变,就一定能引起化学平衡的移动 |
考点:
化学反应速率的影响因素.
分析:
反应速率是指单位时间内反应物浓度的减少或生成物浓度的增加,影响化学反应速率的因素有内因和外因,内因为物质的本身性质,为主要因素,外因有温度、浓度、压强、催化剂以及光照等,为次要因素.
解答:
解:A.无论是吸热反应还是放热反应,升高温度,反应速率都增大,故A错误;
B.增大压强,正逆反应速率都增大,故B错误;
C.改变压强,如气体的浓度改变,则化学反应速率改变,如通入惰性气体而导致压强改变,但参加反应的气体的浓度不变,则反应速率不变,故C正确;
D.如正逆反应速率相等,则平衡不移动,故D错误.
故选C.
点评:
本题考查影响化学反应速率的因素,为高频考点,侧重于学生的分析能力和基本概念、基本理论知识的综合理解和运用的考查,难度不大,注意相关基础知识的积累.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列说法中,正确的是( )
|
| A. | 合金的熔点一般比组成合金的各成分金属高 |
|
| B. | 我国规定商家不得无偿提供塑料袋,目的是降低成本 |
|
| C. | 红宝石、蓝宝石和金刚石都是由碳元素组成的宝石 |
|
| D. | 氮化硅、光导纤维、氧化铝陶瓷等属于新型无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物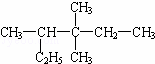 的正确命名是( )
的正确命名是( )
|
| A. | 3,3﹣二甲基﹣4﹣乙基戊烷 | B. | 3,3,4﹣三甲基己烷 |
|
| C. | 3,4,4﹣三甲基己烷 | D. | 2,3,3﹣三甲基己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛.请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其理由是
(用必要的化学用语和相关文字说明).
(2)相同条件下,0.1mol•L﹣1 NH4Al(SO4)2中c(NH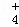 ) (填“等于”“大于”或“小于”)0.1mol•L﹣1 NH4HSO4中c(NH
) (填“等于”“大于”或“小于”)0.1mol•L﹣1 NH4HSO4中c(NH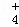 ).
).
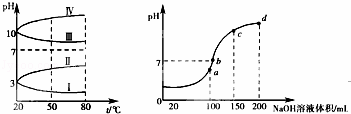
(3)如图1所示是0.1mol•L﹣1电解质溶液的pH随温度变化的图象.
①其中符合0.1mol•L﹣1 NH4Al(SO4)2的pH随温度变化的曲线是 (填写序号),导致pH随温度变化的原因是 ;
②20℃时,0.1mol•L﹣1 NH4Al(SO4)2中2c(SO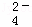 )﹣c(NH
)﹣c(NH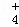 )﹣3c(Al3+)= (填数值).
)﹣3c(Al3+)= (填数值).
(4)室温时,向100mL 0.1mol•L﹣1 NH4HSO4溶液中滴加0.1mol•L﹣1 NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图2所示:试分析图中a、b、c、d四个点,水的电离程度最大是 点;在b点,溶液中各离子浓度由大到小的排列顺序是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法或表示方法正确的是( )
|
| A. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
|
| B. | 由C(石墨)→C(金刚石);△H=+1.9 kJ/mol可知,金刚石比石墨稳定 |
|
| C. | 在稀溶液中:H+(aq)+OH﹣(aq)═H2O(l);△H=﹣57.3 kJ/mol,若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的稀溶液混合,放出的热量大于57.3 kJ |
|
| D. | 在101kPa、25℃时,2g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l);△H=﹣285.8 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,往容积恒定的密闭容器中投入2molA和1molB,发生可逆反应:2A(g)+B(g)⇌C(g)+D(s),达到平衡时,测得压强为原压强的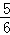 ,则A的转化率为( )
,则A的转化率为( )
|
| A. | 25% | B. | 40% | C. | 50% | D. | 75% |
查看答案和解析>>
科目:高中化学 来源: 题型:
请按要求填空
(1)下列实验操作或对实验事实的描述不正确的是 (填序号)
①用热的浓HCl洗涤附着有MnO2的试管;
②浓硫酸不小心沾在皮肤上,先用抹布擦干净,再用大量的水冲洗;
③测定硫酸铜晶体中结晶水含量的实验中,至少需经过4次称量;④蒸馏石油时,冷凝管中的冷水应上进下出;
⑤向蛋白质溶液中加入浓的无机盐(如Na2SO4、CuSO4)溶液,可使蛋白质盐析而分离提纯;
⑥配制一定浓度的溶液时,若定容时不小心加水超过容量瓶的刻度线,应立即用滴管吸去多余的部分.
(2)实验室利用如图装置进行中和热的测定.
回答下列问题:
①该图中有两处未画出,它们是 、 ;
②在操作正确的前提下提高中和热测定的准确性的关键是 ;
③如果用0.5 mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将 (填“偏大”、“偏小”、“不变”);原因是 .
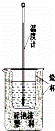
查看答案和解析>>
科目:高中化学 来源: 题型:
把100mL含有MgSO4和K2SO4的混合溶液分成二等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡.则原混合溶液中钾离子的浓度为( )
A. 20(2b﹣a) mol/L B. 20(b﹣2a) mol/L C. 10(2b﹣a) mol/L D. 10(b﹣2a) mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,属于氧化反应的是( )
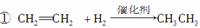
②2CH3CHO+O2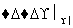 2CH3COOH
2CH3COOH
③CH3CHO+2Cu(OH)2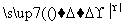 CH3COOH+Cu2O↓+2H2O
CH3COOH+Cu2O↓+2H2O
④CH3CHO+H2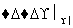 CH3CH2OH
CH3CH2OH
A.①② B.②③
C.③④ D.①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com