
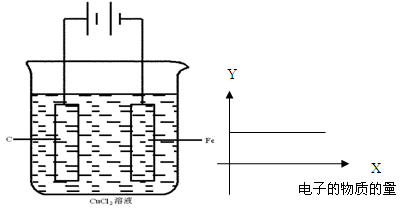
| A.Cu2+物质的量浓度 | B.C棒的质量 |
| C.Fe棒的质量 | D.Cl-物质的量浓度 |


 华东师大版一课一练系列答案
华东师大版一课一练系列答案科目:高中化学 来源:不详 题型:单选题
 从H+、K+、Cu2+、Cl-、SO中选取适当的离子组成符合下列情况的电解质。惰性电解,电 解质的物质的量减少,水的物质的量也减少,pH下降,则电解质的化学式为( )
从H+、K+、Cu2+、Cl-、SO中选取适当的离子组成符合下列情况的电解质。惰性电解,电 解质的物质的量减少,水的物质的量也减少,pH下降,则电解质的化学式为( )| A.HCl | B.K2SO4 | C.CuSO4 | D.KCl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
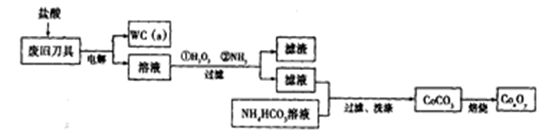
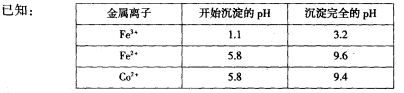
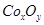 ,并测定其化学式。
,并测定其化学式。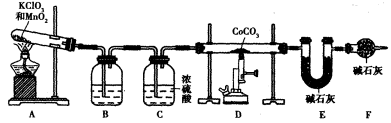
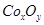 后,若称得E管增重4.40g,D管内残留物质的质量是8.30g,则生成物
后,若称得E管增重4.40g,D管内残留物质的质量是8.30g,则生成物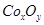 的化学式为____________。
的化学式为____________。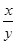 的值______(填“偏大”、“偏小”或“无影响”)。
的值______(填“偏大”、“偏小”或“无影响”)。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.随着电解的进行,c(NaCl)降低,需不断补充饱和食盐水 |
| B.电解过程中采用增大阳极区溶液pH的方法,可以减少Cl2在水中的溶解量 |
| C.阳离子交换膜的作用是阻止OH-移向阳极,以使氢氧化钠在阴极区富集 |
| D.阳极表面用钛氧化物涂层处理,目的是降低电解产物Cl2对电极的腐蚀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
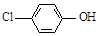 )的废水可以利用微生物电池除去,其原理如下图所示。
)的废水可以利用微生物电池除去,其原理如下图所示。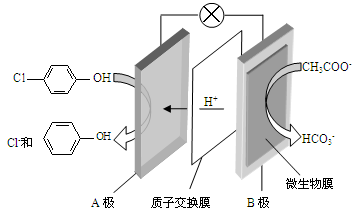
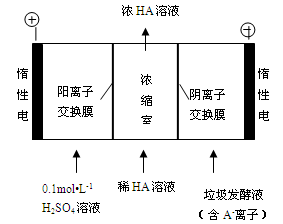
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
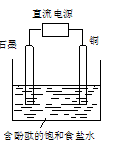
| A.铜电极附近观察到黄绿色气体 |
| B.石墨电极附近溶液呈红色 |
| C.溶液中的Na+向石墨电极移动 |
| D.铜电极上发生还原反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
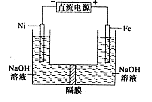
| A.铁是阳极,电极反应为Fe-6e一+4H2O=FeO42-+ 8H+ |
| B.电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极 |
| C.若隔膜为阴离子交换膜,则OH-自右向左移动 |
| D.电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
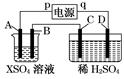
| 时间(min) | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 阴极产生气体 的体积(cm3) | 6 | 12 | 20 | 29 | 39 | 49 | 59 | 69 | 79 | 89 |
| 阳极产生气体 的体积(cm3) | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.10 mol·L-1AgNO3溶液 |
| B.0.10 mol·L-1ZnSO4溶液 |
| C.0.20 mol·L-1CuCl2溶液 |
| D.0.20 mol·L-1Pb(NO3)2溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com