
下列物质按纯净物、混合物、电解质、非电解质的顺序组合的一组为()
A. 纯盐酸、空气、硫酸、干冰
B. 蒸馏水、氨水、碳酸氢钠、二氧化硫
C. 胆矾、盐酸、铁、碳酸钙
D. 生石灰、漂白粉、氯化铜、碳酸钠
考点: 混合物和纯净物;电解质与非电解质.
专题: 物质的分类专题.
分析: 依据概念结合物质的组成结构进行分析判断;由同种物质组成的为纯净物,包括单质和化合物;由不同物质组成的为混合物;在水溶液或熔融状态下能导电的化合物为电解质;在水溶液和熔融状态下都不能导电的化合物为非电解质.
解答: 解:A、纯盐酸、空气、硫酸、干冰中纯盐酸为氯化氢气体的水溶液是混合物,故A错误;
B、蒸馏水、氨水、碳酸氢钠、二氧化硫按纯净物、混合物、电解质、非电解质的顺序组合的,故B正确;
C、胆矾、盐酸、铁、碳酸钙中铁是单质,碳酸钙是电解质,故C错误;
D、生石灰、漂白粉、氯化铜、碳酸钠中的碳酸钠是电解质,故D错误;
故选B.
点评: 本题考查了纯净物、混合物、电解质、非电解质的概念判断及各种物质的成分掌握,题目较简单.


科目:高中化学 来源: 题型:
非金属溴与氯气的性质很相似.在探究溴单质的性质时,其基本程序应该是()
A. 做实验并观察实验现象→分析、解释,得出结论
B. 观察溴的外观性质→做实验并观察实验现象→分析、 解释,得出结论
解释,得出结论
C. 观察溴的外观性质→预测溴的化学性质→做实验并观察实验现象→分析、解释,得出结论
D. 预测溴的性质→做实验并观察实验现象→分析、解释,得出结论 →观察溴的外观性质
→观察溴的外观性质
查看答案和解析>>
科目:高中化学 来源: 题型:
某实验小组用工业上废弃固体(主要成分Cu2S和Fe2O3)混合物制取粗铜和Fe2(SO4)3晶体,设计的操作流程如图:

(1)除酒精灯和铁架台或三脚架外,①中所需的容器和夹持仪器分别为 ,①和⑥中都用到的仪器为 ;
(2)试剂x的化学式为H2O2;x与溶液B反应的离子方程式为 ;
(3)某同学取少量的溶液B向其中加入过量的某种强氧化剂,再滴加KSCN溶液,发现溶液变红色,放置一段时间后,溶液褪色,该同学猜测溶液褪色的原因是溶液中的SCN﹣ 被过量的氧化剂氧化所致,现给出以下试剂:1.0mol•L﹣1硫酸、1.0mol•L﹣1 NaOH溶液、0.1mol•L﹣1 Fe2(SO4)3溶液、20%KSCN溶液、蒸馏水.请你设计合理实验验证乙同学的猜测是否合理.简要说明实验步骤和现象 .
查看答案和解析>>
科目:高中化学 来源: 题型:
已知FeS2中铁元素的化合价为+2价,关于反应:4CuSO4+5FeS2+12H2O═7Cu2S+5FeSO4+12H2SO4的下列说法正确的是()
A. 该反应的氧化剂只有CuSO4
B. SO42﹣既不是氧化产物也不是还原产物
C. 1 mol CuSO4还原了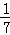 mol的S
mol的S
D. 被还原的S和被氧化的S的质量比为7:3
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示是用于气体制备、干燥(或除杂质)、性质验证、尾气处理的部分仪 器装置(加热及夹持固定装置均已略去,各装置可重复使用也可不用).请根据下列要求回答问题.
器装置(加热及夹持固定装置均已略去,各装置可重复使用也可不用).请根据下列要求回答问题.
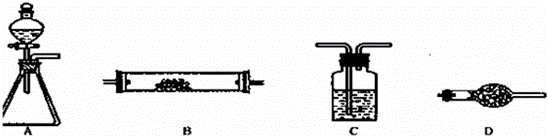
(1)若用A﹣C﹣D﹣B组合进行氢气还原氧化铜实验.分液漏斗中的试剂是盐酸,C中试剂是水,其作用是 ;A中反应开始一段时间后,再加热B.加热B之前的实验操作是 .
(2)为验证氯气不能使干燥的红布条褪色,置红布条于B中,按A﹣C﹣B﹣D连接成实验装置体系.A锥形瓶中试剂选用高锰酸钾晶体,则分液漏斗中的液体是 (填名称);C中试剂是浓硫酸(填名称).已知高锰酸钾反应生成+2价的锰离子,写出此法制备氯气的离子方程式 .
(3)为了进行氨的催化氧化实验,若锥形瓶中盛装足量的Na2O2粉末,分液漏斗中盛装浓氨水,慢慢打开分液漏斗的活塞,产生的气体通过红热的铂粉,各仪器装置按气流方向从左到右连接顺序是(填字母) ;装置B中发生反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是()
A. HClO中氯元素化合价比HClO4中氯元素化合价低,所以HClO4的氧化性强
B. 已知①Fe+Cu2+═Fe2++Cu;②2Fe3++Cu═2Fe2++Cu2+,则氧化性强弱顺序为:Fe3+>Cu2+>Fe2+
C. 已知还原性:B﹣>C﹣>D﹣,反应 2C﹣+D2═2D﹣+C2和反应2C﹣+B2═2B﹣+C2都能发生
D. 具有强氧化性和强还原性的物质放在一起就能发生氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
为确定某溶液的离子组成,分别进行如下实验:
①测定溶液的pH,溶液显强碱性.
②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体.
③在上述溶液中再滴加Ba(NO3)2溶液,产生白色沉淀.
④取上层清液继续滴加Ba(NO3)2溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀.
根据实验以下推测正确的是()
A. 一定有SO32﹣离子
B. 一定有CO32﹣离子
C. 一定有Cl﹣离子存在
D. 不能确定HCO3﹣离子是否存在
查看答案和解析>>
科目:高中化学 来源: 题型:
关于物质的分类正确组合是()
分类
组合 酸 碱 盐 氧化物
A H2SO4 Na2CO3 NaHCO3 SiO2
B HCl NaOH NaCl Na2O
C CO2 NaOH MgCl2 SO3
D HNO3 KOH CaO CaCO3
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
已知KNO3晶体溶解于水时要吸收热量,从溶液中析出KNO3晶体时会放出热量.若有室温下KNO3饱和溶液20mL,向其中加入1g KNO3晶体,充分搅拌后,下列判断正确的是( )
A. 溶液质量增加 B. 溶液的温度降低
C. 晶体不再溶解 D. 溶液的温度和质量都不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com