
【题目】工业合成氨反应N2+3H2![]() 2NH3,是一个正反应为放热的可逆反应。下列说法正确的是
2NH3,是一个正反应为放热的可逆反应。下列说法正确的是
A. 使用合适的催化剂可以加快反应速率,提高生产效率
B. 生成物的总能量大于反应物的总能量
C. 将该反应设计成原电池,放出的热量不变
D. 达到平衡时,N2的浓度与NH3的浓度一定相等
【答案】A
【解析】分析A、使用催化剂加快了反应速率,缩短反应时间,提高反应效率,平衡不移动;B、正反应是放热反应;C、若把该反应设计成原电池,化学能除转化成热能外,还转化成电能,所以放出的热量应减少;D、达到平衡状态时,正逆反应速率相等,各物质的浓度不变,以此解答。
A、使用催化剂加快了反应速率,缩短反应时间,提高反应效率,平衡不移动,所以A选项是正确的;
B、正反应是放热反应,则生成物的总能量小于反应物的总能量,故B错误;
C、若把该反应设计成原电池,化学能除转化成热能外,还转化成电能,所以放出的热量应减少,故C错误;
D.达到平衡状态时,正逆反应速率相等,各物质的浓度不变但不一定相等,故D错误;
所以A选项是正确的。


科目:高中化学 来源: 题型:
【题目】甲醇属于可再生能源,可代替汽油作为汽车燃料,下列热化学方程式中的反应热能够正确表示甲醇燃烧热的是( )
A.CH3OH(l)+ ![]() O2(g)═CO2(g)+2H2O(l)△H=+726.5kJ/mol
O2(g)═CO2(g)+2H2O(l)△H=+726.5kJ/mol
B.CH3OH(l)+ ![]() O2(g)═CO2(g)+2H2O(l)△H=﹣726.5kJ/mol
O2(g)═CO2(g)+2H2O(l)△H=﹣726.5kJ/mol
C.CH3OH(l)+ ![]() O2(g)═CO2(g)+2H2O(g)△H=﹣675.3kJ/mol
O2(g)═CO2(g)+2H2O(g)△H=﹣675.3kJ/mol
D.2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=﹣1453kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组对采集的酸雨样品进行化验,测得数据如下:c(Na+)=5.0×10-6 mol/L、c(NH4+)=2.0×10-5 mol/L、c(NO3-)=2.0×10-4 mol/L、c(SO42-)=4.0×10-4 mol/L,H+和OH-浓度未测定,则此酸雨的pH约为
A.3 B.4 C.5 D.6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,不正确的是( )
A.光合作用是将光能转化为化学能的有效途径
B.煤,石油,天然气都是可再生的化石燃料
C.用植物秸秆制沼气是有效利用生物质能的方式之一
D.开发氢能,太阳能,风能,生物质能等是实现“低碳生活”的有效途径
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,在体积不变的密闭容器中发生反应:X(g)+3Y(g)2Z(g),各组分在不同时刻的浓度如表:
物质 | X | Y | Z |
初始浓度/(molL﹣1) | 0.1 | 0.2 | 0 |
2min末浓度/(molL﹣1) | 0.08 | a | b |
平衡浓度/(molL﹣1) | 0.05 | 0.05 | 0.1 |
下列说法正确的是( )
A.平衡时,X的转化率为5%
B.t℃时,该反应的平衡常数为40
C.增大平衡后的体系压强,v(正)增大,v(逆)减小,平衡向正反应方向移动
D.2 min内,用Y的变化量表示的平均反应速率v(Y)=0.03 molL﹣1min﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以铬铁矿[Fe(CrO2)2]为原料可制备K2Cr2O7和金属铬。实验流程如下:
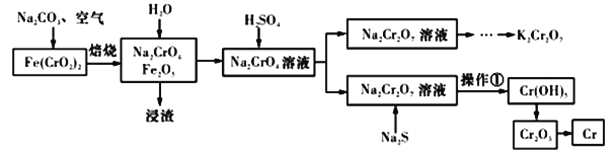
已知:2CrO42-+2H+=Cr2O72-+H2O。pH<3.0,CrO42-含量极小。
(1)写出铬铁矿焙烧转化为Na2CrO4的化学反应方程式:_____________________。焙烧时不能使用陶瓷容器的原因是________________________________________。
(2)判断加入稀硫酸的量已经足量的标准是_______________________________________。
(3)操作①包括过滤和洗涤。实验室洗涤沉淀的操作是________________________________。
(4)Na2S的作用是调节溶液的酸碱度和_____________________。
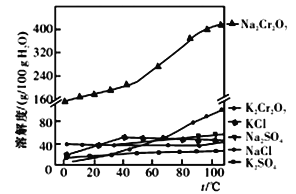
(5)Fe3+在pH为3.7时可完全转化为Fe(OH)3。在上述流程中所得Na2Cr2O7溶液中含有少量Fe3+。请结合上图有关物质的溶解度曲线,设计由Na2Cr2O7溶液制备K2Cr2O7固体的实验方案(实验中须选用的试剂:硫酸溶液、NaOH溶液、KCl固体、蒸馏水):
步骤①除杂质:__________________________________________________________________;
步骤②制备K2Cr2O7固体:__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于0.1 mol/L碳酸钠溶液的叙述正确的是( )
A.溶液中阴离子的物质的量为0.1 mol
B.加水稀释时水解平衡向正反应方向移动,溶液中所有离子浓度均减小
C.升高温度,水解平衡向正反应方向移动
D.加入氢氧化钠固体,可以使溶液中c(Na+):c(CO ![]() 2﹣)=2:1
2﹣)=2:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com