
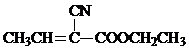 )是合成某种手术用粘合剂的单体,X的合成路线如图:
)是合成某种手术用粘合剂的单体,X的合成路线如图: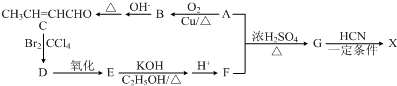

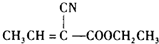 ,故G为CH3C≡CCOOCH2CH3,由F与A反应生成CH3C≡CCOOCH2CH3.C为CH3CH=CHCHO,与溴发生加成反应生成D为CH3CHBrCHBrCHO,D氧化生成E为CH3CHBrCBrCOOH,E发生消去反应、酸化得到生成F为CH3C≡CCOOH,结构G的结构可知,A为CH3CH2OH,A发生催化氧化生成B为CH3CHO,由信息中反应可知,醛中α-H活泼,两分子醛发生加成反应,由B、C转化关系可知,乙醛先发生加成反应,再发生醇的消去反应,可以生成C(CH3CH=CCHO),据此答题.
,故G为CH3C≡CCOOCH2CH3,由F与A反应生成CH3C≡CCOOCH2CH3.C为CH3CH=CHCHO,与溴发生加成反应生成D为CH3CHBrCHBrCHO,D氧化生成E为CH3CHBrCBrCOOH,E发生消去反应、酸化得到生成F为CH3C≡CCOOH,结构G的结构可知,A为CH3CH2OH,A发生催化氧化生成B为CH3CHO,由信息中反应可知,醛中α-H活泼,两分子醛发生加成反应,由B、C转化关系可知,乙醛先发生加成反应,再发生醇的消去反应,可以生成C(CH3CH=CCHO),据此答题.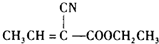 ,故G为CH3C≡CCOOCH2CH3,由F与A反应生成CH3C≡CCOOCH2CH3.C为CH3CH=CHCHO,与溴发生加成反应生成D为CH3CHBrCHBrCHO,D氧化生成E为CH3CHBrCBrCOOH,E发生消去反应、酸化得到生成F为CH3C≡CCOOH,结构G的结构可知,A为CH3CH2OH,A发生催化氧化生成B为CH3CHO,由信息中反应可知,醛中α-H活泼,两分子醛发生加成反应,由B、C转化关系可知,乙醛先发生加成反应,再发生醇的消去反应,可以生成C(CH3CH=CCHO),
,故G为CH3C≡CCOOCH2CH3,由F与A反应生成CH3C≡CCOOCH2CH3.C为CH3CH=CHCHO,与溴发生加成反应生成D为CH3CHBrCHBrCHO,D氧化生成E为CH3CHBrCBrCOOH,E发生消去反应、酸化得到生成F为CH3C≡CCOOH,结构G的结构可知,A为CH3CH2OH,A发生催化氧化生成B为CH3CHO,由信息中反应可知,醛中α-H活泼,两分子醛发生加成反应,由B、C转化关系可知,乙醛先发生加成反应,再发生醇的消去反应,可以生成C(CH3CH=CCHO),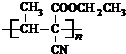 ,故答案为:
,故答案为: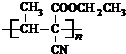 ;
;| Cu |
| △ |
| Cu |
| △ |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、CH3COOH+H2O?CH3COO-+H3O+ |
| B、CO2+H2O?H2CO3 |
| C、CO32-+H2O?HCO3-+OH- |
| D、HCO3-+OH-?CO32-+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
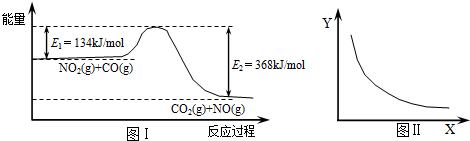
| A、该反应的焓变△H=+234 kJ?mol-1 |
| B、若X表示体系的压强,则Y表示的可能是NO2的转化率 |
| C、若X表示温度则Y表示的可能是CO2物质的量浓度 |
| D、增大CO的起始浓度,平衡向正反应方向移动,反应热增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| 读数次数 | 质量/g | |
| 锥形瓶+水+试样 | 第1次 | 196.30 |
| 第2次 | 196.15 | |
| 第3次 | 196.05 | |
| 第4次 | 196.00 | |
| 第5次 | 196.00 |

查看答案和解析>>
科目:高中化学 来源: 题型:
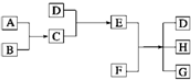 已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如图所示:
已知A、B、C、D为气体,E、F为固体,G是氯化钙,它们之间的转换关系如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 溶解 |
| 沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com