
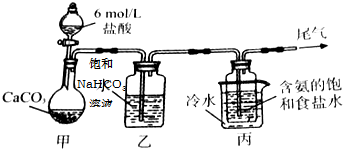
���� ��װ�ü����Ʊ�������̼�������к����Ȼ�������Ժ���ʵ��������ţ���Ҫ��ȥ��װ���ҳ�ȥCO2�е�HCl���壬װ�ñ����ǰ����ı���ʳ��ˮ��ͨ�������̼����̼�����ƾ��壬ͨ�����˵õ�����ϴ�����յõ�̼���ƣ�NaHCO3ת��ΪNa2CO3�ķ����ǹ�����ȷֽ⣬β���к��а����������ŵ������У���Ҫ���գ�
��1�������ı���ʳ��ˮ��ͨ�������̼���������ֽⷴӦ������̼�����ƾ��壻
��2�������ӷ�����ȡ�Ķ�����̼�к����Ȼ��⣬�Ȼ����ܺ�̼�����Ʒ�Ӧ�����ȥ������Ϊ������Ⱦ������β�����գ�
��3��̼������Ϊ�����������ϴ�ӡ�̼�����Ʋ��ȶ����ڼ����������ֽܷ�����̼���ơ�ˮ�Ͷ�����̼��
�����ӳ�ȥ��������ӣ������ӹ������ټ��Ȼ����������ɳ�����̼�ᱵ�����ϸ��������ӣ�����������Һ����ϴҺ���ɣ�����ng����ΪBaCO3������̼�غ����̼���Ƶ���������ƷmgΪ̼���ƺ��Ȼ��ƣ���Ʒ��NaCl����������=$\frac{�Ȼ��Ƶ�����}{��Ʒ������}$��100%��
��� �⣺��1��������������̼��ˮ���Ȼ��Ʒ�����Ӧ����̼�����ƺ��Ȼ�泥���Ӧ����ʽΪNH3+CO2+H2O+NaCl=NaHCO3��+NH4Cl��
�ʴ�Ϊ��NH3+CO2+H2O+NaCl=NaHCO3��+NH4Cl��
��2������������ȡ������̼ʱ������̼�г��Ậ���Ȼ������壬̼�������������ᷴӦ������ͨ��װ���ұ���̼�����Ƶ���Һ��Ϊ�˳���������̼�е��Ȼ������壬β��Ϊ������������̼������Ϊ�д̼�����ζ�����壬Ϊ������Ⱦ�Ϊ��ֹ��Ⱦ������β���к��еİ�������NH3����Ҫ�������մ����������������գ�
�ʴ�Ϊ����ȥCO2�е�HCl���壻 ��������NH3����
��3��������������̼��ˮ���Ȼ��Ʒ�����Ӧ����̼�����Ƴ������Ȼ�泥�ͨ�����˷����̼�����ƣ�������ϴ�ӣ�̼���������ȷ����ķ�ӦΪ��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+CO2��+H2O���������յõ�̼���ƣ�
�ʴ�Ϊ��ϴ�ӣ����գ�
���Ȼ������������ܷ�Ӧ�������ᱵ�����������Ϊ��ȡ�����ϲ���Һ���Թ��У�������������Һ��������ǣ�˵����Һ�к��б����ӣ����Ȼ�����Һ�ѹ�������֮���ǹ����ģ�
�ʴ�Ϊ��ȡ�����ϲ���Һ���Թ��У����������ƣ�����������˵���Ȼ����ǹ����ģ���֮���ǹ����ģ�
BaCl2�ѹ��������ټ��Ȼ����������ɳ�������ʵ�鷽��Ϊ���ã����ϲ���Һ�м����μ�BaCl2��Һ�����ް�ɫ�������ɣ���֤��BaCl2�ѹ�����̼�ᱵ�����������������ӣ�����Ҫ����ϴ�ӣ���ϴ��Һ�еμ���������Һ�������������ɫ������˵��ϴ�Ӹɾ�������ϴ�Ӳ��ɾ�������ng����ΪBaCO3�����ʵ���Ϊ��$\frac{ng}{197g/mol}$����̼���Ƶ�����Ϊ��$\frac{ng}{197g/mol}$�����Ȼ��Ƶ�����Ϊ��m-$\frac{106n}{197}$��������������Ϊ��$\frac{m-\frac{106n}{197}}{m}$��=��1-$\frac{106n}{197m}$����100%��
�ʴ�Ϊ�����ã����ϲ���Һ�м����μ�BaCl2��Һ�����ް�ɫ�������ɣ���֤��BaCl2�ѹ�����AgNO3��Һ����1-$\frac{106n}{197m}$����100%��
���� ������һ���йع�ҵ�ƴ���֪ʶ��һ���ۺ�ʵ����Ŀ������ѧ�������ͽ������������������Ƽ�ԭ���ǽ���Ĺؼ�����Ŀ�Ѷ��еȣ�


 ����ѧҵ���Ե�����ϵ�д�
����ѧҵ���Ե�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
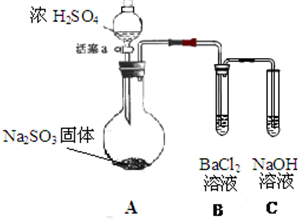 ijͬѧ���������ʵ��װ��ͼ�����г�װ�úͼ���װ���ԣ��������Ѽ��飩��
ijͬѧ���������ʵ��װ��ͼ�����г�װ�úͼ���װ���ԣ��������Ѽ��飩���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
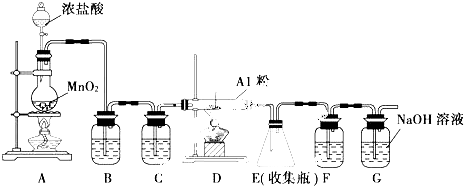
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
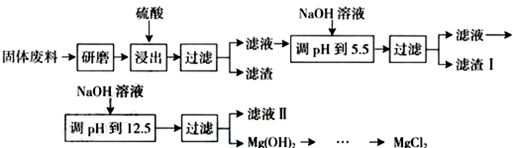
| ������ | Fe3+ | Al3+ | Mg2+ |
| pH | 3.2 | 5.2 | 12.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ʹ��ϡ��Һ | B�� | ѡ����ʵĴ��� | ||
| C�� | ��ϸ���巴Ӧ�� | D�� | ��߷�Ӧ��ϵ���¶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ҩ�� | θ��ƽ | ��ϲ |
| ��Ч�ɷֵĻ�ѧʽ | Al��OH��3 | Al2Mg6��OH��16CO3•4H2O |
| ��Է������� | 78 | 530 |
| ÿƬ����Ч�ɷݵ�ҩ�� | 0.245g | 0.5g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
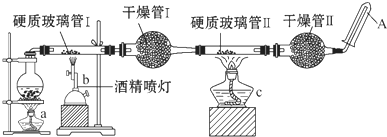 �ڳ����£�Fe��ˮ������Ӧ�����ڸ����£�Fe����ˮ����������Ӧ��Ӧ������װ�ã���̽����Ӧ�IJ��ֲ����Ӳ�ʲ����ܢ��з��뻹ԭ���ۺ�ʯ���Ļ���Ӳ�ʲ����ܢ��м���CuO������ܢ���ʢװ����������ˮ����ͭ��ʯ���Ļ����
�ڳ����£�Fe��ˮ������Ӧ�����ڸ����£�Fe����ˮ����������Ӧ��Ӧ������װ�ã���̽����Ӧ�IJ��ֲ����Ӳ�ʲ����ܢ��з��뻹ԭ���ۺ�ʯ���Ļ���Ӳ�ʲ����ܢ��м���CuO������ܢ���ʢװ����������ˮ����ͭ��ʯ���Ļ�����鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com