
���� ��1���������ʵ����ʵ����뷴Ӧ�ȳ����ȣ��Ȼ�ѧ����ʽ����дҪ����������
��2���ٸ��ݻ�ѧ����ʽ�ĺ�����м������ȽϷ�Ӧ�ȵĴ�С��
����ͬ�����£������ͬ�����ʵ�����ͬ����ֱ�Ϊ1molH2��1molCH4��1molCO���ų��������ֱ�Ϊ285.8KJ��890.3KJ��$\frac{256.5}{2}$KJ���ݴ˽��з�����
��3����֪A������ܶ���ͬ��ͬѹ�¼���������ܶ���ͬ����A��ƽ����Է�������Ϊ16����A�������Ϊ��CH4����H2��CO�ݴ˽��з�����
��� �⣺��1����֪1��������ȫȼ�գ�����Һ̬ˮʱ�ܷų��ų�142.9kJ��������2��������ȫȼ�գ�����Һ̬ˮʱ�ܷų��ų�2��142.9kJ=285.8kJ�����������Ȼ�ѧ����ʽΪH2��g��+$\frac{1}{2}$O2��g��=H2O��l����H=-285.8kJ•mol-1��
�ʴ�Ϊ��H2��g��+$\frac{1}{2}$O2��g��=H2O��l����H=-285.8kJ•mol-1��
��2���١�H���ʱ䣬��ֵΪ��ֵʱ����Ӧ���ȣ����ź��������Խ�ų���������Խ���ź��������ԽС���ų���������ԽС��H2��CH4��CO����Է��������ֱ�Ϊ2��16��28��������ͬ��������3��ȼ�ϵ����ʵ���֮�Ⱦ��ǣ�$\frac{1}{2}$��$\frac{1}{16}$��$\frac{1}{28}$��ȼ�շų�����֮��Ϊ����$\frac{1}{2}$��285.8kJ������$\frac{1}{16}$��890.3kJ������$\frac{1}{28}$��$\frac{265.6}{2}$kJ��=
142.9KJ��55.64KJ��4.74KJ�����Էų�����������H2��
�ʴ�Ϊ��H2��
����ͬ�����£������ͬ�����ʵ�����ͬ����ֱ�Ϊ1molH2��1molCH4��1molCO���ų��������ֱ�Ϊ285.8KJ��890.3KJ��$\frac{256.5}{2}$KJ���ʷų�����������CH4��
�ʴ�Ϊ��CH4��
��3����֪A������ܶ���ͬ��ͬѹ�¼���������ܶ���ͬ����A��ƽ����Է�������Ϊ16����A�������Ϊ
��CH4����1mol�ų�������Ϊ890.3kJ
��H2��CO����H2��CO�ֱ�Ϊxmol��ymol����x+y=1�٣�A��ƽ����Է�������Ϊ16����$\frac{2x+28y}{x+y}=16��$�������٢ڵã�x=$\frac{6}{13}$mol��y=$\frac{7}{13}$mol��1molH2�ų�������Ϊ285.8kJ����$\frac{6}{13}$molH2�ų�������Ϊ$\frac{6}{13}��$285.8kJ=131.9kJ��2molCO�ų�������Ϊ565.6kJ����$\frac{7}{13}$molCO�ų�������$\frac{7}{13}��\frac{1}{2}$��565.6kJ=156.3kJ����
�ų���������Ϊ131.3kJ+156.3kJ=287.6kJ����287.6kJ��Q��890.3kJ��
�ʴ�Ϊ��287.6kJ��Q��890.3kJ��
���� ���⿼��ѧ���й��Ȼ�ѧ����ʽ�ļ���֪ʶ�����Ը�����ѧ֪ʶ���ش��ѶȲ���


 ͬ����ϰ���ϴ�ѧ������ϵ�д�
ͬ����ϰ���ϴ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1.12L | B�� | 2.24L | C�� | 3.36L | D�� | 4.48L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | M�ܷ����������ӳɡ�������Ӧ | |
| B�� | ��̼�����Ʋ��ܼ���M�����д����Ȼ� | |
| C�� | M�ķ���ʽΪC8H8O4 | |
| D�� | M�ı�����һ�ȴ�����2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH3��Һ����Һ������������� | |
| B�� | ϡHNO3������������ŨHNO3 | |
| C�� | �����̬����ʱҪ�ܷⱣ�棬������������ | |
| D�� | ����ֻ�ܱ�Zn��Fe�Ƚ�����ԭ��H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 14.3g | B�� | 25.4g | C�� | 28.6g | D�� | 50.6g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����Ȼ�� | B�� | ˮͨ��ֽ� | C�� | �Ȼ�������ˮ | D�� | ���ڻ���ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
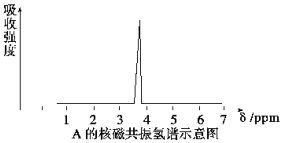 ��1��������A��B�ķ���ʽ����C2H4Br2��A�ĺ˴Ź���������ͼ��ʾ����A�Ľṹ��ʽΪCH2BrCH2Br����Ԥ��B�ĺ˴Ź�����������2���壨�źţ���
��1��������A��B�ķ���ʽ����C2H4Br2��A�ĺ˴Ź���������ͼ��ʾ����A�Ľṹ��ʽΪCH2BrCH2Br����Ԥ��B�ĺ˴Ź�����������2���壨�źţ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ж�����һ��Ԫ�� | B�� | һ����ϡ������Ԫ�� | ||
| C�� | һ���ǹ���Ԫ�� | D�� | һ���ǽ���Ԫ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com