
分析 (1)碱或强碱弱酸盐其溶液都呈碱性;
(2)pH=-lgc(H+);
(3)醋酸钠促进水电离,根据氢离子浓度结合水的离子积常数计算氢氧根离子浓度;
(4)醋酸根离子在溶液中水解生成氢氧根离子,溶液显碱性;
解答 解:(1)碱或强碱弱酸盐其溶液都呈碱性,氢氧化钠和氨水、醋酸钠溶液都呈碱性,
故答案为:②④⑤;
(2)常温下0.01mol/L HCl溶液中c(H+)=0.01mol/L,pH=-lgc(H+)=-lg0.01=2,故答案为:2;
(3)醋酸钠促进水电离,醋酸钠溶液中氢离子浓度为10-11mol/L,根据水的离子积常数知,氢氧根离子浓度等于10-3 mol/L,
故答案为:10-3 mol/L;
(4)醋酸根离子在溶液中水解生成氢氧根离子,溶液显碱性,其水解离子方程式为:CH3COO-+H2O?CH3COOH+OH-;
故答案为:CH3COO-+H2O?CH3COOH+OH-;
点评 本题考查了弱电解质的电离、溶液PH计算等知识点,根据弱电解质电离特点来分析解答,明确盐类水解实质是解本题关键,题目难度不大.


 每课必练系列答案
每课必练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
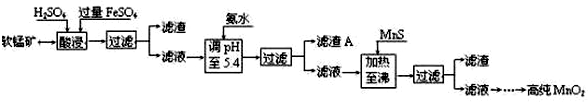
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 | CuS | ZnS | MnS | FeS |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 | ≥-0.42 | ≥2.5 | ≥7 | ≥7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 1:3 | C. | 3:2 | D. | 1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| B. | 铁和稀硝酸反应:Fe+2H+═Fe2++H2↑ | |
| C. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| D. | FeCl2溶液跟Cl2反应:2Fe2++Cl2═2Fe3++2Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 室温下,pH=3的溶液中:AlO2-、Al3+、Cl-、SO42- | |
| B. | 含有大量Fe3+的溶液中:K+、Mg2+、S2-、NO3- | |
| C. | 由水电离的c(H+)=10-11 mol•L-1的溶液中,K+、Na+、Cl-、SO42- | |
| D. | c(H+)<c(OH-)的溶液中:Na+、NH4+、CO32-、S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,78g Na2O2含有的阴离子数为NA | |
| B. | 常温常压下,22.4 L氢气中含氢原子数目为2 NA | |
| C. | 0.5 mol/L的NaCl溶液中,含有Cl-数目为0.5 NA | |
| D. | 1mol Fe在足量氯气中完全反应,失去的电子数为2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:B2->D3+ | |
| B. | 最高价氧化物对应的水化物碱性:C>D | |
| C. | 失电子能力:A>C | |
| D. | A与B可形成共价化合物:A2B、A2B2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
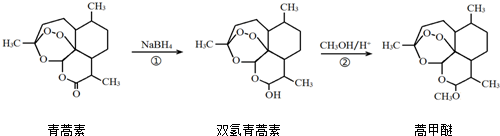
| A. | 青蒿素的分子式是C15H21O4 | |
| B. | 青蒿素在NaOH溶液中可以发生水解反应 | |
| C. | 反应②有H2O生成 | |
| D. | 反应①氧化反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com