
分析 (1)二氧化硫具有还原性,可以抗氧化;
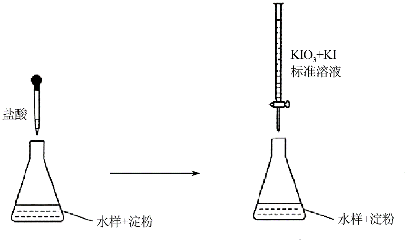
(2)酸性条件下S2O32-发生自身的氧化还原反应,生成二氧化硫,二氧化硫与水反应生成亚硫酸;
(3)①酸性条件下,KIO3溶液与KI溶液发生反应生成I2;
②反应①所得I2的作用是氧化亚硫酸根离子和硫代硫酸根离子;
③100mL的水样共消耗xmL标准溶液.若消耗1mL标准溶液相当于SO32-的质量1g,所以100mL中含有xgSO32-,所以1L该水样中SO32-的含量为104xmg/L;
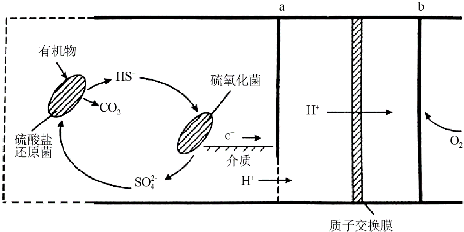
(4)①HS-在硫氧化菌作用下转化为SO42-,失电子发生氧化反应,电极反应式是HS-+4H2O-8e-=SO42-+9H+;
②由图可知硫酸盐还原菌可以将有机物氧化成二氧化碳,而硫氧化菌可以将硫氢根离子氧化成硫酸根离子,所以两种细菌存在,就会循环把有机物氧化成CO2 放出电子.
解答 解:(1)SO2可以防止酒液氧化.这应用了SO2的还原性,故答案为:还原性;
(2)酸性条件下S2O32-发生自身的氧化还原反应,生成二氧化硫,二氧化硫与水反应生成亚硫酸,使水体中亚硫酸浓度增大,故答案为:在酸性条件下2H++S2O32-=SO2↓+S↓+H2O,SO2+H2O=H2SO3,导致溶液中酸性增强;
(3)①酸性条件下,KIO3溶液与KI溶液发生反应生成I2,离子方程式为:IO3-+5I-+6H+=3I2+3H2O,故答案为:1、5、6、H+、3、3;
②反应①所得I2的作用是氧化亚硫酸根离子和硫代硫酸根离子,故答案为:氧化亚硫酸根离子和硫代硫酸根离子;
③100mL的水样共消耗xmL标准溶液.若消耗1mL标准溶液相当于SO32-的质量1g,所以100mL中含有xgSO32-,所以1L该水样中SO32-的含量为104xmg/L,故答案为:104x;(4)①HS-在硫氧化菌作用下转化为SO42-,失电子发生氧化反应,电极反应式是HS-+4H2O-8e-=SO42-+9H+,故答案为:HS-+4H2O-8e-=SO42-+9H+;②由图可知硫酸盐还原菌可以将有机物氧化成二氧化碳,而硫氧化菌可以将硫氢根离子氧化成硫酸根离子,所以两种细菌存在,就会循环把有机物氧化成CO2 放出电子,使电池则可以持续供电,故答案为:两种细菌存在,就会循环把有机物氧化成CO2 放出电子,使电池则可以持续供电.
点评 本题考查元素化合物相关计算问题、氧化还原滴定以及电化学的相关知识,综合性强,有一定的难度.


 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案科目:高中化学 来源: 题型:选择题
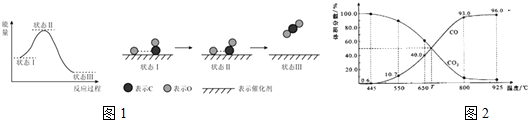
| A. | 该反应中旧键断裂吸收的总能量大于新键形成放出的总能量 | |
| B. | 反应物的总能量高于生成物的总能量 | |
| C. | 该反应为放热反应 | |
| D. | 该反应的化学能可以转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
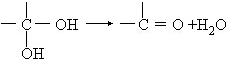
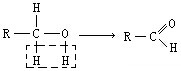
 (在方框中填写有机物的结构简式,说明加氧氧化)
(在方框中填写有机物的结构简式,说明加氧氧化)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 打开反应釜,将Na 暴露在空气中与氧气反应 | |
| B. | 向反应釜通入Cl2,Na 在Cl2中燃烧生成NaCl | |
| C. | 向反应釜加大量H2O,通过化学反应“除掉”金属钠 | |
| D. | 向反应釜滴加C2H5OH,并设置放气管,排出氢气和热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯与溴能发生取代反应,因此不能用苯萃取溴水中的溴 | |
| B. | 相同质量的苯和立方烷(C${\;}_{{8}_{\;}}$H8)完全燃烧,耗氧量一样多 | |
| C. | 乙烯和聚乙烯都能发生加成反应 | |
| D. | 为了防止蛋白质盐析,疫苗等生物制剂应冷冻储存 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
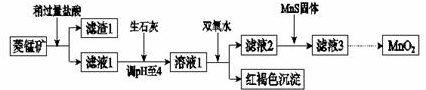
| Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀时 | 8.3 | 6.3 | 2.7 | 4.7 |
| 完全沉淀时 | 9.8 | 8.3 | 3.7 | 6.7 |
 纸置于阳极附近,若试纸变蓝则证明有Cl2生成.
纸置于阳极附近,若试纸变蓝则证明有Cl2生成.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | NaOH/mol•L-1 | HA/mol•L-1 | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.1 | 0.2 | pH<7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,0.1 mol•L-1Na2S溶液中存在:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| B. | 常温下,0.1 mol•L-1HA溶液与0.1 mol•L-1NaOH溶液恰好完全反应时,溶液中一定存在:c(Na+)=c(A-)>c(OH-)=c(H+) | |
| C. | 常温下,将0.1 mol•L-1CH3COOH溶液加水稀释,当溶液的pH从3.0升到4.0时,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$的值增大到原来的10倍 | |
| D. | 常温下,pH=7的CH3COONa和CH3COOH混合溶液中c(Na+)=0.1 mol•L-1:c(Na+)=c(CH3COOH)>c(CH3COO-)>c(H+)=c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com