
| 离子 | H+ | K+ | NO3- | SO42- |
| 物质的量(mol) | 0.5 | 0.1 | 0.6 | 0.15 |
| 0.9mol-0.6mol |
| 3 |
| 0.1mol |
| 0.2L |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、受热时碳酸钠比碳酸氢钠稳定 |
| B、在同温下,碳酸钠比碳酸氢钠的溶解度大 |
| C、物质的量相等的碳酸钠与碳酸氢钠分别溶于水后,碳酸氢钠水溶液的碱性较强 |
| D、相同物质的量的碳酸钠与碳酸氢钠分别与足量的盐酸反应,两者放出的二氧化碳一样多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③⑥ | B、②③⑥⑧ |
| C、①④⑤⑦ | D、①②③⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H2)?c(CO) |
| c(H2O) |
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
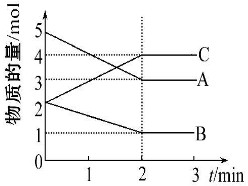
 化曲线如图所示.下列说法正确的是
化曲线如图所示.下列说法正确的是查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向物质的量比为1:1的Na2CO3和NaOH混合溶液中通入少量CO2,NaOH先发生反应 |
| B、向体积比为1:1的SO2和CO2混合气体中加入少量氨水,CO2先发生反应 |
| C、向物质的量之比为1:1的FeCl3和CuCl2混合溶液中加入少量Fe粉,Cu2+先被还原 |
| D、向NH4Al(SO4)2溶液中滴加少量NaOH溶液,NH4+先发生反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com