
 2NO + O2 ¦¤H >0 “ļµ½Ę½ŗāŗó£¬ÉżĪĀ,»ģŗĻĘųĢåµÄ£Ø £©²»±ä
2NO + O2 ¦¤H >0 “ļµ½Ę½ŗāŗó£¬ÉżĪĀ,»ģŗĻĘųĢåµÄ£Ø £©²»±ä| A£®ĆÜ¶Č | B£®ŃÕÉ« | C£®Ń¹Ēæ | D£®×ÜĪļÖŹµÄĮæ |
 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĪŹ“šĢā
| “߻ƼĮ |
| Ź±¼ä/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c£ØNO£©/mol?L-1 | 1.00”Į10-3 | 4.50”Į10-4 | 2.50”Į10-4 | 1.50”Į10-4 | 1.00”Į10-4 | 1.00”Į10-4 |
| c£ØCO£©/mol?L-1 | 3.60”Į10-3 | 3.05”Į10-3 | 2.85”Į10-3 | 2.75”Į10-3 | 2.70”Į10-3 | 2.70”Į10-3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 2C(Ęų)“ļµ½Ę½ŗāµÄ±źÖ¾ŹĒ( )
2C(Ęų)“ļµ½Ę½ŗāµÄ±źÖ¾ŹĒ( ) ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®»Æѧ·“Ó¦µÄĻŽ¶Č¶¼ĻąĶ¬ |
| B£®æÉŅŌĶعżøıäĪĀ¶ČæŲÖĘ»Æѧ·“Ó¦µÄĻŽ¶Č |
| C£®æÉŅŌĶعżŃÓ³¤»Æѧ·“Ó¦µÄŹ±¼äøıä»Æѧ·“Ó¦µÄĻŽ¶Č |
| D£®µ±Ņ»øö»Æѧ·“Ó¦ŌŚŅ»¶ØĢõ¼žĻĀ“ļµ½ĻŽ¶ČŹ±£¬·“Ó¦¼“Ķ£Ö¹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| ±ąŗÅ | »Æѧ·½³ĢŹ½ | Ę½ŗā³£Źż | ĪĀ¶Č | |
| 979K | 1173K | |||
| I | Fe(s)+CO2(g) 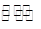 2 FeO(s)+CO(g) 2 FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| II | CO(g)+H2O(g) 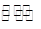 CO2(g)+H2(g) CO2(g)+H2(g) | K2 | 1.62 | b |
| III | Fe(s)+H2O(g)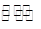 FeO(s)+H2(g) FeO(s)+H2(g) | K3 | a | 1.68 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 4P (g)£«Q(g)
4P (g)£«Q(g)
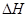 £¼0”£ŌŚŅ»¶ØĪĀ¶Č”¢Ń¹ĒæĻĀ“ļµ½Ę½ŗā£¬Ę½ŗāŹ±PµÄĪļÖŹµÄĮæÓėĘšŹ¼Ź±¼ÓČėNµÄĪļÖŹµÄĮæµÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£ŗ
£¼0”£ŌŚŅ»¶ØĪĀ¶Č”¢Ń¹ĒæĻĀ“ļµ½Ę½ŗā£¬Ę½ŗāŹ±PµÄĪļÖŹµÄĮæÓėĘšŹ¼Ź±¼ÓČėNµÄĪļÖŹµÄĮæµÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£ŗ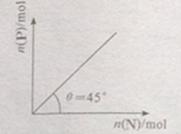
| A£®Ę½ŗāŹ±NµÄ×Ŗ»ÆĀŹĪŖ50% |
B£®µ±ĪĀ¶ČÉżøßŗó£¬ŌņĶ¼ÖŠ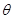 £¾45 £¾45 |
| C£®ČōŌŁ¼ÓČėN£¬ŌņÕż”¢Äę·“Ó¦ĖŁĀŹ¾łÖš½„Ōö“ó |
| D£®ČōŌŁ¼ÓČėN£¬Ōņ·“Ó¦ĢåĻµÖŠĘųĢåĆÜ¶Č¼õŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
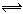 2AB(g) £¬·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄ±źÖ¾ŹĒ
2AB(g) £¬·“Ó¦“ļµ½Ę½ŗāדĢ¬µÄ±źÖ¾ŹĒ ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
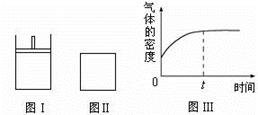 ””””
”””” a Z£Øg£©”£
a Z£Øg£©”£| A£®ĪļÖŹZµÄ»Æѧ¼ĘĮæŹża = 2 |
| B£®ČōX”¢Y¾łĪŖĘųĢ¬£¬ŌņŌŚĘ½ŗāŹ±XµÄ×Ŗ»ÆĀŹ£ŗ¢ń£¾ ¢ņ |
| C£®Čō¢ņÖŠĘųĢåµÄĆܶČČēĶ¼¢óĖłŹ¾£¬ŌņX”¢Y¶¼ĪŖĘųĢ¬ |
| D£®ČōXĪŖ¹ĢĢ¬”¢YĪŖĘųĢ¬£¬Ōņ¢ń”¢¢ņÖŠ“ÓæŖŹ¼µ½Ę½ŗāĖłŠčµÄŹ±¼ä£ŗ¢ń£¾¢ņ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĪŹ“šĢā
 CH3OH(g)
CH3OH(g)| A£®Éś³ÉCH3OHµÄĖŁĀŹÓėĻūŗÄCOµÄĖŁĀŹĻąµČ | B£®»ģŗĻĘųĢåµÄĆÜ¶Č²»±ä |
| C£®»ģŗĻĘųĢåµÄĻą¶ŌĘ½¾ł·Ö×ÓÖŹĮæ²»±ä | D£®CH3OH”¢CO”¢H2µÄÅØ¶Č¶¼²»ŌŁ·¢Éś±ä»Æ |
| ĪĀ¶Č | 250”ę | 300”ę | 350”ę |
| K | 2.041 | 0.270 | 0.012 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com