
| A�� | 3Cl2��g��+8NH3��g���T6NH4Cl��s��+N2��g���ڳ��������Է����У���÷�Ӧ�ġ�H��0 | |
| B�� | ��⾫��ͭʱ�����Һ��CuSO4�����ʵ���Ũ�Ȳ��� | |
| C�� | �����£������pH����ͬ��HA��HB������ֱ���������п��Ӧ��HA�ų������࣬˵�����ԣ�HB��HA | |
| D�� | N2��g��+3H2��g��?2NH3��g����H��0��������������ʱ�����¶ȣ���Ӧ����v��H2����������ƽ��ת���ʾ����� |
���� A��3Cl2��g��+8NH3��g���T6NH4Cl��s��+N2��g����S��0����G=��H-T��S���ڳ��������Է����У���÷�Ӧ�ġ�H��0��
B����⾫��ͭʱ�������Ȼ��õĽ���Ҫ�ŵ磻
C�������pH����ͬHA��HB������ֱ���������п��Ӧ��HA�ų�����࣬��HA��Ũ�ȴ�
D�������¶ȣ�ƽ�������ȷ����ƶ���
��� �⣺A��3Cl2��g��+8NH3��g���T6NH4Cl��s��+N2��g����S��0����G=��H-T��S���ڳ��������Է����У���÷�Ӧ�ġ�H��0����A��ȷ��
B����⾫��ͭʱ�������Ȼ��õĽ���Ҫ�ŵ磬���Ե��Һ��CuSO4�����ʵ���Ũ�ȼ�С����B����
C�������pH=3��HA��HB������ֱ���������п��Ӧ��HA�ų�����࣬��HA��Ũ�ȴ�HAΪ���ᣬ��������HB��HA����C��ȷ��
D��N2��g��+3H2��g��?2NH3��g����H��0����ӦΪ���ȷ�Ӧ�������¶�ƽ��Ӧ�����ȷ����ƶ������������ƶ���������ת���ʽ��ͣ���D����
��ѡAC��
���� ���⿼���Ϊ�ۺϣ��漰����ʹ���ԭ������Ӧ���Է��Լ�Ӱ�췴Ӧ���ʵ����أ���ѧƽ���ƶ���Ӱ�����ص����⣬���ؿ���ѧ���ۺ����û�ѧ֪ʶ����������Ŀ�ѶȲ���


 ��1����Ԫ�¿�������ĩϵ�д�
��1����Ԫ�¿�������ĩϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
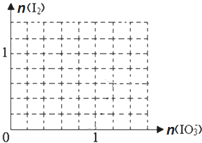 �����������У�±��Ԫ�أ�F��Cl��Br��I���ĵ��ʼ���������;�㷺��
�����������У�±��Ԫ�أ�F��Cl��Br��I���ĵ��ʼ���������;�㷺��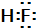 ����HF��HCl��������з����HF�ķ�����������
����HF��HCl��������з����HF�ķ�����������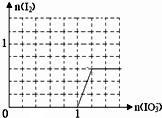 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ϼۣ��ۣ��ڣ��� | B�� | ԭ�Ӱ뾶���ڣ��٣��� | ||
| C�� | �縺�ԣ��ۣ��٣��� | D�� | ��һ�����ܣ��ۣ��ڣ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
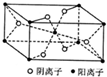 X��Y��Z��RΪǰ������Ԫ�أ���ԭ��������������XY2���γ��������Ҫ����֮һ��Z��̬ԭ�ӵ�M����K���������ȣ�R2+��3d�����9�����ӣ���ش��������⣺
X��Y��Z��RΪǰ������Ԫ�أ���ԭ��������������XY2���γ��������Ҫ����֮һ��Z��̬ԭ�ӵ�M����K���������ȣ�R2+��3d�����9�����ӣ���ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.1 mol•L-1 AgNO3��Һ��H+��K+��SO42-��I- | |
| B�� | ʹ���ȱ�����Һ�У�Fe2+��Al3+��NO3-��Cl-��S2- | |
| C�� | $\frac{Kw}{c��H+��}$=0.1 mol•L-1����Һ��Na+��K+��SiO32-��AlO2- | |
| D�� | ������Ӧ��������H2����Һ�У�Na+��NH4+��C6H5O-��CH3COO- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
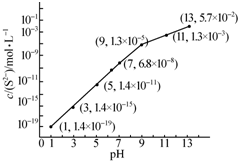 �о���Ԫ�ؼ��仯��������ʾ�����Ҫ���壮
�о���Ԫ�ؼ��仯��������ʾ�����Ҫ���壮| Ka1 | Ka2 | |
| H2SO3 | 1.3��10-2 | 6.3��10-4 |
| H2CO3 | 4.2��10-7 | 5.6��10-11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | x+10 | B�� | x+26 | C�� | x-34 | D�� | x-24 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
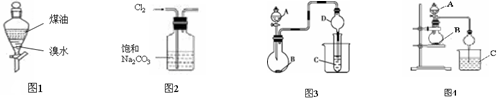 ��������
��������| A�� | ����ͼ1��ɡ���ú������ȡ��ˮ�е�Br2����������ã��ϲ��Ⱥ�ɫ���²㼸����ɫ | |
| B�� | ʵ������ȡ����Cl2������ͼ2װ�ó�ȥCl2�е�HCl�������� | |
| C�� | ͼ3�У���A��B��C�ֱ�ΪŨ���ᡢNa2SO3���塢ʯ����Һ����C����Һ�ȱ�����ɫ | |
| D�� | ͼ4�У���AΪŨ��ˮ��BΪ��ʯ�ң�C������ϡ��Һ��ʵ���пɿ���C���ȱ���Ǻ����壬˵��AgOH�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
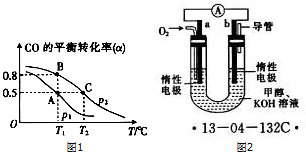
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com