
【题目】下列物质分类中,前者包括后者的是( )
A.电解质 石墨
B.胶体 分散系
C.混合物 漂白粉
D.碱性氧化物 CO2
科目:高中化学 来源: 题型:
【题目】茉莉花香气的成分有多种,有机物E(C9H10O2)是其中的一种,它可以从茉莉花中提取,也可以用酒精和苯的某一同系物(C7H8)为原料进行人工合成,合成路线如下:
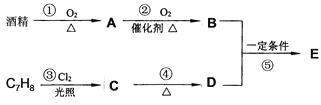
已知:D与酒精具有相同的含氧官能团,E为酯。
完成下列填空:
(1)下列物质中官能团的名称是:B___________________,C___________________。
(2)③的有机反应类型是:_______________________, 反应①、④发生还需要的试剂分别是:反应①___________________,反应④______________________。
(3)反应⑤的化学方程式为:___________________________________________________。
(4)E的同分异构体中,苯环上只有一个取代基,并包含一个酯基的结构有多个,下面是其中2个的结构简式: ![]() 、
、![]() ,请再写出2个符合上述要求的E的同分异构体结构简式:______________和 _____________。
,请再写出2个符合上述要求的E的同分异构体结构简式:______________和 _____________。
(5)请写出以CH2=CHCH2CH3为唯一有机原料制备![]() 的合成路线_________(无机试剂任用)。
的合成路线_________(无机试剂任用)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)![]() 2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据图示得出的判断结论正确的是
2AB3(g)化学平衡状态的影响,得到如下图所示的变化规律(图中T表示温度,n表示物质的量),根据图示得出的判断结论正确的是
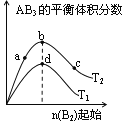
A. 反应速率a>b>c
B. 达到平衡时A2的转化率大小为:b>a>c
C. 若T2>T1,则正反应是吸热反应
D. 达到平衡时,AB3的物质的量大小为:c>b>a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中含有丰富的镁资源。某同学设计从模拟海水中制备MgO的实验方案:
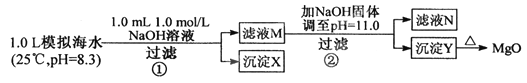
模拟海水中的离子浓度/mol·L-1 | Na+ | Mg2+ | Ca2+ | Cl- | HCO3- |
0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
【注】溶液中某种离子的浓度小于1.0![]() 10-5mol
10-5mol![]() L-,可认为该离子不存在。
L-,可认为该离子不存在。
实验过程中,假设溶液体积不变。已知:
Ksp(CaCO3)=4.96![]() 10-9 Ksp(MgCO3)=2.1
10-9 Ksp(MgCO3)=2.1![]() 10-5
10-5
Ksp(Ca(OH)2)=4.68![]() 10-6 Ksp(Mg(OH)2)=5.61
10-6 Ksp(Mg(OH)2)=5.61![]() 10-12
10-12
下列说法正确的是
A. 沉淀物x为CaCO3
B. 滤液M中存在Mg2+ ,不存在Ca2+
C. 滤液N中存在Mg2+ , Ca2+
D. 步骤②中应改为加入4.2g NaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】气体的体积主要由以下什么因素决定:( )
①气体的分子多少 ②气体分子的大小
③气体分子间的平均距离 ④气体分子的相对分子质量.
A.①②
B.①③
C.②③
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物麻黄碱和牛磺酸的结构简式如图。有关麻黄碱、牛磺酸的叙述正确的是

A. 分子式分别为 C10H16ON、C2H7NO2S
B. 均能与金属钠及氢氧化钠溶液反应
C. 均能发生取代反应,麻黄碱还能发生加成反应
D. 牛磺酸与HSCH2CH( NH2)COOH( 半胱氨酸) 互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A、B和气体甲、乙、丙以及物质C、D、E、F,它们之间能发生如下反应。(图中有些反应的产物和反应条件没有标出)

请回答下列问题:
(1)A的化学式为_____________,丙的化学式为_____________;
(2)写出下列反应的离子方程式:
① _________________________________________;
④ _________________________________________;
⑤ _________________________________________。
(3)写出C溶液与Al反应的化学方程式____________________。
(4)浓硫酸具有强氧化性却可以用B材料车运输,是因为_________________。
(5)为鉴定B单质,将试样用稀盐酸溶解,取上层清液后需再加入的试剂(填写字母代号)是_____________。
A. 碘水 B. NaOH溶液 C. KSCN溶液 D. Na2SO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于化学平衡常数(K),电离平衡常数(Ka或Kb),水解平衡常数(Kh),沉淀溶解平衡常数(Ksp),水的离子积常数(Kw)的叙述中错误的是( )
A. K、Ka或Kb、Kh、Ksp、Kw都与温度有关,温度越高,常数值越大
B. 比较Ksp与离子积Qc的相对大小,可判断难溶解电解质在给定条件下沉淀能否生成或溶解
C. K值越大,正反应进行的程度越大,一般地说,K>105时,该反应进行得就基本完全了
D. 弱酸HA的Ka与NaA的Kh、水的离子积常数Kw三者间的关系可表示为:Kw=Ka·Kh
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com