
| A、0.01mol?L-1醋酸溶液 |
| B、0.02mol?L-1醋酸与0.01mol?L-1NaOH溶液等体积混合液 |
| C、0.03mol?L-1醋酸与0.01mol?L-1NaOH溶液等体积混合液 |
| D、pH=2的盐酸与pH=12NaOH溶液等体积混合液 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SiO2既能与HF溶液反应,又能与NaOH溶液反应,说明SiO2是两性氧化物 |
| B、用大理石和浓盐酸反应制取CO2气体,立即通入一定浓度的Na2SiO3溶液中,出现白色沉淀证明H2CO3的酸性比H2SiO3的酸性强 |
| C、向某溶液中滴加硝酸酸化的Ba(NO3)2溶液产生白色沉淀,说明该溶液中含有SO42- |
| D、相同体积pH均为3的HA和HB两种酸分别与足量的锌充分反应,HA放出的氢气多,说明HB的酸性比HA的酸性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③④ | B、①②③ |
| C、②③ | D、② |
查看答案和解析>>
科目:高中化学 来源: 题型:
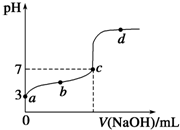 现有浓度均为0.1mol?L-1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、
现有浓度均为0.1mol?L-1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、| c(CH3COO-)?c(H+) |
| c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| n(CH4) |
| n(N2) |
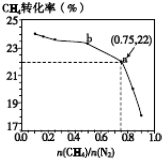
A、
| ||
B、
| ||
| C、b点对应的平衡常数比a点的大 | ||
| D、a点对应的NH3的体积分数约为13% |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、灼烧B,得到红褐色固体,说明B是Fe(OH)3 |
| B、A是NH3 |
| C、固体中至少存在3种成分 |
| D、若向溶液E中通入过量HCl气体,则现象不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com