
| A���������������������ֱ���ȫȼ�գ����߷ų������� |
| B����C��ʯī����C�����ʯ����H=+1.9 kJ?mol-1��֪�����ʯ��ʯī�ȶ� |
| C����ϡ��Һ�У�H++OH-=H2O��H=-57.3 kJ?mol-1��������1 mol CH3COOH�Ĵ�����Һ�뺬1 mol NaOH����Һ��ϣ��ų�������С��57.3 kJ |
| D����101 kPaʱ��2 g H2��ȫȼ������Һ̬ˮ���ų�285.8 kJ����������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ2H2��g��+O2��g��=2H2O��l����H=+285.8 kJ?mol-1 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢ڢ� | B���٢ڢ� |
| C���ڢۢ� | D���ۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����������Ȼ�����Һ��Ӧ����ɫ |
| B����������Ũ������ܳʻ�ɫ |
| C���Ϻ�ɫ�ĵ�����������Ȼ�̼�ʻƺ�ɫ |
| D��˫�����Լ��뵰������Һ��Ӧ���õ����ɫ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A | B | C | D | |
| ʵ��������װ�� | 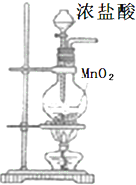 |  NaOH��Һ NaOH��Һ | 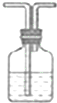 Ũ���� Ũ���� | 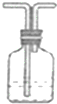 ����ʳ��ˮ ����ʳ��ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2Fe3++SO2+2H2O�T2Fe2++SO42-+4H+ |
| B��I2+SO2+2H2O�TH2SO4+2HI |
| C��H2O2+2H++SO42-�TSO2��+O2��+2H2O |
| D��2Fe3++2I-�T2Fe2++I2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��33.6 L |
| B��11.2 L |
| C��22.4 L |
| D��44.8 L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A | B | C | D | |
| ǿ����� | NaCl | H2SO4 | CaCO3 | HNO3 |
| ������� | HF | BaSO4 | HClO | CH3COOH |
| �ǵ���� | Cl2 | CS2 | C2H5OH | H2S |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com