
| A. | 1 mol H2SO4与1 mol Ba(OH)2完全中和所放出的热量为中和热 | |
| B. | 强酸和强碱的稀溶液发生中和反应一定是放热反应,弱酸和弱碱反应一定也是放热反应 | |
| C. | CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO2,故反应一定是吸热反应 | |
| D. | 酸和碱发生中和反应生成1 mol 水,这时的反应热叫中和热 |
分析 A.中和热是指强酸、强碱生成1mol水放出的热量;
B、酸碱中和反应一定是放热反应;
C、CO和氧气反应生成稳定的CO2的反应属于放热反应;
D、中和热是指稀的强酸、强碱生成1mol水放出的热量,据此回答.
解答 解:A、1 mol 硫酸与1mol Ba(OH)2 完全中和生成硫酸钡沉淀和2molH2O,同时SO42-和Ba2+反应生成BaSO4,需要放出热量,所以放出的热量不是中和热,故A错误;
B、酸碱中和反应一定是放热反应,强酸和强碱的稀溶液发生中和反应一定是放热反应,弱酸和弱碱反应一定也是放热反应,故B正确;
C、CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO2,反应一定是放热反应,故C错误;
D、稀的强酸、强碱生成1mol水放出的热量叫中和热,故D错误.
故选B.
点评 本题涉及中和热的概念以及反应热效应的判断知识,属于综合知识的考查,难度中等.


科目:高中化学 来源: 题型:填空题
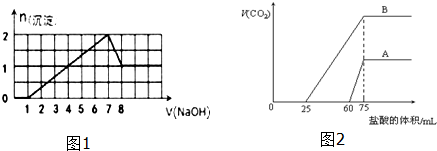
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
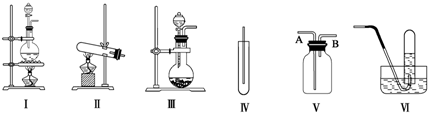
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
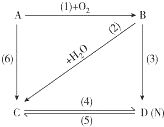 图中A是一种金属单质,B是淡黄色固体,D的焰色反应呈黄色;试指出A、B、C、D是何种物质,并写出有关的化学方程式:
图中A是一种金属单质,B是淡黄色固体,D的焰色反应呈黄色;试指出A、B、C、D是何种物质,并写出有关的化学方程式:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
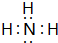 .实验室制取该种物质的化学方程式为Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$ 2NH3↑+CaCl2+2H2O.
.实验室制取该种物质的化学方程式为Ca(OH)2+2NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$ 2NH3↑+CaCl2+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | He | B. | S | C. | Si | D. | P |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上,用焦炭在电炉中还原二氧化硅得到含杂质的粗硅 | |
| B. | 煤经过气化和液化两个物理变化,可变为清洁能源 | |
| C. | 如将纳米材料分散到液体分散剂中,该分散系可发生丁达尔现象,由此可推测纳米材料的直径为1~100 nm之间 | |
| D. | 将苦卤浓缩、氧化,鼓入热空气或水蒸气提取海水中的溴,溴元素又称“海洋元素” |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com