
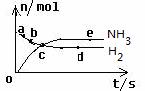
合成氨工业对国民经济和社会发展具有重要意义。对于密闭容器中的 N2(g)+3H2(g) 2NH3(g),在673K 30MPa下,n(NH3)
2NH3(g),在673K 30MPa下,n(NH3)
和n(H2)随时间变化的关系如右图所示。下列叙述正确的是
A.a点的正反应速率比b点的小
B.d点和e点n(N2)不相等
C.c点反应达平衡
D. d点的正反应速率与e点正反应速率相等
 |
科目:高中化学 来源: 题型:
(2013·新课标全国卷Ⅱ,27)氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌[含有Fe(Ⅱ)、Mn(Ⅱ)、Ni(Ⅱ)等杂质]的流程如下:
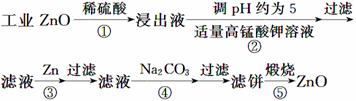
提示:在本实验条件下,Ni(Ⅱ)不能被氧化;高锰酸钾的还原产物是MnO2。
回答下列问题:
(1)反应②中除掉的杂质离子是__________,发生反应的离子方程式为__________;在加高锰酸钾溶液前,若pH较低,对除杂的影响是________________。
(2)反应③的反应类型为____________,过滤得到的滤渣中,除了过量的锌外还有______________。
(3)反应④形成的沉淀要用水洗,检验沉淀是否洗涤干净的方法是________________。
(4)反应④中产物的成分可能是ZnCO3·xZn(OH)2,取干燥后的滤饼11.2 g,煅烧后可得到产品8.1 g,则x等于__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
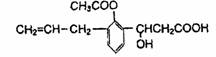
有机物的结构简式如下图:则此有机物可发生的反应类型有:
①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦中和
A.①②③⑤⑥ B.②③④⑤⑥
C.①②③④⑤⑥⑦ D.②③④⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
长效碳酸氢铵是我国自主开发的一种新型化肥,工业生产碳酸氢铵的工艺流程如下:
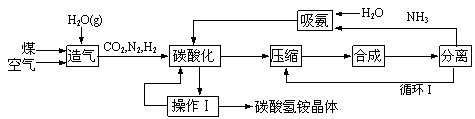 |
根据题意回答下列问题:
(1)操作Ⅰ有多步组成,包括冷却、过滤、洗涤、干燥;实验室进行过滤操作用到的玻璃仪器有___________,实验室进行该洗涤操作时宜用酒精代替水洗涤,理由是____________;
(2)分离工序是将氨从反应混合物中分离出来,其分离原理利用了氨的_________性质,设计循环Ⅰ的目的是_______________________________________;
(3)造气工序包括脱硫过程,目的是除去气体中的SO2等气体,实验室进行此操作可选用的试剂是________(填写编号);
A.NaHCO3溶液 B. NaOH溶液 C.Ca(OH)2溶液 D.Na2SO3溶液
(4)实验室实现吸氨过程可以是下列装置中的_____________(填写编号);

A. B. C. D.
(5)索尔维创建氨碱法不久后的1898年, 施莱信(Schlosing)就提出用碳酸氢铵固体与氯化钠饱和溶液作用生成碳酸氢钠再加热制纯碱的方法。写出生成碳酸氢钠的化学方程式:______________________________________; 为了进一步提纯碳酸氢钠晶体,可采用的方法有:________(填写编号);
A. 加热灼烧法 B. 重结晶法 C.酸中和法 D. 碱沉淀法
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关元素的性质及其递变规律正确的是
A.同周期金属元素的化合价越高,其原子失电子能力越强
B.第二周期元素从左到右,最高正价从+1递增到+7
C.同主族元素的简单阴离子还原性越强,则该元素对应的气态氢化物稳定性越强
D.IA族与VIIA族元素间可形成共价化合物或离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
(1) 在这些元素中,化学性质最不活泼的是_____________ (填具体元素符号,下同)。
(2) 在最高价氧化物的水化物中,酸性最强的化合物的分子式是_______,碱性最强的化合物的化学式是_____________。
(3) 最高价氧化物是两性氧化物的元素是_____________;写出它的氧化物与氢氧化钠反应的离子方程式____________________________________________。
(4) 元素④与⑥形成的化合物属于__________________(填 “共价”或“离子”)化合物。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W是短周期元素,X元素原子的最外层未达到8电子稳定结构,工业上通过分离液态空气获得其单质;Y元素原子最外电子层上s、p电子数相等;Z元素+2价阳离子的核外电子排布与氖原子相同;W元素原子的M层有1个未成对的p电子。下列说法一定正确的是 ( )
A.Z元素的单质在一定条件下能与X元素的单质反应
B.Z元素的离子半径大于W元素的离子半径
C.X元素的氢化物的水溶液显碱性
D.Y元素最高价氧化物的晶体具有很高的熔点和沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
相同质量的下列物质分别与等浓度的NaOH溶液反应,至体系中均无固体物质,消耗碱量最多的是 ( )
A.Al B.Al(OH)3
C.AlCl3 D.Al2O3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com