
【题目】已知乙烯能发生以下转化:

(1)乙烯的结构简式为: 。
(2)写出B、D化合物中官能团的名称:B ;D ;
(3)写出反应的化学方程式
①: 反应类型:
②: 反应类型:
③: 反应类型:
【答案】
(1)CH2 =CH2 ;
(2)羟基、羧基;
(3)①CH2 =CH2 + H2O![]() CH3CH2OH ;加成反应② 2CH3CH2OH+O 2
CH3CH2OH ;加成反应② 2CH3CH2OH+O 2 ![]() 2CH3CHO+2H2O;氧化反应,CH3CH2OH+CH3COOH
2CH3CHO+2H2O;氧化反应,CH3CH2OH+CH3COOH ![]() CH3COOCH2CH3+H2O ;酯化反应(取代反应)。
CH3COOCH2CH3+H2O ;酯化反应(取代反应)。
【解析】
试题分析:(1)乙烯分子中的2个C原子之间形成2对共用电子对,每个C原子再与2个H原子形成2对共用电子对,其结构简式为CH2 =CH2 ;(2)乙烯与水发生加成反应产生B是乙醇,官能团是—OH;乙醇和乙酸D发生反应产生乙酸乙酯和水,所以化合物D中官能团的名称羧基;(3)①乙烯与水发生加成反应产生乙醇,反应的化学方程式是CH2 =CH2 + H2O![]() CH3CH2OH ;②乙醇与O2在Cu或Ag作催化剂时发生氧化反应产生乙醛和水,反应的化学方程式是2CH3CH2OH+O 2
CH3CH2OH ;②乙醇与O2在Cu或Ag作催化剂时发生氧化反应产生乙醛和水,反应的化学方程式是2CH3CH2OH+O 2 ![]() 2CH3CHO+2H2O;③乙醇与乙酸在浓硫酸存在时,在加热条件下发生酯化反应,产生乙酸乙酯和水,反应的化学方程式是:CH3CH2OH+CH3COOH
2CH3CHO+2H2O;③乙醇与乙酸在浓硫酸存在时,在加热条件下发生酯化反应,产生乙酸乙酯和水,反应的化学方程式是:CH3CH2OH+CH3COOH ![]() CH3COOCH2CH3+H2O。
CH3COOCH2CH3+H2O。


科目:高中化学 来源: 题型:
【题目】6种相邻周期主族元素的相对位置如下表,M元素原子核外电子数是Y元素原子核外电子数的2倍,W元素原子的次外层电子数是最外层电子数的2倍。用化学用语回答下列问题:

(1)Y在周期表中的位置是________。
(2)X、Y、Z三种元素的原子半径由大到小的顺序是________。
(3)W、M、Q三种元素最高价氧化物对应的水化物中,酸性由强到弱的顺序是________。
(4)W的最高价氧化物可以和Z的氢化物反应,利用该反应可刻蚀玻璃,反应的化学方程式是________。
(5)X的含10个电子 的气态氢化物甲是一种重要的化工原料。甲的电子式是 ,实验室制备甲的化学方程式是________, X的含18个电子的气态氢化物丙可与空气构成一种环保型碱性燃料电池,电池工作时丙发生的电极反应方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)第二周期元素中,第一电离能介于B和O之间的元素有 。
(2)N、O可以组成微粒NO2+,它的电子式为 ,其等电子体有 (至少2种)。
(3)元素金(Au)处于周期表中的第六周期,与Cu同族,Au原子外围电子排布式为______;
(4)某有机物结构如下图所示,其分子中的原子除H外有 个以sp3杂化,2mol该分子含有π键的数目为

(5)已知Ti3+可形成配位数为6的配合物。现有含钛的两种颜色的晶体,一种为紫色,另一种为绿色,但相关实验证明,两种晶体的组成皆为TiCl3·6H2O。为测定这两种晶体的化学式,设计了如下实验:
a.分别取等质量的两种配合物晶体的样品配成待测溶液;
b.分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c.沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现紫色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为绿色晶体的水溶液反应得到沉淀质量的1.5倍。则绿色晶体配合物的化学式为 。(表示出内界和外界)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了预防碘缺乏症,国家规定每千克食盐中应含有40~50 mg碘酸钾。碘酸钾晶体具有较高的稳定性,但在酸性溶液中,碘酸钾是一种较强的氧化剂,能跟某些还原剂反应生成碘;在碱性溶液中,碘酸钾能被氯气、次氯酸等更强的氧化剂氧化为更高价的碘的含氧酸盐。工业生产碘酸钾的流程如图所示。
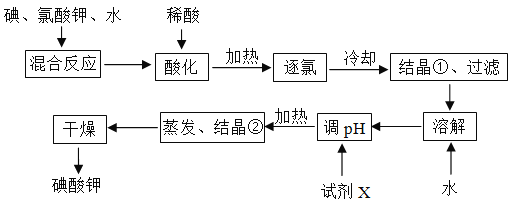
(1)碘在周期表中的位置为__________________;
(2)碘、氯酸钾、水混合反应时,若两种还原产物所得电子的数目相同,请配平该反应的化学方程式:____I2+____KClO3+____H2O=____KH(IO3)2+____KCl+____Cl2↑;
(3)混合反应后,用稀酸酸化的作用是___________________________,在稀盐酸和稀硝酸中不能选用的酸是_________,理由是__________________________________;
(4)试剂X的化学式为__________,写出用试剂X调pH的化学方程式__________________;
(5)如果省略“酸化”、“逐氯”、“结晶①、过滤”这三步操作,直接用试剂X调整反应混合物的pH,对生产碘酸钾有什么影响?________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)已知断裂1mol C—H键,要吸收热量414.4 kJ;断裂1 mol C—C键,要吸收热量347.4 kJ;生成1 mol C===C键,会放出热量615.3 kJ;生成1 mol H—H键,会放出热量435.3 kJ。某有机物分解的反应可表示为:

若在反应中消耗了1 mol乙烷,则有关该反应的说法正确的是
A.该反应放出251.2 kJ的热量
B.该反应吸收251.2 kJ的热量
C.该反应放出125.6 kJ的热量
D.该反应吸收125.6 kJ的热量
(二)如图所示的原电池,一段时间后某极析出1.28g的固体。回答下列问题:

(1)正极是 (填“锌”或“银”),发生了 反应。
(2)正极的电极反应为 。
(3)上述过程中共转移电子 mol。
(4)锌片的质量 (填“增加”或“减少”) g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ如图所示:已知甲、乙、丙常温下都为气体。
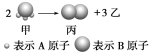
(1)乙气体的分子式 。(用A、B表示,A、B可以选择性使用)
(2)若测得生成物的混合气体对氢气的相对密度为d,则甲的摩尔质量为 。(用d表示)
(3)标准状况下,11.2L甲气体溶于500mL水中,所得溶液的密度为ρg/cm3,则所得溶液中甲的物质的量浓度为 (用d、ρ表示)(甲的摩尔质量用(2)中的数据)。
Ⅱ完成下列离子方程式。
(1)贝壳溶于醋酸溶液: 。
(2)向氢氧化钡溶液中加入少量小苏打溶液: 。
(3)碳酸氢铵和足量浓烧碱溶液混合: 。
(4)向次氯酸钠溶液中通足量SO2气体: 。
(5)向溴化亚铁溶液中通入足量氯气: 。
(6)向偏铝酸钠溶液中通入足量CO2气体: 。
(7)向硫酸亚铁溶液中加入酸性高锰酸钾溶液: 。
(8)金属锌和硫酸、三氧化二砷反应生成砷化氢: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 常温下,醋酸和氨水的电离平衡常数均为1.8×10-5。向10mL浓度为0.1molL-1的NH3H2O溶液中滴加相同浓度的CH3COOH(温度变化忽略不计),在滴加过程中( )
A.c(NH4+)与c(NH3H2O)之和始终保持不变
B.水的电离程度始终增大
C.![]() 始终减小
始终减小
D.当加入CH3COOH的体积为10mL时,溶液pH>7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸铜晶体,俗称蓝矾、胆矾,具有催吐,祛腐,解毒。取5.0 g胆矾样品逐渐升高温度使其分解,分解过程的热重如下表。回答下列问题:
温度范围/℃ | 固体质量/g |
258~680 | 3.20 |
680~1000 | 1.60 |
1000以上 | 1.44 |
(1)测定蓝矾属于晶体的物理方法是____________。其中SO42-中S原子的轨道杂化形式是____________;H2O的空间构型是__________________。
(2)将硫酸铜晶体加热到258~680℃生成的物质A,A是__________(化学式);A溶于水配成溶液,加入氨水,观察到的现象是_____________________________________________;最终得到溶液中的含铜元素的离子是_________________(化学式),该离子含有的化学键类型有___________________。
(3)将硫酸铜晶体加热到1000℃以上生成的物质C,在C中的铜的离子的基态电子排布式是____________;
(4)如图是硫酸铜晶体分解得到一定温度的产物的晶胞(白球和黑球代表不同的原子)。
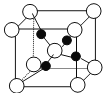
①该温度是_______________。
②铜原子的配位数是_______________。
③已知该晶体的密度为dg·cm-3,则晶胞参数是_________________pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在容积固定的某密闭容器中发生反应N2+3H2![]() 2NH3。在10s内N2的浓度由5 mol·L-1降至4 mol·L-1,下列说法正确的是( )
2NH3。在10s内N2的浓度由5 mol·L-1降至4 mol·L-1,下列说法正确的是( )
A. 用NH3表示的化学反应速率为0.1 mol·L-1·s-1
B. 使用合适的催化剂,可以加快该反应的速率
C. 增加H2的浓度或降低温度都会加快该反应速率
D. 反应足够长时间,N2、H2中至少有一种物质浓度降为零
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com