
”¾ĢāÄæ”æÅäÖĘŅ»¶ØĪļÖŹµÄĮæÅØ¶ČµÄNaOHČÜŅŗŹ±£¬µ¼ÖĀÅضČĘ«øßµÄŌŅņæÉÄÜŹĒ (””””)
A. ŅĘŅŗŹ±£¬²»É÷½«ŅŗĢåĮ÷µ½ĘæĶā B. ČŻĮæĘæŹ¢¹żNaOHČÜŅŗ£¬Ź¹ÓĆĒ°Ī“Ļ“µÓ
C. ČŻĮæĘæÖŠŌÓŠÉŁĮæµÄÕōĮóĖ® D. ¶ØČŻŹ±ŃöŹÓæĢ¶ČĻß
 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠø÷×éĄė×Ó£¬ÄÜŌŚÖø¶ØČÜŅŗÖŠ“óĮæ¹²“ęµÄŹĒ£Ø £©
A.ĪŽÉ«ČÜŅŗÖŠ£ŗNa+”¢MnO4©”¢CO32©”¢Cl©
B.ÄÜŹ¹×ĻÉ«ŹÆČļŹŌ¼Į±äŗģµÄČÜŅŗÖŠ£ŗOH©”¢K+”¢Ba2+”¢Na+
C.ĶøĆ÷µÄĖįŠŌČÜŅŗÖŠ£ŗFe3+”¢Mg2+”¢Cl©”¢NO3©
D.pH=1µÄČÜŅŗÖŠ£ŗNH4+”¢Fe2+”¢Cl©”¢NO3©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ±½¼×ĖįÄĘ£ØNaA£©æÉÓĆ×÷ŅūĮĻµÄ·ĄøƼĮ£¬ŃŠ¾æ±ķĆ÷±½¼×Ėį£ØHA£©µÄŅÖ¾śÄÜĮ¦ĻŌÖųøßÓŚA© £¬ ŌŚÉś²śĢ¼ĖįŅūĮĻµÄ¹ż³ĢÖŠ£¬³żĮĖĢķ¼ÓNaAĶā£¬»¹Šč¼ÓŃ¹³åČėCO2ĘųĢ壬ŅŃÖŖ25”ꏱ£¬HA”¢H2CO3µÄµēĮ¦Ę½ŗā³£Źż·Ö±šĪŖK=6.25”Į10©5”¢K1=4.3”Į10©7 £¬ ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø²»æ¼ĀĒŅūĮĻÖŠĘäĖū³É·Ö£©£Ø £©
A.ĢįøßCO2³äĘųŃ¹Į¦£¬ŅūĮĻÖŠc£ØA©£©²»±ä
B.µ±pHĪŖ5.0Ź±£¬ŅūĮĻÖŠ ![]() =0.16
=0.16
C.Ļą±ČÓŚĪ“³äCO2µÄŅūĮĻ£¬Ģ¼ĖįŅūĮĻµÄŅÖ¾śÄÜĮ¦½ĻµĶ
D.½įŗĻH+µÄÄÜĮ¦£ŗA©£¾HCO3©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚĢå»ż¾łĪŖ1L£¬pH¾łµČÓŚ2µÄŃĪĖįŗĶ“×ĖįČÜŅŗ£¬·Ö±šĶ¶Čė0.23g Na£¬ŌņĻĀĶ¼ÖŠ±Č½Ļ·ūŗĻ·“Ó¦ŹĀŹµµÄĒśĻߏĒ£Ø £©
A.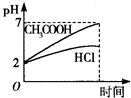
B.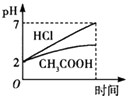
C.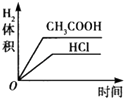
D.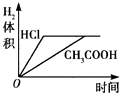
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³ä·ÖĄūÓĆŅŃÓŠµÄŹż¾ŻŹĒ½ā¾ö»ÆѧĪŹĢā·½·ØµÄÖŲŅŖĶ¾¾¶£®¶ŌŹż¾ŻµÄĄūÓĆĒéæöÕżČ·µÄŹĒ
A.ĄūÓĆ»ÆŃ§Ę½ŗā³£ŹżÅŠ¶Ļ»Æѧ·“Ó¦½ųŠŠµÄæģĀż
B.ĄūÓĆČܽā¶ČŹż¾ŻÅŠ¶ĻŃõ»Æ»¹Ō·“Ó¦·¢ÉśµÄæÉÄÜŠŌ
C.ĄūÓĆ·ŠµćŹż¾ŻĶĘ²ā½«Ņ»Š©ŅŗĢå»ģŗĻĪļ·ÖĄėµÄæÉÄÜŠŌ
D.ĄūÓĆĪļÖŹµÄĦ¶ūÖŹĮæÅŠ¶ĻĻąĶ¬×“Ģ¬ĻĀ²»Ķ¬ĪļÖŹĆܶȵēóŠ”
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻĢāŅā½ā“š
£Ø1£©ČÜŅŗÖŠ£¬c£ØH+£©=10©x molL©1 £¬ c£ØOH©£©=10©y molL©1 £¬ xÓėyµÄ¹ŲĻµČēĶ¼1ĖłŹ¾£® 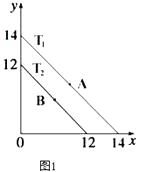
¢ŁČō“ÓAµćµ½Bµć£¬æɲÉČ”µÄ“ėŹ©ĪŖ
¢ŚT2”ꏱ£¬½«pH=0µÄNaHSO4ČÜŅŗÖšµĪµĪ¼Óµ½pH=2 µÄ“×ĖįČÜŅŗÖŠ£¬ŌņĖ®µēĄė³öµÄc£ØOH©£©½«£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±”¢”°²»±ä”±£©£®
¢ŪŅŃÖŖ£ŗT1”ꏱ£¬“×ĖįµÄµēĄė³£ŹżĪŖ 1.8”Į10©5 £¬ Ōņ T1”ꏱ£¬ŌŚ 0.5molL©1µÄ“×ĖįČÜŅŗÖŠÓÉ“×ĖįµēĄė³öµÄ c£ØH+£©Ō¼ŹĒĖ®µēĄė³öµÄ c£ØH+£©µÄ±¶ £®
¢ÜT2”ꏱ£¬½«Ä³ČÜŅŗ£Ø“ĖČÜŅŗĀś×ć lg[ ![]() ]=10£©µĪČėŗ¬ Na+”¢HS©”¢SO42©”¢K+µÄČÜŅŗÖŠ£¬·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ £®
]=10£©µĪČėŗ¬ Na+”¢HS©”¢SO42©”¢K+µÄČÜŅŗÖŠ£¬·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ £®
£Ø2£©Ģå»ż¾łĪŖ1mL pH=2µÄŅ»ŌŖĖįHAŗĶHB£¬¼ÓĖ®Ļ”ŹĶ¹ż³ĢÖŠpHÓėČÜŅŗĢå»ż¹ŲĻµČēĶ¼2ĖłŹ¾£ŗ 
¢ŁmµÄȔֵĪŖ £®
¢ŚaµćĖįµÄÅضČbµćĖįµÄÅØ¶Č£ØĢī”°£¾”±”¢”°£¼”±”¢”°=”±£©£®
¢ŪČō m£¼4£¬³£ĪĀĻĀaµćµ½cµćµÄ¹ż³ĢÖŠ£¬ĻĀĮŠ±ķ“ļŹ½µÄŹż¾Ż±ä“óµÄŹĒ £®
A£®c£ØA©£© B£®n£ØH+£©n£ØOH©£© C£® ![]() D£®
D£® ![]()
£Ø3£©ŅŃÖŖ£ŗ25”ꏱ£¬HCN”¢H2CO3 µÄµēĄėĘ½ŗā³£Źż·Ö±šĪŖK=4.9”Į10©10 £¬ K1=4.3”Į10©7”¢K2=5.6”Į10©11 £¬ ĻņNaCNČÜŅŗÖŠĶØČėÉŁĮæCO2 £¬ Ėł·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøßĪĀĮŃ½ā·Ø“¦Ąķ¹¤Ņµ·ĻĮņĖįµÄŌĄķĪŖ£ŗ2H2SO4£Øl£©=2SO2£Øg£©+O2£Øg£©+2H2O£Øg£©”÷H=+550kJ/mol£¬ĖüÓÉĮ½²½·“Ó¦×é³É£ŗ
i£®H2SO4£Øl£©=SO3£Øg£©+H2O£Øg£©”÷H=+177kJ/mol
ii£®SO3£Øg£©·Ö½ā£®
£Ø1£©SO3£Øg£©·Ö½āµÄČČ»Æѧ·½³ĢŹ½ĪŖ
£Ø2£©¹¤ŅµÉĻ³£ÓĆSO2ÖʱøNa2S2O3 £¬ Ļņ0.1mol/LµÄNa2S2O3ČÜŅŗÖŠµĪ¼ÓĻ”ĮņĖįµÄĄė×Ó·½³ĢŹ½ĪŖ £®
£Ø3£©·“Ó¦iiµÄ”÷S0 £ØĢī”°£¾”±”¢”°£¼”±”¢”°=”±£©£®
£Ø4£©¶Ō·“Ó¦ii£¬æÉÓĆV2O5×÷“߻ƼĮ£® ŅŃÖŖ£ŗSO2+V2O5SO3+V2O4K1”¢ ![]() O2+V2O4V2O5K2 £¬ ŌņŌŚĻąĶ¬ĪĀ¶ČĻĀ£¬2SO3£Øg£©2SO2£Øg£©+O2£Øg£©µÄĘ½ŗā³£Źż K=£ØÓĆK1”¢K2±ķŹ¾£©£®
O2+V2O4V2O5K2 £¬ ŌņŌŚĻąĶ¬ĪĀ¶ČĻĀ£¬2SO3£Øg£©2SO2£Øg£©+O2£Øg£©µÄĘ½ŗā³£Źż K=£ØÓĆK1”¢K2±ķŹ¾£©£®
£Ø5£©L£ØL1”¢L2£©£¬XæÉ·Ö±š“ś±ķŃ¹Ēæ»ņĪĀ¶Č£¬ČēĶ¼±ķŹ¾LŅ»¶ØŹ±£¬·“Ó¦iiÖŠSO3£Øg£©µÄĘ½ŗā×Ŗ»ÆĀŹĖęXµÄ±ä»Æ¹ŲĻµ£® 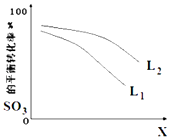
¢ŁX“ś±ķµÄĪļĄķĮæŹĒ£»
¢Ś±Č½ĻL1”¢L2µÄ“óŠ” £®
£Ø6£©Ī¬³ÖĢåĻµ×ÜŃ¹pŗć¶Ø£¬ŌŚT”ꏱ£¬ĪļÖŹµÄĮæĪŖ9mol”¢Ģå»żĪŖ2LµÄSO3£Øg£©·¢Éś·“Ó¦£ŗ2SO3£Øg£©2SO2£Øg£©+O2£Øg£©£¬ŅŃÖŖSO3µÄĘ½ŗā×Ŗ»ÆĀŹ25%£¬ŌņŌŚøĆĪĀ¶ČĻĀ·“Ó¦µÄĘ½ŗā³£ŹżK=£ØÓĆ×ī¼ņ·ÖŹż±ķŹ¾£©£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ±ź×¼×“æöĻĀ£¬½«22.4L HClĶźČ«ČÜÓŚ1LĖ®ÖŠ£ØĖ®µÄĆÜ¶Č½üĖĘĪŖ1g/mL£©£¬ČÜŅŗµÄĆܶČĪŖ¦Ń g/cm3 £¬ ČÜŅŗµÄĢå»żĪŖV mL£¬ČÜÖŹµÄÖŹĮæ·ÖŹżĪŖw£¬ČÜÖŹµÄĪļÖŹµÄĮæÅضČĪŖc mol/L£®ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ£Ø £©
¢Łw= ![]() ”Į100% c=1molL©1 ĻņÉĻŹöČÜŅŗÖŠŌŁ¼ÓČėV mLĖ®ŗó£¬ĖłµĆČÜŅŗµÄÖŹĮæ·ÖŹż“óÓŚ0.5w ĖłµĆČÜŅŗÖŠŗ¬ÓŠNAøöHCl·Ö×Ó£®
”Į100% c=1molL©1 ĻņÉĻŹöČÜŅŗÖŠŌŁ¼ÓČėV mLĖ®ŗó£¬ĖłµĆČÜŅŗµÄÖŹĮæ·ÖŹż“óÓŚ0.5w ĖłµĆČÜŅŗÖŠŗ¬ÓŠNAøöHCl·Ö×Ó£®
A.Č«²æ
B.¢Ł¢Ū¢Ü
C.¢Ł¢Ū
D.Ö»ÓŠ¢Ł
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĪļÖŹŹōÓŚ“æ¾»ĪļµÄŹĒ
A. ĒąĶB. CuSO45H2OC. Ė®²£Į§D. Fe(OH)3½ŗĢå
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com