
| A、浓氨水可检验氯气管道泄漏 |
| B、明矾可用作除去污水中悬浮颗粒的絮凝剂 |
| C、Si和SiO2都用于制造光导纤维 |
| D、硬铝、青铜和不锈钢都属合金 |


科目:高中化学 来源: 题型:
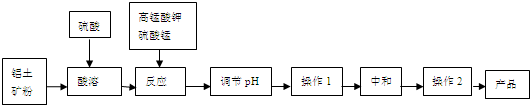
| n(MnO2) |
| n(Fe) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaCl2=Ca2++2Cl- |
| B、Ba(OH)2=Ba2++2OH- |
| C、HNO3=H++NO3- |
| D、NaHCO3=Na++H++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Ba2+、Cl-、NO3- |
| B、K+、Na+、Br-、S2- |
| C、H+、Fe3+、I-、NO3- |
| D、Na+、Ba2+、OH-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D |
| 淀粉--混合物 | 液氯--非电解质 | 苯酚--有机物 | 水晶--分子晶体 |
| 胆矾--纯净物 | 碳酸钙--强电解质 | 纯碱--盐 | 食盐--离子晶体 |
| 盐酸--化合物 | 醋酸--弱电解质 | 水--氧化物 | 金刚石--原子晶体 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
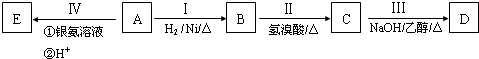
 ,由单体F制有机玻璃的反应类型是
,由单体F制有机玻璃的反应类型是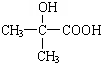 ,写出由G作为单体在一定条件下生成聚酯的化学方程式:
,写出由G作为单体在一定条件下生成聚酯的化学方程式:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com